

Nông Chu Hải
Giới thiệu về bản thân



































Gọi số hạt proton và neutron của nguyên tử X là Px và NX; số hạt proton và neutron của nguyên tử M là PM và NM.
+ Tổng số hạt cơ bản trong hợp chất M2X là 116 hạt nên 2PX + NX + 2PM + NM = 116 (1).
+ Số hạt mang điện trong phân tử M2X nhiều hơn số hạt không mang điện là 36 nên 2PX + 2PM - NX - NM = 36 (2).
+ Số khối của X lớn hơn M là 9 nên (PM + NM) - (PX + NX) = 9 (3).
+ Tổng số hạt trong X2- nhiều hơn trong M+ là 17 nên (2PX + NX + 2) - (2PM + NM - 1) = 17 (4).
Từ (1), (2), (3) và (4), ta có: PM = 11, NM = 12, PX = 16, NX = 16.
Cho 2 hợp chất sau: CO2 và NH3
a) Viết công thức Lewis và công thức cấu tạo của 2 hợp chất trên.
b) Hợp chất nào tan trong nước, hợp chất nào không tan trong nước? Giải thích cụ thể.
Hướng dẫn giải:
a) Công thức Lewis của CO2 là:

Công thức Lewis của NH3 là:

Công thức cấu tạo của CO2 là:
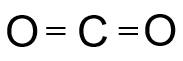
Công thức cấu tạo của NH3 là:

b) NH3 tan trong nước do phân tử NH3 tạo được liên kết hydrogen với phân tử nước, còn CO2 không tan trong nước do phân tử CO2 không tạo được liên kết hydrogen với phân tử H2O.
Cho 2 nguyên tố X và Y có số hiệu nguyên tử lần lượt là 11 và 8.
a) Viết cấu hình electron nguyên tử của X và Y.
b) Dùng sơ đồ biểu diễn sự hình thành liên kết giữa X và Y.
Hướng dẫn giải:
Cho 2 nguyên tố X và Y có số hiệu nguyên tử lần lượt là 11 và 8.
a) Viết cấu hình electron nguyên tử của X và Y.
b) Dùng sơ đồ biểu diễn sự hình thành liên kết giữa X và Y.
a) Cấu hình electron nguyên tử của X (Z = 11) là 1s22s22p63s1.
Cấu hình electron nguyên tử của Y (Z = 8) là 1s22s22p4.
b) Dựa vào cấu hình electron của nguyên tử X và nguyên tử Y, ta thấy X là nguyên tố kim loại (có 1 electron lớp ngoài cùng) và Y là nguyên tố phi kim (có 6 electron lớp ngoài cùng).
Vậy liên kết giữa X và Y là liên kết ion.
Sự tạo thành liên kết giữa X và Y:
X → X+ + 1e
Y + 2e → Y2-
2X+ + Y2- → X2Y
Cho kim loại X thuộc nhóm IIA trong bảng tuần hoàn.
a. Viết công thức hydroxide (Y) tương ứng của X.
b. Hoà tan hoàn toàn 5,832 gam hydroxide Y bởi lượng vừa đủ 73 gam dung dịch HCl 10% thu được dung dịch T. Tìm kim loại X.
Hướng dẫn giải:
a. Công thức hydroxide Y của nguyên tố X thuộc nhóm IIA trong bảng tuần hoàn là X(OH)2.
b. PTHH
X(OH)2 + 2HCl → XCl2 + 2H2O
Khối lượng HCl tham gia phản ứng là:
\(m_{H C l} = 73 \times 10 \% = 7 , 3 g\)
\(n_{H C l} = \frac{7 , 3}{36 , 5} = 0 , 2 \left(\right. m o l \left.\right)\)
⇒ \(n_{X \left(\left(\right. O H \left.\right)\right)_{2}} = \frac{n_{H C l}}{2} = \frac{0 , 2}{2} = 0 , 1 \left(\right. m o l \left.\right)\)
\(M_{X \left(\left(\right. O H \left.\right)\right)_{2}} = \frac{5 , 832}{0 , 1} = 58 , 32 \left(\right. g . m o l^{- 1} \left.\right)\)
\(M_{X} = 58 , 32 - 2 \times m_{O H} = 58 , 32 - 2 \times 34 = 24 , 32\)
Vậy X là nguyên tố Mg.
- Công thức electron của
+ Br2: 
+ CO2: 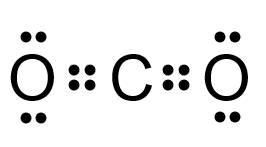
+ C2H4:
- Công thức cấu tạo:
+ Br2: Br \(-\) Br.
+ CO2: O \(=\) C \(=\) O.
+ C2H4: H2C \(=\) CH2.
