

Bùi Thanh Hòa
Giới thiệu về bản thân



































Áp dụng công thức \(v‾=ΔCΔt=0,22−0,14=0,03(Ms)v=ΔtΔC=40,22−0,1=0,03(sM)\)
Áp dụng công thức
\(ΔfH298°=ΣΔfH298°(sp)−ΣΔfH298°(cđ)ΔfH298°=ΣΔfH298°(sp)−ΣΔfH298°(cđ)\)= 2.(-393,5) + 3.(-285,84) - (-84,7) = -1559,82 kJ.
a. PTHH
2KMnO4 + 16HClđặc ----> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Chất khử: HCl
Chất oxi hóa: KMnO4
Quá trình oxi hóa: 2Cl- ---> Cl20 + 2e |x5
Quá trình khử: Mn+7 + 5e ---> Mn+2 |x2
b, nNaI = 0,2.0,1 = 0,02 (mol)
PTHH: 2NaI + Cl2 ---> 2NaCl + I2
mol: 0,02 --> 0,01
=> PTHH: 2KMnO4 + 16HClđặc ----> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
mol: 0,004 <--- 0,01
=> mKMnO4 = n.M = 0,004.158 = 0,632(g)
- NaCl tan tốt trong nước, phân ly hoàn toàn thành ion Na+ và Cl-, giúp dung dịch dẫn điện tốt.
- AgCl rất ít tan trong nước nên số ion có trong dung dịch nhỏ, làm giảm khả năng dẫn điện.
\((1)2Fe+3Cl2→to2FeCl3\)
\((2)Br2+2KI→2KBr+I2(2)Br2+2KI→2KBr+I2\)
\((3)Zn+2HCl→ZnCl2+H2(3)Zn+2HCl→ZnCl2+H2\)
\((4)AgNO3+NaBr→AgBr+NaNO3(4)AgNO3+NaBr→AgBr+NaNO3\)
Tốc độ phản ứng trung bình là sự thay đổi nồng độ của các chất tham gia phản ứng (chất đầu) hoặc sản phẩm trong một khoảng thời gian nhất định. Với phản ứng trên, tốc độ trung bình của phản ứng có thể được viết dưới dạng:
\(vtb=−12Δ[NOCl]Δt=12Δ[NO]Δt=Δ[Cl2]Δtvtb=2−1ΔtΔ[NOCl]=21ΔtΔ[NO]=ΔtΔ[Cl2]\)
mglucose=100%mdd.C%=100%V.D.C%=100%500.1,1.5%=27,5(g)
⇒ \(n_{g l u c o s e} = \frac{27 , 5}{180} = \frac{11}{72} \left(\right. m o l \left.\right)\)
⇒ Năng lượng tối đa một người bệnh nhận được khi truyền một chai 500 mL dung dịch glucose 5% là
\(2803 , 0. \frac{11}{72} = 428 , 24 \left(\right. k J \left.\right)\).
a)
![]()
- Chất khử: HCl.
- Chất oxi hóa: MnO2.
b)
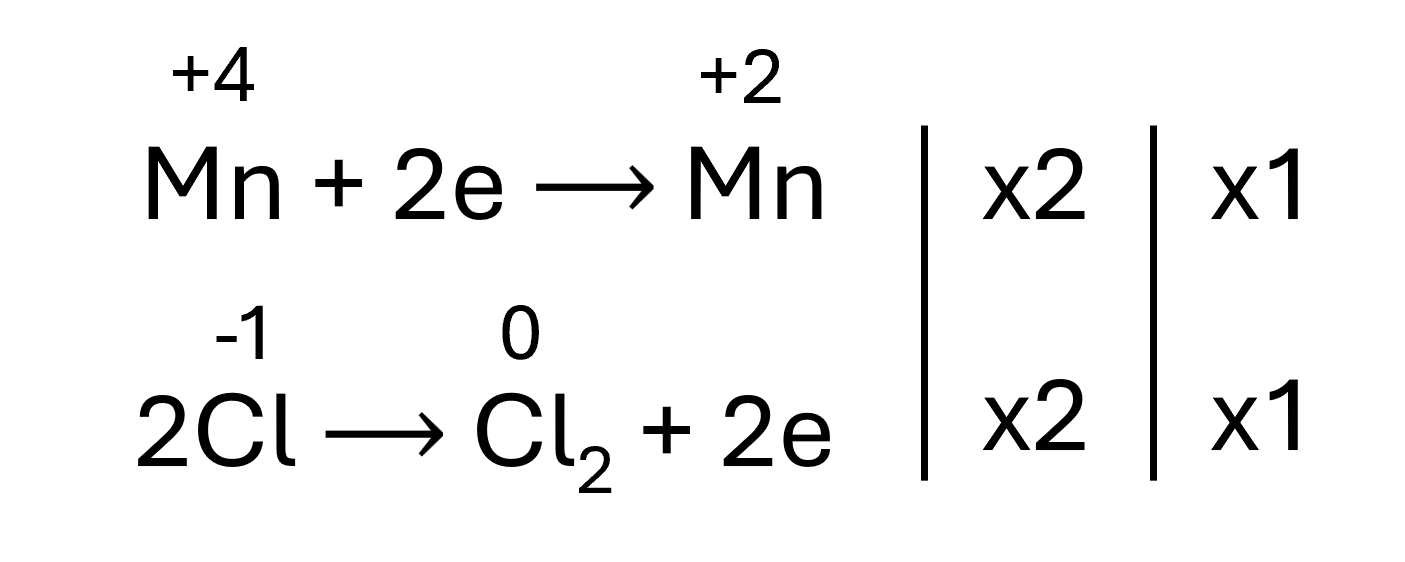
⇒ MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
-Phản ứng tỏa nhiệt:
+ Phản ứng đốt than.
+ Phản ứng phân hủy glucose trong cơ thể.
- Phản ứng thu nhiệt:
+ Phản ứng nhiệt phân KMnO4.
+ Phản ứng C sủi tan trong nước.
Bạn chưa trả lời câu hỏi này. Trả lời câ