Trần Trà My
Giới thiệu về bản thân
Chào mừng bạn đến với trang cá nhân của Trần Trà My





0





0





0





0





0





0





0
2025-12-14 21:06:58
- (Z = 15): Cấu hình electron là [Ne]3s23p3[𝑁𝑒]3𝑠23𝑝3. Nguyên tử P có 5 electron ở lớp vỏ ngoài cùng. Để đạt cấu hình bền vững của khí hiếm gần nhất (Ar, 8 electron), P cần thêm 3 electron.
- H (Z = 1): Cấu hình electron là 1s11𝑠1. Nguyên tử H có 1 electron ở lớp vỏ ngoài cùng. Để đạt cấu hình bền vững của khí hiếm gần nhất (He, 2 electron - cấu hình duet), H cần thêm 1 electron.
- Mỗi nguyên tử P góp 3 electron.
- Mỗi nguyên tử H góp 1 electron.
- Tổng cộng có 3 cặp electron dùng chung, tạo thành ba liên kết cộng hóa trị đơn (P-H).
- Lúc này, xung quanh nguyên tử P có 5+3=85+3=8 electron (đạt cấu hình octet) và xung quanh mỗi nguyên tử H có 1+1=21+1=2 electron (đạt cấu hình duet).
2025-12-14 21:05:53
a. Viết công thức hydroxide (Y) tương ứng của X. Answer: X(OH)2𝑋(𝑂𝐻)2 Kim loại X thuộc nhóm IIA trong bảng tuần hoàn, nên có hóa trị II. Công thức hydroxide tương ứng của X là X(OH)2𝑋(𝑂𝐻)2. b. Hoà tan hoàn toàn 5,832 gam hydroxide Y bởi lượng vừa đủ 73 gam dung dịch HCl 10% thu được dung dịch T. Tìm kim loại X. Tính số mol HCl Khối lượng HCl𝐇𝐂𝐥nguyên chất trong dung dịch: mHCl=73×10100=7,3gam𝑚𝐻𝐶𝑙=73×10100=𝟕,𝟑gam Số mol HCl𝐇𝐂𝐥: nHCl=mHClMHCl=7,336,5=0,2mol𝑛𝐻𝐶𝑙=𝑚𝐻𝐶𝑙𝑀𝐻𝐶𝑙=7,336,5=𝟎,𝟐mol Viết phương trình phản ứng và lập mối quan hệ Phương trình phản ứng giữa hydroxide Y ( X(OH)2𝑋(𝑂𝐻)2) và HCl𝐇𝐂𝐥: X(OH)2+2HCl→XCl2+2H2O𝑋(𝑂𝐻)2+2𝐻𝐶𝑙→𝑋𝐶𝑙2+2𝐻2𝑂 Theo phương trình phản ứng, số mol X(OH)2𝑋(𝑂𝐻)2bằng một nửa số mol HCl𝐇𝐂𝐥: nX(OH)2=12nHCl=12×0,2=0,1mol𝑛𝑋(𝑂𝐻)2=12𝑛𝐻𝐶𝑙=12×0,2=𝟎,𝟏mol Tìm khối lượng mol của Y và xác định X Khối lượng mol của X(OH)2𝑋(𝑂𝐻)2: MX(OH)2=mX(OH)2nX(OH)2=5,8320,1=58,32g/mol𝑀𝑋(𝑂𝐻)2=𝑚𝑋(𝑂𝐻)2𝑛𝑋(𝑂𝐻)2=5,8320,1=𝟓𝟖,𝟑𝟐g/mol Khối lượng mol của X(OH)2𝑋(𝑂𝐻)2cũng bằng MX+2×(16+1)𝑀𝑋+2×(16+1): MX+2×17=58,32𝑀𝑋+2×17=58,32 MX+34=58,32𝑀𝑋+34=58,32 MX=58,32−34=24,32g/mol𝑀𝑋=58,32−34=𝟐𝟒,𝟑𝟐g/mol Khối lượng mol nguyên tử của kim loại X là 24,32 g/mol. Kim loại có khối lượng mol này và thuộc nhóm IIA là Magie (Mg). Answer: Kim loại X là Mg (Magie).
2025-12-14 21:05:39
a. Viết công thức hydroxide (Y) tương ứng của X. Answer: X(OH)2𝑋(𝑂𝐻)2 Kim loại X thuộc nhóm IIA trong bảng tuần hoàn, nên có hóa trị II. Công thức hydroxide tương ứng của X là X(OH)2𝑋(𝑂𝐻)2. b. Hoà tan hoàn toàn 5,832 gam hydroxide Y bởi lượng vừa đủ 73 gam dung dịch HCl 10% thu được dung dịch T. Tìm kim loại X. Tính số mol HCl Khối lượng HCl𝐇𝐂𝐥nguyên chất trong dung dịch: mHCl=73×10100=7,3gam𝑚𝐻𝐶𝑙=73×10100=𝟕,𝟑gam Số mol HCl𝐇𝐂𝐥: nHCl=mHClMHCl=7,336,5=0,2mol𝑛𝐻𝐶𝑙=𝑚𝐻𝐶𝑙𝑀𝐻𝐶𝑙=7,336,5=𝟎,𝟐mol Viết phương trình phản ứng và lập mối quan hệ Phương trình phản ứng giữa hydroxide Y ( X(OH)2𝑋(𝑂𝐻)2) và HCl𝐇𝐂𝐥: X(OH)2+2HCl→XCl2+2H2O𝑋(𝑂𝐻)2+2𝐻𝐶𝑙→𝑋𝐶𝑙2+2𝐻2𝑂 Theo phương trình phản ứng, số mol X(OH)2𝑋(𝑂𝐻)2bằng một nửa số mol HCl𝐇𝐂𝐥: nX(OH)2=12nHCl=12×0,2=0,1mol𝑛𝑋(𝑂𝐻)2=12𝑛𝐻𝐶𝑙=12×0,2=𝟎,𝟏mol Tìm khối lượng mol của Y và xác định X Khối lượng mol của X(OH)2𝑋(𝑂𝐻)2: MX(OH)2=mX(OH)2nX(OH)2=5,8320,1=58,32g/mol𝑀𝑋(𝑂𝐻)2=𝑚𝑋(𝑂𝐻)2𝑛𝑋(𝑂𝐻)2=5,8320,1=𝟓𝟖,𝟑𝟐g/mol Khối lượng mol của X(OH)2𝑋(𝑂𝐻)2cũng bằng MX+2×(16+1)𝑀𝑋+2×(16+1): MX+2×17=58,32𝑀𝑋+2×17=58,32 MX+34=58,32𝑀𝑋+34=58,32 MX=58,32−34=24,32g/mol𝑀𝑋=58,32−34=𝟐𝟒,𝟑𝟐g/mol Khối lượng mol nguyên tử của kim loại X là 24,32 g/mol. Kim loại có khối lượng mol này và thuộc nhóm IIA là Magie (Mg). Answer: Kim loại X là Mg (Magie).
2025-12-14 21:05:05
- Phân tử Br2𝐁𝐫𝟐:
- Mỗi nguyên tử Br có 7 electron hóa trị. Công thức electron có một cặp electron dùng chung (liên kết đơn) giữa hai nguyên tử Br và ba cặp electron không liên kết trên mỗi nguyên tử.
- Công thức electron: ∶Br̈∶Br̈∶∶𝐁𝐫̈∶𝐁𝐫̈∶
- Công thức cấu tạo: Br−Br𝐁𝐫−𝐁𝐫
- Phân tử CO2𝐂𝐎𝟐:
- Nguyên tử C có 4 electron hóa trị, mỗi nguyên tử O có 6 electron hóa trị. Công thức electron có hai cặp electron dùng chung (liên kết đôi) giữa nguyên tử C và mỗi nguyên tử O, cùng với hai cặp electron không liên kết trên mỗi nguyên tử O.
- Công thức electron: ∶Ö∶∶C∶∶Ö∶∶𝐎̈∶∶𝐂∶∶𝐎̈∶
- Công thức cấu tạo: O=C=O𝐎=𝐂=𝐎
- Phân tử C2H4𝐂𝟐𝐇𝟒:
- Mỗi nguyên tử C có 4 electron hóa trị, mỗi nguyên tử H có 1 electron hóa trị. Công thức electron có hai cặp electron dùng chung (liên kết đôi) giữa hai nguyên tử C, và một cặp electron dùng chung (liên kết đơn) giữa mỗi nguyên tử C với hai nguyên tử H.
- Công thức electron:
- Công thức cấu tạo:
2025-12-14 21:04:18
Số neutron của nguyên tử M là
13𝟏𝟑, và số neutron của nguyên tử X là
14𝟏𝟒.
2025-12-14 21:03:45
a) Viết công thức Lewis và công thức cấu tạo của 2 hợp chất trên Công thức Lewis của CO2𝐂𝐎𝟐 Phân tử CO2𝐂𝐎𝟐 có một nguyên tử Carbon liên kết cộng hóa trị với hai nguyên tử Oxygen. Công thức Lewis thể hiện các cặp electron liên kết và không liên kết. :O=C=O::O=C=O: Công thức cấu tạo của CO2𝐂𝐎𝟐 Công thức cấu tạo chỉ tập trung vào các liên kết giữa các nguyên tử: O=C=OO=C=O Công thức Lewis của NH3𝐍𝐇𝟑 Phân tử NH3𝐍𝐇𝟑 có một nguyên tử Nitrogen liên kết cộng hóa trị với ba nguyên tử Hydrogen. Nitrogen có một cặp electron không liên kết (cặp electron tự do). H-N..-H| HH-𝑁..-H|H Công thức cấu tạo của NH3𝐍𝐇𝟑 Công thức cấu tạo của amoniac: H-N-H| HH-N-H|H b) Hợp chất nào tan trong nước, hợp chất nào không tan trong nước? Giải thích cụ thể. Amoniac ( NH3𝐍𝐇𝟑) tan nhiều trong nước, trong khi carbon dioxide ( CO2𝐂𝐎𝟐) tan rất ít trong nước. Giải thích
- Amoniac ( NH3𝐍𝐇𝟑): Phân tử NH3𝐍𝐇𝟑 có tính phân cực mạnh và có khả năng tạo liên kết hydrogen với các phân tử nước. Sự tương tác mạnh mẽ này làm cho amoniac dễ dàng hòa tan trong nước.
- Carbon dioxide ( CO2𝐂𝐎𝟐): Mặc dù có các liên kết C=O phân cực, nhưng do cấu trúc hình học tuyến tính, hai mômen lưỡng cực C=O triệt tiêu lẫn nhau, làm cho toàn bộ phân tử CO2𝐂𝐎𝟐 không phân cực. Theo nguyên tắc "chất tan đồng dạng với dung môi đồng dạng", CO2𝐂𝐎𝟐 tan rất ít trong dung môi phân cực như nước.
2025-12-14 21:03:04
a) Viết cấu hình electron nguyên tử của X và Y Step 1: Xác định cấu hình electron của X (Z=11) Nguyên tố X có số hiệu nguyên tử Z=11𝑍=11, là Natri (Na). Cấu hình electron của X là: 1s22s22p63s1𝟏𝐬𝟐𝟐𝐬𝟐𝟐𝐩𝟔𝟑𝐬𝟏 Step 2: Xác định cấu hình electron của Y (Z=8) Nguyên tố Y có số hiệu nguyên tử Z=8𝑍=8, là Oxi (O). Cấu hình electron của Y là: 1s22s22p4𝟏𝐬𝟐𝟐𝐬𝟐𝟐𝐩𝟒 Answer: Cấu hình electron của X là 1s22s22p63s1𝟏𝐬𝟐𝟐𝐬𝟐𝟐𝐩𝟔𝟑𝐬𝟏. Cấu hình electron của Y là 1s22s22p4𝟏𝐬𝟐𝟐𝐬𝟐𝟐𝐩𝟒. b) Dùng sơ đồ biểu diễn sự hình thành liên kết giữa X và Y Step 1: Xác định loại liên kết X là kim loại nhóm IA, có 1 electron lớp ngoài cùng. Y là phi kim nhóm VIA, có 6 electron lớp ngoài cùng. X có xu hướng nhường 1 electron để đạt cấu hình bền vững, Y có xu hướng nhận 2 electron để đạt cấu hình bền vững. Do đó, liên kết hình thành giữa X và Y là liên kết ion, tạo thành hợp chất có công thức X2Y𝐗𝟐𝐘(hoặc Na2O𝐍𝐚𝟐𝐎). Step 2: Biểu diễn sự hình thành ion Nguyên tử X nhường 1 electron tạo thành ion dương X+𝑋+: X→X++1e−𝑋→𝑋++1𝑒− Nguyên tử Y nhận 2 electron tạo thành ion âm Y2−𝑌2−: Y+2e−→Y2−𝑌+2𝑒−→𝑌2− Step 3: Biểu diễn sự kết hợp của các ion Để tạo thành hợp chất trung hòa về điện, cần 2 nguyên tử X nhường tổng cộng 2 electron cho 1 nguyên tử Y nhận 2 electron: 2X+Y→2X++Y2−→X2Y2𝑋+𝑌→2𝑋++𝑌2−→𝐗𝟐𝐘 Answer: Sơ đồ biểu diễn sự hình thành liên kết ion giữa X và Y là: 2X+Y→X2Y2𝑋+𝑌→𝐗𝟐𝐘 Trong đó, 2 nguyên tử X nhường 2 electron cho 1 nguyên tử Y để hình thành các ion X+𝑋+và Y2−𝑌2−, các ion này hút nhau bằng lực hút tĩnh điện tạo thành hợp chất ion X2Y𝐗𝟐𝐘.
2025-12-14 20:53:45
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
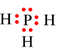
2025-12-14 20:51:39
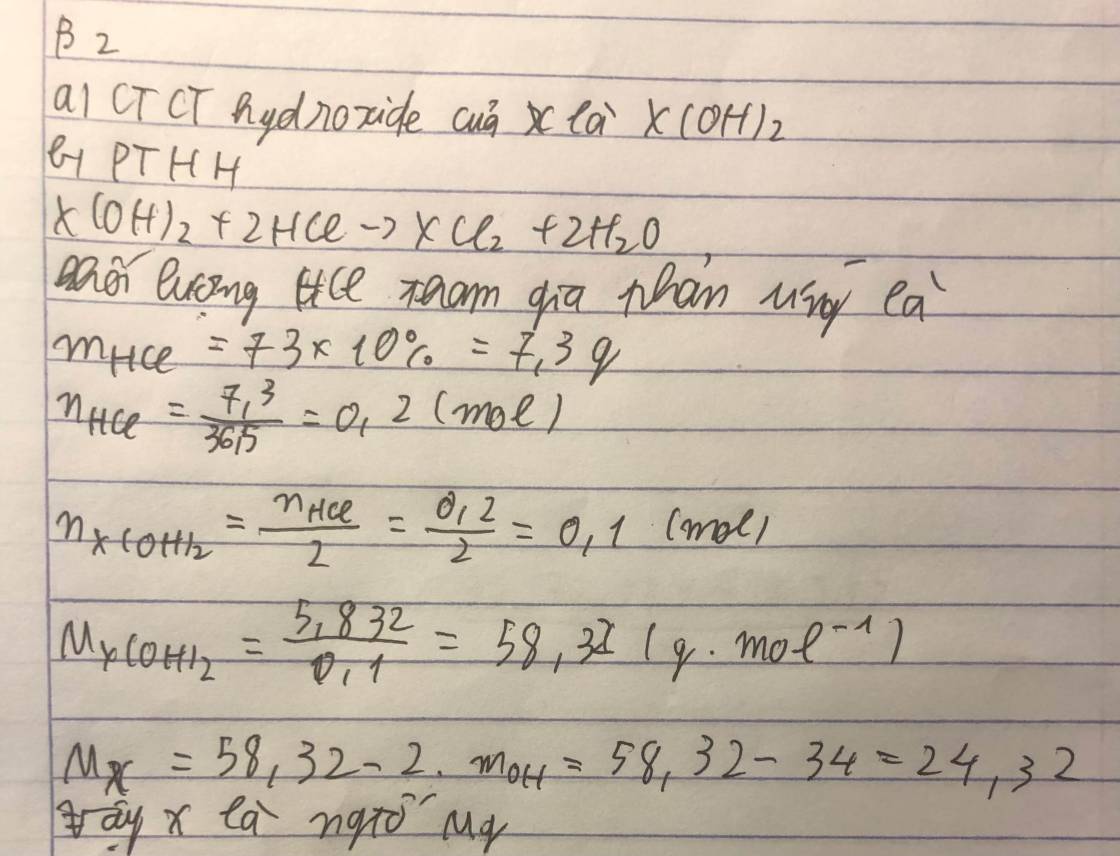
2025-12-14 20:51:05