

Nguyễn Công Dũng
Giới thiệu về bản thân



































Gọi công thức chung của hai muối chloride là RCl.
RCl + AgNO3 → AgCl + RNO3
\(n_{R C l} = n_{A g N O_{3}}\)= 0,03 (mol)
⇒ MR = 28,33 (g/mol).
Mà A và B là hai kim loại kiềm thuộc hai chu kì liên tiếp nên A và Na và B là K ⇒ Công thức hai muối là NaCl và KCl.
Gọi x và y lần lượt là số mol của NaCl và KCl, ta có:
(1) x + y = 0,03
(2) 58,5x + 74,5y = 1,915
⇒ x = 0,02 và y = 0,01
⇒ Khối lượng hai muối NaCl và KCl lần lượt là 1,17 gam và 0,745 gam.
a) Cấu hình electron nguyên tử: 1s22s22p63s23p1 hay [Ne] 3s23p1
b)
- Số electron = 13 ⇒ ô số 13.
- Số lớp electron = 3 ⇒ chu kì 3.
- Số electron lớp ngoài cùng = 3 ⇒ nhóm IIIA.
Gọi số hạt proton và neutron của nguyên tử X là Px và NX; số hạt proton và neutron của nguyên tử M là PM và NM.
+ Tổng số hạt cơ bản trong hợp chất M2X là 116 hạt nên 2PX + NX + 2PM + NM = 116 (1).
+ Số hạt mang điện trong phân tử M2X nhiều hơn số hạt không mang điện là 36 nên 2PX + 2PM - NX - NM = 36 (2).
+ Số khối của X lớn hơn M là 9 nên (PM + NM) - (PX + NX) = 9 (3).
+ Tổng số hạt trong X2- nhiều hơn trong M+ là 17 nên (2PX + NX + 2) - (2PM + NM - 1) = 17 (4).
Từ (1), (2), (3) và (4), ta có: PM = 11, NM = 12, PX = 16, NX = 16.
a) Công thức Lewis của CO2 là:

Công thức Lewis của NH3 là:

Công thức cấu tạo của CO2 là:
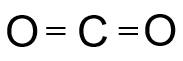
Công thức cấu tạo của NH3 là:

b) NH3 tan trong nước do phân tử NH3 tạo được liên kết hydrogen với phân tử nước, còn CO2 không tan trong nước do phân tử CO2 không tạo được liên kết hydrogen với phân tử H2O.
a) Cấu hình electron nguyên tử của X (Z = 11) là 1s22s22p63s1.
Cấu hình electron nguyên tử của Y (Z = 8) là 1s22s22p4.
b) Dựa vào cấu hình electron của nguyên tử X và nguyên tử Y, ta thấy X là nguyên tố kim loại (có 1 electron lớp ngoài cùng) và Y là nguyên tố phi kim (có 6 electron lớp ngoài cùng).
Vậy liên kết giữa X và Y là liên kết ion.
Sự tạo thành liên kết giữa X và Y:
X → X+ + 1e
Y + 2e → Y2-
2X+ + Y2- → X2Y
Nguyên tử Phosphor (P, Z = 15) có cấu hình electron là \([Ne]3s^{2}3p^{3}\), với 5 electron hóa trị. Để đạt cấu hình bền vững của khí hiếm Argon (Ar), P cần thêm 3 electron để có 8 electron ở lớp ngoài cùng (tuân theo quy tắc octet). Nguyên tử Hydrogen (H, Z = 1) có cấu hình electron là \(1s^{1}\), với 1 electron hóa trị. Để đạt cấu hình bền vững của khí hiếm Helium (He), H cần thêm 1 electron để có 2 electron ở lớp ngoài cùng