

Triệu Duy Khôi
Giới thiệu về bản thân



































Một số biện pháp hạn chế khí thải công nghiệp: - *Lắp đặt hệ thống xử lý khí thải*: Sử dụng công nghệ lọc, hấp thụ, trung hòa để loại bỏ các chất ô nhiễm. - *Sử dụng năng lượng sạch*: Chuyển đổi sang năng lượng tái tạo như mặt trời, gió để giảm phát thải. - *Tối ưu hóa quy trình sản xuất*: Áp dụng công nghệ tiên tiến, giảm thiểu chất thải. - *Trồng cây xanh*: Tăng cường khả năng hấp thụ CO₂ và cải thiện chất lượng không khí. - *Kiểm soát và giám sát*: Thực hiện đo đạc, báo cáo định kỳ để đảm bảo tuân thủ quy định. - *Nâng cao nhận thức*: Đào tạo nhân viên, tuyên truyền về bảo vệ môi trường.
- nH₂ = 8,05675 / 22,4 = 0,36 mol - Phản ứng: Fe + 2HCl → FeCl₂ + H₂ 2Al + 6HCl → 2AlCl₃ + 3H₂ - Đặt nFe = x, nAl = y - 56x + 27y = 9,65 - x + 1,5y = 0,36 - Giải hệ: x = 0,1; y = 0,15 - m = mFeCl₂ + mAlCl₃ = 0,1×127 + 0,15×133,5 = 32,725 g
a) Hiện tượng: Xuất hiện kết tủa trắng AgCl. Phương trình hóa học: CaCl₂ + 2AgNO₃ → 2AgCl↓ + Ca(NO₃)₂ b) Tính khối lượng AgCl: - nCaCl₂ = 0,555 / 111 = 0,005 mol - nAgNO₃ = 1,7 / 170 = 0,01 mol - AgNO₃ hết, CaCl₂ dư - nAgCl = nAgNO₃ = 0,01 mol - mAgCl = 0,01 × 143,5 = 1,435 g c) Chất còn lại: CaCl₂, Ca(NO₃)₂ - nCaCl₂ dư = 0,005 - 0,005 = 0 mol (hết) - nCa(NO₃)₂ = 0,01 / 2 = 0,005 mol - Vdd = 0,1 L - CM Ca(NO₃)₂ = 0,005 / 0,1 = 0,05 M
Các phương trình hóa học để hoàn thành chuỗi chuyển hóa: 1. Fe + H₂SO₄ → FeSO₄ + H₂ 2. FeSO₄ + 2NaOH → Fe(OH)₂ + Na₂SO₄ 3. Fe(OH)₂ + 2HCl → FeCl₂ + 2H₂O 4. FeCl₂ + Zn → Fe + ZnCl₂
Ví dụ về phản ứng: - *Phản ứng thu nhiệt*: Quá trình hòa tan NH₄NO₃ (amoni nitrat) vào nước. Quá trình này thu nhiệt từ môi trường xung quanh, làm giảm nhiệt độ của dung dịch. - *Phản ứng tỏa nhiệt*: Đốt cháy xăng (C₈H₁₈) trong động cơ xe máy. Quá trình này tỏa ra một lượng nhiệt lớn, tạo ra năng lượng để xe hoạt động.
Những chất là oxide trong danh sách là: - BaO (Oxide bazơ) - CO₂ (Oxide axit) - P₂O₅ (Oxide axit) Các chất còn lại không phải là oxide: - NaOH (Bazơ) - HCl (Axit) - NaCl (Muối) - CuSO₄ (Muối) - NO (Oxide trung tính)
a.biến đổi hoá học
b.biến đổi vật lý
c.biến đổi hoá học
d.biến đổi vật lý
e.biến đổi hoá học
ại \(x = 9\) thì:
\(C = x^{14} - 10 x^{13} + 10 x^{12} - 10 x^{11} + . . . + 10 x^{2} - 10 x + 10\)
\(C = x^{14} - \left(\right. x + 1 \left.\right) x^{13} + \left(\right. x + 1 \left.\right) x^{12} - \left(\right. x + 1 \left.\right) x^{11} + . . . + \left(\right. x + 1 \left.\right) x^{2} - \left(\right. x + 1 \left.\right) x + x + 1\)
\(C = x^{14} - x^{14} - x^{13} + x^{13} + x^{12} - x^{12} - x^{11} + . . . + x^{3} + x^{2} - x^{2} - x + x + 1\)
\(C = 1\).
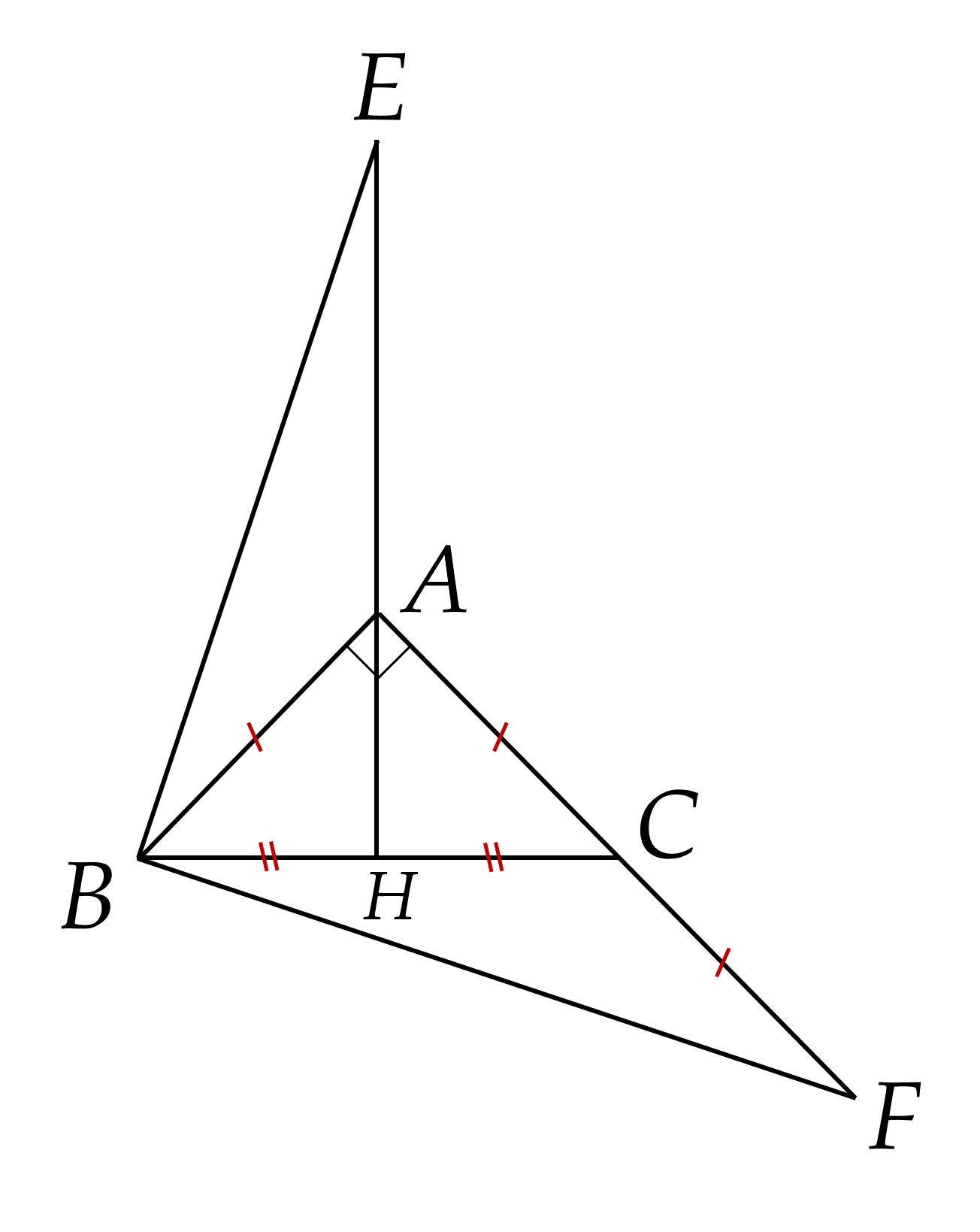
a) Xét \(\Delta A H B\) và \(\Delta A H C\) có:
\(A B = A C\) (gt);
\(A H\) chung;
\(H B = H C\) (\(H\) là trung điểm của \(B C\));
Suy ra \(\Delta A H B = \Delta A H C\) (c.c.c).
b) Vì \(\Delta A H B = \Delta A H C\) (cmt) suy ra \(\hat{A H B} = \hat{A H C}\) (cặp góc tương ứng).
Mà \(\hat{A H B} + \hat{A H C} = 18 0^{\circ}\) (hai góc kề bù).
Suy ra \(\hat{A H B} = \hat{A H C} = 9 0^{\circ}\).
Vậy \(A H \bot B C\).
c) Vi \(\Delta A H B = \Delta A H C\) (cmt) suy ra \(\hat{H A B} = \hat{H A C} = 4 5^{\circ}\);
\(\hat{H C A} = \hat{H B A} = \frac{18 0^{\circ} - \hat{B A C}}{2} = 4 5^{\circ}\) (cặp góc tương ứng).
Xét \(\Delta E B A\) và \(\Delta B F C\) có:
\(A B = C F\) (gt);
\(\hat{B A E} = \hat{B C F}\) (cùng bù với \(\hat{H A B} = \hat{H C A} = 4 5^{\circ}\));
\(E A = B C\) (gt);
Suy ra \(\Delta E B A = \Delta B F C\) (c.g.c).
Trả lời câu hỏi này
Bài 4
Xem hướng dẫn Bình luận (95)a) Biến cố \(A\) là biến cố ngẫu nhiên, biến cố \(B\) là biến cố chắc chắn, biến cố \(C\) là biến cố không thể.
b) Xác suất của biến cố \(A\) là: \(\frac{3}{6} = \frac{1}{2}\).