Dương Thị Hồng
Giới thiệu về bản thân



































1. Phương trình phản ứng: Fe+2HCl→FeCl 2 +H 2 2. Tính toán: Số mol Fe: n Fe = 56 8,96 =0,16 mol Theo phương trình: n H 2 =n Fe =0,16 mol Thể tích khí H 2 ở điều kiện chuẩn (áp suất 1 bar, nhiệt độ 25°C): V=0,16×24,79=3,9664 lít
Có 5 yếu tố chính ảnh hưởng đến tốc độ phản ứng:
1:Nồng độ: Khi tăng nồng độ chất phản ứng, số va chạm có hiệu quả giữa các phân tử tăng lên \rightarrow Tốc độ phản ứng tăng.
2 Nhiệt độ: Khi tăng nhiệt độ, các phân tử chuyển động nhanh hơn, năng lượng va chạm tăng \rightarrow Tốc độ phản ứng tăng. (Thường tăng 10°C thì tốc độ tăng 2-4 lần).
3 Áp suất (đối với chất khí): Khi tăng áp suất, khoảng cách giữa các phân tử khí giảm lại (tương đương tăng nồng độ) \rightarrow Tốc độ phản ứng tăng.
4Diện tích bề mặt (đối với chất rắn): Khi chia nhỏ chất rắn (nghiền nhỏ, đập vụn), diện tích tiếp xúc giữa các chất phản ứng tăng lên \rightarrow Tốc độ phản ứng tăng.
5Chất xúc tác: Là chất làm giảm năng lượng hoạt hóa của phản ứng nhưng không bị tiêu hao sau phản ứng \rightarrow Tốc độ phản ứng tăng.
Nồng độ: Tăng nồng độ chất phản ứng → tăng số va chạm hiệu quả → tăng tốc độ phản ứng. Nhiệt độ: Tăng nhiệt độ → các phân tử chuyển động nhanh, năng lượng lớn → tăng số va chạm hiệu quả → tăng tốc độ phản ứng. Áp suất (chất khí): Tăng áp suất → các phân tử gần nhau hơn (tăng nồng độ) → tăng tốc độ phản ứng. Diện tích tiếp xúc (chất rắn): Tăng diện tích tiếp xúc (nghiền nhỏ) → tăng khả năng va chạm → tăng tốc độ phản ứng. Chất xúc tác: Giảm năng lượng hoạt hóa của phản ứng → tăng tốc độ phản ứng (nhưng không bị biến đổi sau phản ứng).
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
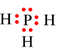
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.