Cho S tác dụng H2 thu H2S biết VH2S thu được là 1,68l. Hiệu suất pứ ;à 80%
a)Tính mS pứ
b)Tính VH2 pứ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTHH:
S + H2 \(\rightarrow\) H2S
a) Số mol H2S thu được là:
1,68 : 22,4 = 0,075 (mol)
Theo PTHH, số mol S tham gia phản ứng là 0,075 mol.
Khối lượng S phản ứng là:
0,075 . 32 = 2,4 (g)
Vì hiệu suất phản ứng là 80% nên KL S cần là:
2,4 .80% = 1,92 (g)
b) Theo PTHH, số mol H2 tham gia phản ứng là 0,075 mol.
Thể tích H2 phản ứng là:
0,075 . 22,4 = 1,68 (l)
Vì hiệu suất phản ứng là 80% nên KL H2 cần là:
1,68 . 80% = 1,344 (l)

Nếu phản ứng xảy ra hoàn toàn thì khối lượng hỗn hợp phải là 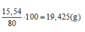
![]()

PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
\(n_{H_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,75}{3}\), ta được H2 dư.
Theo PT: \(n_{Fe\left(LT\right)}=2n_{Fe_2O_3}=0,4\left(mol\right)\)
Mà: H% = 80%
\(\Rightarrow n_{Fe\left(TT\right)}=0,4.80\%=0,32\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Fe}=0,32\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,32.22,4=7,168\left(l\right)\)
Bạn tham khảo nhé!

2Al+6HCl----->2AlCl3+3H2
nAl=2,7/27=0,1 mol
cứ 2mol Al------> 2 mol AlCl3
0,1mol ----->0,1 mol
mAlCl3=0,1.133,5=13.35g
H%=80%------->mAlCl3 thực tế thu được =13,35.80/100=10,68g
n Al = 2,7/27 =0,1 mol
2Al + 6HCl ---> 2AlCl3 + 3H2
0,1 ---> 0,1
ADCT : H% =80% ----> m AlCl3 tạo thành = (m AlCl3 thực tế . H% ) / 100
hay m AlCl3 = ((0,1.133,5) .80 ) / 100 =10,68 %

\(n_{AgCl}=\dfrac{43.05}{143.5}=0.3\left(mol\right)\) \(\Rightarrow n_{HCl}=0.3\left(mol\right)\)
\(n_{HCl}=\dfrac{6.72}{22.4}=0.3\left(mol\right),n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(H_2+Cl_2\underrightarrow{^{^{t^0}}}2HCl\)
\(0.15....0.15.......0.3\)
\(H\%=\dfrac{0.15}{0.2}\cdot100\%=75\%\)

Đáp án: D
Gọi công thức ancol cần tìm là: ROH
Số mol 2 ancol tương ứng là a, b
Phần 1:
→ a + b = 0,1
46a + (R+17)b = 3,9 → (29 – R)b = 0,7 → 29 > R → R = CH3 → CH3OH
Phần 2:
nCH3COOH = 0,5
H=80%
Nên ta có:
meste = 0,05.0,8(15+44+15+15+44+29) = 6,48

Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{FeCl_2\left(LT\right)}=n_{H_2\left(LT\right)}=n_{Fe}=0,2\left(mol\right)\)
Mà: H% = 75%
\(\Rightarrow n_{FeCl_2\left(TT\right)}=n_{H_2\left(TT\right)}=0,2.75\%=0,15\left(mol\right)\)
\(\Rightarrow m_{FeCl_2}=0,15.127=19,05\left(g\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)