Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Các phương trình phản ứng
2KNO3 2KNO2 + O2↑ (1)
2KClO3 2KCl + 3O2↑ (2)
b) Theo (1) và (2), thấy số mol hai muối tham gia phản ứng như nhau nhưng số mol oxi tạo thành khác nhau và do đó thể tích khí oxi thu được là khác nhau.
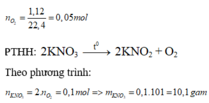
Theo (1): nO2 = nKNO3 =
= 0,05 mol; VO2 = 0,05x22,4 = 1,12 lít
Theo (2): nO2 = nKClO3 =
= 0,15 mol; VO2 = 0,15x22,4 = 3,36 lít
c) Để thu được 1,12 lít khí (0,05 mol) O2, thì:
Theo (1): nKNO3 = 2nO2 = = 0,1 mol; mKNO3 = 0,1x101 = 10,1 g
Theo (2): nKClO3 = nO2 =
x0,05 mol; VKClO3 =
x0,05x122,5 = 4,086 g.

Ở thí nghiệm 2: Chỉ có Al tác dụng với dung dịch NaOH và bị hòa tan hết vì NaOH dư.
Chất rắn còn lại là Mg = 0,6 gam hay = 0,6 : 24 = 0,025 mol
Ở thí nghiệm 1: Số moi H2 = 1,568 : 22,4 = 0,07 mol. Gọi x là số mol Al.
Phương trình hóa học:
2Al + 3H2S04 \(\rightarrow\) Al2(S04)3 + 3H2
x \(\rightarrow\) 1,5x (mol)
Mg + H2S04 \(\rightarrow\) MgS04 + H2
0,025 \(\rightarrow\) 0,025 (mol)
Theo hiđro, ta có: 1,5x + 0,025 = 0,07 => x = 0,03 mol = mol Al Khối lượng của hỗn hợp: m = mMg + mAl = 0,6 + 0,03.27 = 1,41 gam
%Mg = \(\dfrac{0,6}{1,41}\) x 100% = 42,55%; %Al = 100% - 42,55% = 57,45%.
Ở thí nghiệm 2: Chỉ có Al tác dụng với dung dịch NaOH và bị hòa tan hết vì NaOH dư.
Chất rắn còn lại là Mg = 0,6 gam hay = 0,6 : 24 = 0,025 mol
Ở thí nghiệm 1: Số moi H2 = 1,568 : 22,4 = 0,07 mol. Gọi x là số mol Al.
Phương trình hóa học:
2Al + 3H2S04 → Al2(S04)3 + 3H2
x → 1,5x (mol)
Mg + H2S04 → MgS04 + H2
0,025 → 0,025 (mol)
Theo hiđro, ta có: 1,5x + 0,025 = 0,07 => x = 0,03 mol = mol Al Khối lượng của hỗn hợp: m = mMg + mAl = 0,6 + 0,03.27 = 1,41 gam
%Mg = x 100% = 42,55%; %Al = 100% - 42,55% = 57,45%.

nZn = 0,3 mol
Zn + Cl2 \(\underrightarrow{t^o}\) ZnCl2
\(\Rightarrow\) VCl2 = 0,3.22,4 = 6,72 (l)
MnO2 + 4HCl \(\underrightarrow{t^o}\) MnCl2 + Cl2 + 2H2O
\(\Rightarrow\) mMnCl2 = 0,3.126 = 37,8 (g)
a) PTHH xảy ra: Zn + Cl2→ ZnCl2
b) số mol Zn tham gia phản ứng : nZn=\(\dfrac{19,5}{65}\)=0,3(mol)
PTHH: Zn+ Cl2→ZnCl2
Theo phương trình (mol ) : 1 1 1
Theo đề (mol) : 0,3 ⇒0,3
Thể tích Cl2 cần dùng cho phản ứng :
VO2=0,3.22,4=6,72(lít)
Mong chị thông cảm vì em mới học lớp 7 , nên câu c em chưa biết làm ạ .

a,pthh:2Fe+3Cl2--->2FeCl3
b,nFe=11,2/56=0,2(mol)
từ pthh nCl2=\(\dfrac{3}{2}\)nFe=\(\dfrac{3}{2}.0,2=0,3\left(mol\right)\)
VCl2=0,3.22,4=6,72(l)
c,nCl2=14,4/22,4\(\dfrac{14,4}{22,4}=\dfrac{9}{14}\)(mol)
từ pthh nFe=\(\dfrac{2}{3}\)nCl2=\(\dfrac{9}{14}.\dfrac{2}{3}=\dfrac{3}{7}\)
mFe=56.\(\dfrac{3}{7}\)=24(g)
Bạn ơi đề câu b không cho ở điều kiện nào cả sao bạn biết là điều kiện tiêu chuẩn?

nO2 = 0,05 mol
2KMnO4 \(\underrightarrow{t^o}\) K2MnO4 + MnO2 + O2
\(\Rightarrow\) mKMnO4 = 0,1.158.\(\dfrac{100}{75}\) \(\approx\) 21,1 (g)

a;
Fe3O4 + 4H2 \(\rightarrow\)3Fe + 4H2O (1)
nFe=\(\dfrac{33,6}{56}=0,6\left(mol\right)\)
Theo PTHH 1 ta có:
\(\dfrac{1}{3}\)nFe=nFe3O4=0,2(mol)
mFe3O4=0,2.232=46,4(g)
b;
Theo PTHH 1 ta có:
nH2=\(\dfrac{4}{3}\)nFe=0,8(mol)
VH2=22,4.0,8=17,92(lít)
c;
Zn + 2HCl \(\rightarrow\)ZnCl2 + H2 (2)
2Al + 6HCl\(\rightarrow\)2AlCl3 + 3H2 (3)
Đặt nZn=a \(\Leftrightarrow\)mZn=65a
nAl=b\(\Leftrightarrow\)mAl=27b
Ta có hệ pt:
\(\left\{{}\begin{matrix}65a+27b=23,8\\a+\dfrac{3}{2}b=0,8\end{matrix}\right.\)
=>a=0,2;b=0,4
mZn=65.0,2=13(g)
mAl=23,8-13=10,8(g)

bài 2 :cách 1:
Al + HCl -> H2.
H2 khử hh.
cho hh kloại thu đc vào HCl ;lại thấy Cu k tan
PTPƯ:
2Al+ 6HCl-------> 2AlCl3 + 3H2
H2 + CuO ---- xt nhiệt độ--------> Cu+ H2O
3H2+ Fe2O3------- xt nhiệt độ----> 2Fe+ 3H2O
Fe+HCl -------> FeCl2
cách 2; dùng pư nhiệt nhôm để thu đc hh 2kloại Cu và fe.
sau đó cho vào dd HCl
3CuO + 2Al ----- xt nhiệt độ------> Al2O3 + 3Cu
Fe2O3+ 2Al --------xt nhiệt độ-------> Al2O3+ 2Fe
cách 3: cho hh oxit vào dd HCl. thu đc 2 m' là CuCl2 và FeCl3.
cho Al vào dd để đẩy 2 m'
thu đc hh 2 kloại Cu và Fe. còn lại làm giống ở trên :d
CuO + 2HCl -------> CuCl2 + H2O
Fe2O3 +6 HCl -------> 2FeCl3 +3 H2O
Al + FeCl3------> AlCl3 + Fe
2Al+ 3CuCl2-------> 2AlCl3+ 3Cu
Bài 1 bạn kẻ bảng cho từng chất tác dụng với nhau rồi nhận biết sự có mặt từng chất qua hiện tượng .
2KMnO4 + 16HCl \(\rightarrow\) 2KCl + 2MnCl2 + 5Cl2 + 8H2O
33,6 lít khí chứ bạn nhỉ
V Cl2=33,6 lít \(\rightarrow\) nCl2=\(\frac{33,6}{22,4}\)=1,5 mol
\(\rightarrow\) nKMnO4=\(\frac{2}{5}\)nCl2=0,6 mol \(\rightarrow\) mKMnO4=0,6.(39+55+16.4)=94,8