Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B
Gọi số hạt proton, nơtron và electron lần lượt là p, n và e.
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 155:
p + e + n = 155 hay 2p + n = 155 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 33 hạt
(p+e) – n = 33 hay 2p – n = 33 (2)
Giải (1), (2) ta có p = e = 47. Vậy X là Ag.

Đáp án B
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 155:
p + e + n = 155 hay 2p + n = 155(do p=e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 33 hạt.
(p+e) – n = 33 hay 2p – n = 33(2)
Giải (1), (2) ta có p = e = 47

Cái nguyên tử X mình làm ko ra bạn xem lại đề cái 53,125 nếu là 53,125% thì bạn giải ra đươc p = 16 và n = 17 đó là lưu huỳnh ( ra nghiệm đẹp mình nghĩ là đúng )
Ta có 2p + n = 8 và n = 52,63/100 . ( p + n ) từ hệ trên bạn giải ra p = 9 và n = 10 đó là Flo

Bước 1. Ký hiệu
- \(p\): số proton.
- \(e\): số electron.
- \(n\): số nơtron.
Ta có:
\(p + e + n = 24\)
Vì là nguyên tử trung hòa điện nên:
\(p = e\)
Điều kiện đề cho:
\(e = n\)
⟹ Suy ra:
\(p = e = n\)
Bước 2. Tính số hạt
Gọi số hạt mỗi loại = \(x\).
\(p = e = n = x\)
⟹ Tổng:
\(p + e + n = 3 x = 24 \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } x = 8\)
⟹ \(p = 8 , e = 8 , n = 8\).
Bước 3. Xác định Z, N, A
- \(Z = p = 8\).
- \(N = n = 8\).
- \(A = Z + N = 8 + 8 = 16\).
✅ Kết quả:
\(Z = 8 , N = 8 , A = 16\)
👉 Vậy nguyên tử X chính là oxi \(\left(\right. _{8}^{16} O \left.\right)\).

Giả sử số hiệu nguyên tử và số nơtron của nguyên tử nguyên tố X lần lượt là Z, N.
Ta có hpt:
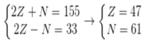
→ X là Ag → Chọn B.


Đáp án D
Gọi Z là số proton của X => Số electron của X là Z
Gọi N là số nơtron của X
=>X là Ag