Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

NaBr + AgNO3 \(\rightarrow\)AgBr + NaNO3
NaCl + AgNO3 \(\rightarrow\) AgCl + NaNO3
\(C_M=0,5M\Rightarrow n_{AgNO_3}=0,025\left(mol\right)\)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
\(\Rightarrow x=9,0557.10^{-3};y=0,01594\)
\(\Rightarrow C\%=\frac{0,594.58,5}{50}.100\%=1,865\%\)
NaBr + AgNO3 →→AgBr + NaNO3
NaCl + AgNO3 →→ AgCl + NaNO3
CM=0,5M⇒nAgNO3=0,025(mol)CM=0,5M⇒nAgNO3=0,025(mol)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
⇒x=9,0557.10−3;y=0,01594⇒x=9,0557.10−3;y=0,01594
⇒C%=0,594.58,550.100%=1,865%⇒C%=0,594.58,550.100%=1,865%

=
= 0, 025 mol
Phương trình hóa học của phản ứng:
NaBr + AgNO3 → AgBr↓ + NaNO3
X mol x mol x mol
NaCl + AgNO3 → AgCl↓ + NaNO3
Y mol y mol y mol
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Ta có hệ phương trình đại số:
Giải ra , ta có x = 0, 009 mol NaBr
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
C% = x 100% = 1,86%

- Tính acid phụ thuộc vào khả năng tách H của acid. Phân tử nào càng dễ tách H thì tính acid càng mạnh
- Trong nhóm halogen, từ F đến I có độ âm điện giảm dần
=> Khả năng liên kết H-X giảm dần
=> Khả năng tách H trong HX tăng dần
=> Tính acid tăng dần
=> Dung dịch HF có tính acid yếu nhất

Chọn đáp án A
m d d A g N O 3 = V.D = 50.1,0625 = 53,125 (gam)
ð m A g N O 3 = 53 , 125 . 8 100 = 4,25 (gam) => n A g N O 3 = 4 , 25 170 = 0,025 (mol)
Nồng độ % của 2 muối bằng nhau => Khối lượng 2 muối bằng nhau.
N a C l : x m o l N a B r : y m o l → x + y = 0 , 025 58 , 5 x = 103 y → x = 0 , 0159 y = 0 , 0091
ð
C
%
N
a
C
l
=
0
,
0159.58
,
5
50
.100% = 1,86%

Hai muối ban đầu có thể là Na2CO3 và CaCl2
PTHH: Na2CO3 + CaCl2 --> 2NaCl + CaCO3
Do dung dịch chỉ chứa muối NaCl
=> Phản ứng vừa đủ
=> \(\dfrac{n_{Na_2CO_3}}{n_{CaCl_2}}=\dfrac{1}{1}\)
Xét \(\dfrac{m_{Na_2CO_3}}{m_{CaCl_2}}=\dfrac{106.n_{Na_2CO_3}}{111.n_{CaCl_2}}=\dfrac{106}{111}\)

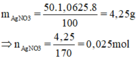
Phương trình hóa học của phản ứng:
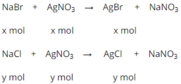
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Gọi nNaBr = x, nNaCl = y.
Theo pt: nNaBr = nAgNO3; nNaCl = nAgNO3
⇒ nNaBr + nNaCl = nAgNO3
Ta có hệ phương trình đại số: 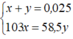
Giải ra, ta có x ≈ 0,009 mol
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
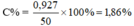

1: \(AgNO_3+NaI\rightarrow NaNO_3+AgI\downarrow\)
\(AgNO_3+NaCl\rightarrow NaNO_3+AgCl\downarrow\)
\(AgNO_3+NaBr\rightarrow NaNO_3+AgBr\downarrow\)
2: nếu xuất hiện kết tủa trắng thì ống nghiệm đó là NaCl
nếu xuất hiện kết tủa vàng nhạt thì ống nghiệm đó là NaBr
nếu xuất hiện kết tủa vàng đậm thì ống nghiệm đó là NaI
nếu ko xuất hiện kết tủa thì ống nghiệm đó là NaF

2Cl2 + 2H2O —> 4HCl + O2
Cl + 2Na —-> 2NaCl (nhiệt độ)
NaCl + AgNO3 —> AgCl + NaNO3
Bạn ở dưới sai sai thì phải:
2Na + Cl2 -> (t°) 2NaCl
NaCl + AgNO3 -> AgCl + AnNO3

Tự cân bằng nhá!
a,
\(HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\
Cl_2+Fe\rightarrow FeCl_3\\
FeCl_3+NaOH\rightarrow Fe\left(OH\right)_3+NaCl\\
NaCl+H_2SO_{4\left(dn\right)}\rightarrow Na_2SO_4+HCl\\
HCl+CuO\rightarrow CuCl_2+H_2O\\
CuCl_2+AgNO_3\rightarrow Cu\left(NO_3\right)_2+AgCl\)
b,
\(KMnO_4+HCl\rightarrow KCl+MnCl_2+Cl_2+H_2O\\ Cl_2+H_2\rightarrow HCl\\ HCl+Fe\left(OH\right)_3\rightarrow FeCl_3+H_2O\\ FeCl_3+AgNO_3\rightarrow Fe\left(NO_3\right)_3+AgCl\\ AgCl-as,t^o->Ag+Cl_2\\ Cl_2+NaBr\rightarrow NaCl+Br_2\\ Br_2+NaI\rightarrow NaBr+I_2\)
c, Giống câu b 3 pt đầu
\(HCl+Fe\left(OH\right)_2\rightarrow FeCl_2+H_2O\\
FeCl_2+AgNO_3\rightarrow Fe\left(NO_3\right)_2+AgCl\\
AgCl-as,t^o->Ag+Cl_2\)
d,
\(HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\
Cl_2+Fe\rightarrow FeCl_3\\
FeCl_3+NaOH\rightarrow Fe\left(OH\right)_3+NaCl\\
Fe\left(OH\right)_3+H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+H_2O\)
e,
\(HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\
Cl_2+NaOH\rightarrow NaCl+NaClO+H_2O\\
NaCl+H_2SO_{4\left(dn\right)}\rightarrow Na_2SO_4+HCl\\
CuO+HCl\rightarrow CuCl_2+H_2O\\
CuCl_2+AgNO_3\rightarrow Cu\left(NO_3\right)_2+AgCl\\
AgCl-as,t^o->Ag+Cl_2\)
f,
\(MnO_2+HCl\rightarrow MnCl_2+Cl_2+H_2O\\ Cl_2+KOH-t^o->KClO_3+KCl+H_2O\\ KClO_3\rightarrow KCl+O_2\\ KCl+H_2SO_{4\left(dn\right)}\rightarrow K_2SO_4+HCl\\ HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\ Ca\left(OH\right)_2+Cl_2\rightarrow CaCl_2+Ca\left(ClO\right)_2+H_2O\)

\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\left(1\right)\\ m_{giảm}=m_{Br_2}-m_{Cl_2}\\ \Leftrightarrow n_{NaCl\left(1\right)}=n_{NaBr\left(1\right)}=\dfrac{13,35}{160-71}=0,15\left(mol\right)\\ \Rightarrow\%m_{NaBr}=\dfrac{103.0,15}{42,6}.100\approx36,268\%\\ \Rightarrow\%m_{NaCl}\approx63,732\%\)
Bổ sung:
\(C\%_{ddNaBr\left(trongA\right)}=\dfrac{0,15.103}{200}.100=7,725\%\\ C\%_{ddNaCl\left(trongA\right)}=\dfrac{42,6-0,15.103}{200}.100=13,575\%\)
=))
ummm......
cũng được!
Sự khác biệt về tính dẫn điện chủ yếu bắt nguồn từ độ tan khác nhau của hai loại muối này trong nước
1.So sánh tính tan trong nước
NaCl:tan rất tốt trong nước,ở nhiệt độ phòng,dộ tan NaCl khoảng 36g/100g
AgCl:Là muối kết tủa thực tế được coi là không tan trong nước(độ tan cực kì thấp,khoảng 1,9×10-⁴g/100g nước ở 25°C)
2.Giải thích tính dẫn điện
Đối với NaCl:
khi cho vào nước,NaCl phân ly hoàn toàn thành các ion tự do:
NaCl---->Na+ +Cl-
Vì NaCl tan rất tốt,nồng độ các ion Na+ và Cl- trong dung dịch rất lớn.Các ion óng vai trò là những vật dẫn điện,giúp dòng điện đi qua dung dịch một cách dễ dàng
Đối với AgCl:
Mặc dù AgCl là hợp chất ion,nhưng do lực hút giữa các ion Ag+và Cl-trong mạng lưới tính thể rất mạnh,nước không thể tách chúng ra hiệu quả.Chỉ có một lượng cực nhỏ AgCl phân li thành ion:
AgCl(s)------><---------Ag+(ag)+Cl-(aq)
Vì nồng độ ion tự do trong nước quá thấp (gần như bằng không),dung dịch AgCl dẫn điện rất kém,thậm chí được coi là không dẫn điện trong điều kiện thông thường
Kết luận: NaCl dẫn điện tốt hơn AgCl chủ yếu do độ tan.NaCl tan tốt tạo ra nhiều ion tự do,trong khi AgCl hầu như không tan nên không có đủ ion để tải điện
NaCl: tan rất tốt trong nước
AgCl: rất ít tan trong nước
NaCl có tính dẫn điện tốt hơn AgCl vì:
+) sự phân ki ion
+) nồng độ ion
muối NaCl tan tốt trong nước hơn muối AgCl. Tại vì tính kim loại của Na mạnh hơn tính kim loại của Ag
So sánh tính tan: NaCl: tan tốt trong nước. AgCl: rất ít tan (gần như không tan, tạo kết tủa trắng). Giải thích tính dẫn điện: Khi tan trong nước, NaCl → Na⁺ + Cl⁻ (phân li hoàn toàn) ⇒ nhiều ion tự do ⇒ dẫn điện tốt. AgCl hầu như không tan ⇒ rất ít phân li ra Ag⁺, Cl⁻ ⇒ hầu như không có ion ⇒ dẫn điện kém. Kết luận: NaCl dẫn điện tốt hơn AgCl vì độ tan lớn → tạo nhiều ion trong dung dịch, còn AgCl không tan → không tạo ion.
NaCl tan nhiều trong nước, trong khi AgCl hầu như không tan. NaCl dẫn điện tốt hơn AgCl vì NaCl tan và phân li thành các ion tự do trong nước, còn AgCl không tan nên không tạo được ion tự do dẫn điện,.
So sánh tính tan trong nước:
-NaCl (Natri clorua): Tan rất tốt trong nước.
-AgCl (Bạc clorua): Hầu như không tan trong nước, tạo thành kết tủa.
Giải thích tính dẫn điện:
-Một chất dẫn điện được trong nước là nhờ sự chuyển động của các ion tự do.
-NaCl tan tốt và phân ly hoàn toàn thành các ion Na+ và Cl-. Do có nồng độ ion tự do cao nên dung dịch NaCl dẫn điện rất tốt.
-AgCl là muối không tan, nên khi cho vào nước nó không phân ly ra các ion (hoặc lượng ion là cực kỳ nhỏ). Vì thiếu các hạt mang điện tự do nên AgCl dẫn điện rất kém hoặc không dẫn điện.
Như vậy,Dù cùng là muối halide, nhưng NaCl dẫn điện tốt hơn AgCl vì nó tan tốt trong nước để tạo ra các ion tự do.