Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Ta có: \(n_{KCl}=\dfrac{1,49}{74,5}=0,02\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{KCl}=0,03\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,03.24,79=0,7437\left(l\right)\)
b, Theo PT: \(n_{KClO_3\left(TT\right)}=n_{KCl}=0,02\left(mol\right)\)
\(\Rightarrow m_{KClO_3\left(TT\right)}=0,02.122,5=2,45\left(g\right)\)
\(\Rightarrow H=\dfrac{2,45}{3,5}.100\%=70\%\)

\(n_{KClO3}=\dfrac{5,25}{122,5}=\dfrac{3}{70}\left(mol\right)\)
a) PTHH : \(2KClO_3\xrightarrow[]{t^o}2KCl+3O_2\)
\(\dfrac{3}{70}\) \(\dfrac{3}{70}\) \(\dfrac{9}{140}\)
b) \(V_{O2\left(dktc\right)}=\dfrac{9}{140}.22,4=1,44\left(l\right)\)
c) \(m_{KCl\left(lt\right)}=\dfrac{3}{70}.74,5=\dfrac{447}{140}\left(mol\right)\)
\(\Rightarrow H\%=\dfrac{m_{tt}}{m_{lt}}.100\%=\dfrac{2,235}{\dfrac{447}{140}}.100\%=70\%\)

a, \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
b, \(n_{KCl}=\dfrac{0,745}{74,5}=0,01\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{KCl}=0,015\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,015.24,79=0,37185\left(l\right)\)
\(m_{O_2}=0,015.32=0,48\left(g\right)\)
c, \(n_{KClO_3\left(pư\right)}=n_{KCl}=0,01\left(mol\right)\)
\(\Rightarrow m_{KClO_3\left(pư\right)}=0,01.122,5=1,225\left(g\right)\)
\(\Rightarrow H=\dfrac{1,225}{2,5}.100\%=49\%\)

\(n_{KCl}=\dfrac{17.88}{74.5}=0.24\left(mol\right)\)
\(2KClO_3\underrightarrow{^{^{t^0}}}2KCl+3O_2\)
\(0.24.............0.24\)
\(m_{KClO_3}=\dfrac{0.24\cdot122.5}{80\%}=36.75\left(g\right)\)

nKClO3=0,04 mol
nKCl=0,034 mol
2KClO3. =>2KCl. +3O2
0,034 mol<=0,034 mol=>0,051 mol
H%=0,034/0,04.100%=83,89%
VO2=0,051.22,4=1,1424 lit
\(n_{KClO_3}=\frac{4,9}{122,5}=0,04\left(mol\right)\)
\(n_{KCl}=\frac{2,5}{74,5}=0,034\left(mol\right)\)
\(2KClO_3->2KCl+3O_2\left(1\right)\)
theo (1) \(n_{KClO_3\left(pư\right)}=n_{KCl}=0,034\left(mol\right)\)
hiệu suất phản ứng là
\(\frac{0,034}{0,04}.100\%=83,89\%\)
theo (1) \(n_{O_2}=\frac{3}{2}n_{KCl}=0,051\left(mol\right)\)
=> \(V_{O_2}=0,051.22,4=1,1424\left(l\right)\)

nKClO3 = 49/122,5 = 0,4 (mol)
PTHH: 2KClO3 -> (t°, MnO2) 2KCl + 3O2
nO2 (TT) = 0,6 . 90% = 0,54 (mol)
VO2 = 0,54 . 22,4 = 12,096 (l)

a, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, \(n_{O_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{2}{3}n_{O_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,2.102=20,4\left(g\right)\)
c, \(H=\dfrac{18,36}{20,4}.100\%=90\%\)

Gọi hiệu suất phản ứng là a
$2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
Ta thấy :
V SO2 / 2 = V O2 nên hiệu suất tính theo số mol của SO2 hoặc O2
V SO2 phản ứng = 4,48a(lít)
V O2 phản ứng = 2,24a(lít)
V SO3 = V SO2 pư = 4,48a(lít)
Sau phản ứng, khí gồm :
SO2 : 4,48 - 4,48a(lít)
O2 : 2,24 - 2,24a(lít)
SO3 : 4,48a(lít)
Suy ra :
4,48 - 4,48a + 2,24 - 2,24a + 4,48a = 5,6
=> a = 0,5 = 50%
Hỗn hợp khí gồm :
SO2 : 4,48 -4,48.0,5 = 2,24 lít
O2 : 2,24 - 2,24.0,5 = 1,12 lít
SO3 : 4,48.0,5 = 2,24 lít
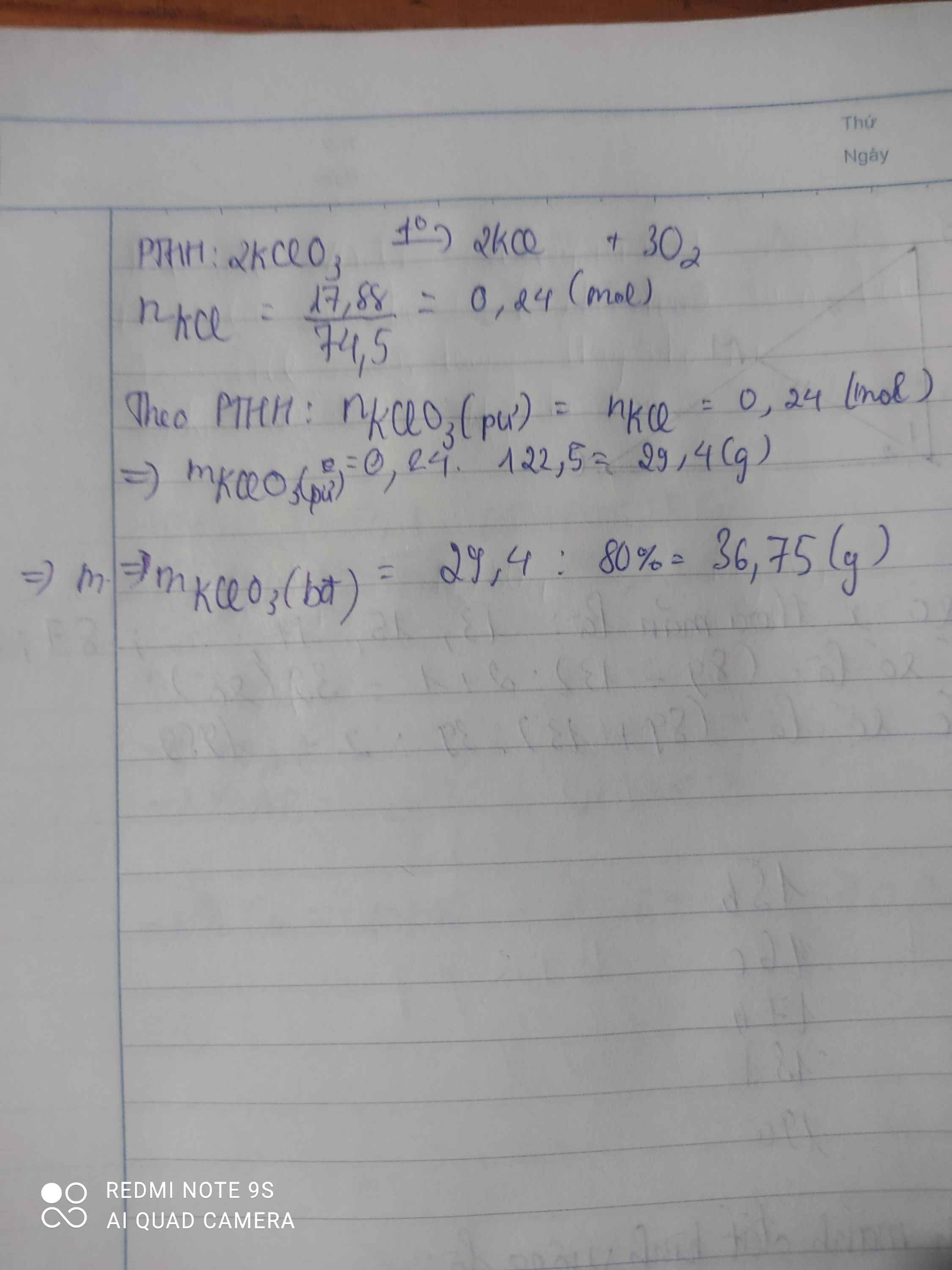
\(n_{KClO_3}=\dfrac{7}{122,5}=\dfrac{2}{35}\left(mol\right)\)
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
2/35 2/35 3/35
\(V_{O_2}=\dfrac{3}{35}.24,79\approx2,1249\left(l\right)\)
\(m_{KCl}=\dfrac{2}{35}.74,5\approx4,257\left(g\right)\)
\(H=\dfrac{2,98}{4,257}.100\%=70\%\)
Mình tưởng nO2 phải tính theo KCl chứ :v
cái m KCl kia chắc là thực tế thu được á chỉ để tính hiệu suất thôi con mol chắc vẫn tính theo KClO3
O2 thì cũng thực tế thu đc chứ, hiệu suất chỉ có từng đấy thì sao mà O2 thu được nhiều hơn đc b :))
Lớp 8 đề nó như này cho VO2 chắc chỉ để tính Hiệu suất th chứ không cần cầu kì như bài khó hơn đâu