Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

C46.
1.
Bảo toàn điện tích: \(n_{OH^-}=n_{K^+}+2n_{Ba^{2+}}=0,03+2.0,02=0,07\left(mol\right)\)
\(pH=13\Rightarrow\left[OH^-\right]=10^{-1}\Rightarrow n_{OH^- \left(dư\right)}=10^{-1}.0,2=0,02\left(mol\right)\)
\(\Rightarrow y=n_{H^+}=n_{OH^-\left(pư\right)}=0,07-0,02=0,05\left(mol\right)\)
Bảo toàn điện tích: \(n_{H^+}=n_{NO_3^-}+n_{Cl^-}\Leftrightarrow0,05=0,02+z\Rightarrow z=0,03\)

$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề



X: Fe3O4
Y: FeCl2
Z: FeCl3
T: Fe(OH)2
U: Fe(OH)3
A: NaCl (hoặc H2O)
B: H2O (hoặc NaCl)
D: H2 (hoặc Cl2)
E: Cl2 (hoặc H2)
F: NaOH
G: HCl
PTHH:
a) NaCl + H2O -dpmn----> 1/2 H2 + 1/2 Cl2 + NaOH
H2 + Cl2 -to-> 2 HCl
HCl + NaOH -> NaCl + H2O
b) 3 Fe +2 O2 -to->Fe3O4
Fe3O4 + 8 HCl -> FeCl2 +2 FeCl3 + H2O
FeCl2 + 2 NaOH -> Fe(OH)2 + 2 NaCl
FeCl3 +3 NaOH -> Fe(OH)3 + 3NaCl
Chúc em học tốt!


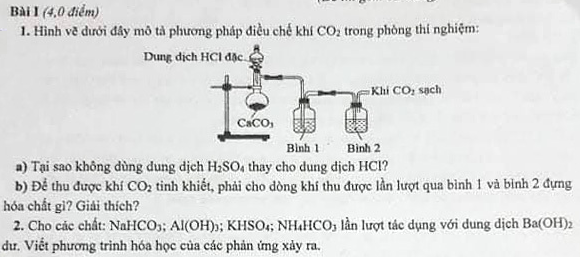
A là dung dịch H2SO4
B: Na2CO3
C: H2SO4 đặc
D: Xút (NaOH)
Khi cho DD H2SO4 tác dụng với Na2CO3 giải phóng khí SO2 mang theo hơi nước.
Bình C để giữ hơi nước lại trong bình (H2SO4 đặc háu nước) SO2 không tác dụng tiếp tục được dẫn qua bình đựng.
Để tránh SO2 thoát ra bên ngoài gây ô nhiễm môi trường và 1 số bệnh cho con người nên Xút được đặt ở miệng bình để tạo muối.




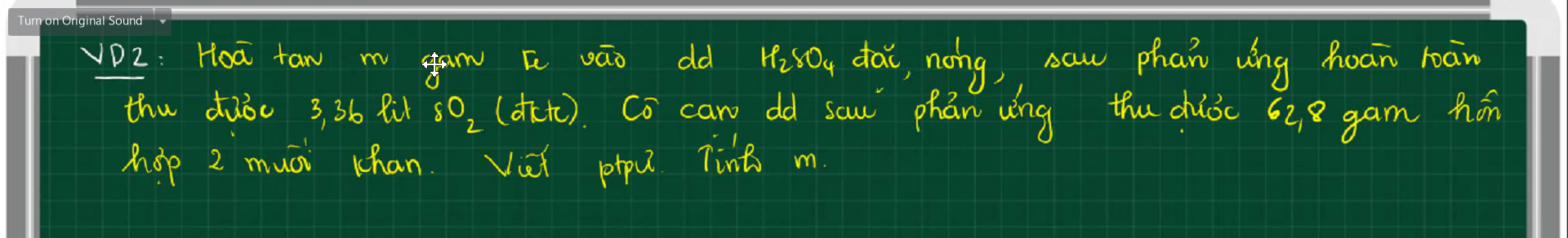
 Giúp mình nha !!!
Giúp mình nha !!! Giúp hộ mình nha !!!
Giúp hộ mình nha !!!






Link Facebook: Cuộc thi Trí tuệ VICE | Facebook
vẫn là facebook :(((
anh Quốc Anh ơi
em ko có tài khoản face ạ
làm sao bây h
Thì thôi
cứ tưởng mình là người tối cổ nhất cái hoc24 vì ko có face :)
tui cungko co face nek mak tui cung cha tham gia lm gi
Hóa C55 bài 2a :
Để phục hồi những bức tranh đó người ta phun lên bức tranh nước oxi già H2O2, bức tranh sẽ trắng trở lại
giải thích: Pb(OH)2.PbCO3 lâu ngày tác dụng dần với khí H2S có trong không khí tạo ra PbS màu đen :
Pb(OH)2 + H2S →PbS↓+ 2H2O
Phun dung dịch H2O2 sẽ làm cho PbS chuyển thành PbSO4 màu trắng : PbS + 4H2O2 → PbSO4↓ + 4H2O.
Hoá học C55
1) b) Vì chì khi tương tác trên bề mặt dung dịch HCl loãng thì tạo thành muối không tan PbCl2; khi tương tác trên bề mặt dung dịch H2SO4 dưới 80% thì tạo thành muối không tan PbSO4 bám lên bề mặt, ngăn cản chì tiếp xúc với axit nên phản ứng dừng lại.
Phương trình hóa học:
Pb + 2HCl --> PbCl2↓+ H2
Pb + H2SO4 --> PbSO4↓+ H2
Nhưng với dung dịch đậm đặc hơn của các axit đó thì chì lại tan tốt do các muối khó tan trên chuyển thành chuyển thành hợp chất dễ tan trong nước. Phương trình hóa học:
PbCl2 + 2HCl --> H2[PbCl4]
PbSO4 + H2SO4 --> Pb(HSO4)2
Thiếc dễ tan trong dung dịch axit loãng cũng như đặc, vì tạo thành muối tan trong nước. Phương trình hóa học:
Sn + 2HCl --> SnCl2 + H2
Sn + H2SO4 --> SnSO4 + H2
Hoá học C55.
3) 1.a) Khi cho CaCO3 tác dụng với dung dịch H2SO4 sẽ tạo thành kết tủa CaSO4 ít tan, bao quanh CaCO3 ngăn cản sự tiếp xúc của CaCO3 với H2SO4 khiến cho lượng CO2 điều chế ra ít. Vì thế người ta không dùng dung dịch H2SO4 để điều chế khí CO2.
Phương trình hóa học:
CaCO3 + H2SO4 --> CaSO4 + CO2 + H2O
Hóa học C55
3) 2.
Ba(OH)2 + NaHCO3 → H2O + NaOH + BaCO3↓
Ba(OH)2 + 2KHSO4 → 2H2O + K2SO4↓ + BaSO4↓
Ba(OH)2 + 2Al(OH)3 → 4H2O + Ba(AlO2)2
Ba(OH)2 + NH4HCO3 → 2H2O + NH3 + BaCO3↓
Hóa học C55
4) 1.a) Gọi Z(A), Z(B) lần lượt là số đơn vị điện tích hạt nhân trong A, B.
Ta có: Z(A) + 3Z(B) = 40 và A thuộc chu kỳ 3
⇒ 11 <= Z(A) <= 18 ⇒ 7,3 <= Z(B) <= 9,6
⇒ Z(B) = 8 hoặc Z(B) = 9
Z(B) = 8 (O) --> Z(A) = 16 (S) (chọn)
Z(B) = 9 (F) ⇒ Z(A) = 13 (Al) (loại vì trong nguyên tử A và B, số proton bằng số nơtron.)
Cấu hình electron của A và B:
A(Z = 8): 1s^2 2s^2 2p^4
B (Z = 16): 1s^2 2s^2 2p^6 3s^2 3p^4
Hóa học C55
4) 1b. Cấu trúc phân tử AB3: SO3:
Trong phân tử SO3 có 2 liên kết cộng hóa trị (liên kết đôi) được hình thành bởi sự góp chung electron của S với O và 1 liên kết cho nhận (được hình thành bằng đôi electron chỉ do S đóng góp).