
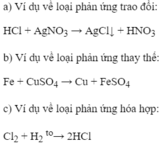
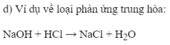
a) Loại phản ứ...">
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời. a) 2CO + O2 Phản ứng này là phản ứng oxi hóa - khử (và cũng là phản ứng hóa hợp). Khí CO khi đốt là cháy được. Vai trò của co là chất khử. Phản ứng này tỏa nhiều nhiệt nên dược dùng trong luyện gang, thép. b) CO + CuO Phản ứng này là phản ứng oxi hóa - khử. Phản ứng này xảy ra ở nhiệt độ cao. Vai trò của CO là chất khử. Phản ứng này dùng để điều chế Cu. a) 2CO + O2 Phản ứng này là phản ứng oxi hóa - khử (và cũng là phản ứng hóa hợp). Khí CO khi đốt là cháy được. Vai trò của co là chất khử. Phản ứng này tỏa nhiều nhiệt nên dược dùng trong luyện gang, thép. b) CO + CuO Phản ứng này là phản ứng oxi hóa - khử. Phản ứng này xảy ra ở nhiệt độ cao. Vai trò của CO là chất khử. Phản ứng này dùng để điều chế Cu. Các phương trình hóa học: a) С + 2CuO b) С + 2PbO c) С + CO2 d) С + 2FeO Các phản ứng trên dều thuộc loại phản ứng oxi hóa - khử. Vai trò của с là chất khử. Các phản ứng: a), b) dùng điều chế kim loại. c), d) xảy ra trong quá trình luyện gang, dùng luyện gang. khối lượng thanh kim loại giảm -> nguyển tử khối của KL phải lớn hơn Cu và đứng trước Cu trong dãy điện hóa Đặt x,y lần lượt là số mol của Zn,Fe *TN1 :đề sai nha em!!! *TN2 :nH2=6.72/22.4=0.3 mol Zn + 2HCl --> ZnCl2 + H2(1) x 2x x Fe + 2HCl --> FeCl2 + H2(2) y 2y y Theo pthh,ta có hệ pt: 65x + 56y = 18.6 x+y= 0.3 giải hệ trên,ta được :x=0.2,y=0.1 a)=>nHCl=0.4+0.2=0.6 mol CM HCl=0.6/1=0.6 M b) mZn=65*0.2=13g mFe=56*0.1=5.6g đề này rất đúng , chỉ cần xét về số l h2 thoát ra là được . bài này rất dễ \(n_{MgCO3}=\dfrac{8,4}{84}=0,1\left(mol\right)\) a) Pt : \(2CH_3COOH+MgCO_3\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O|\) 2 1 1 1 1 0,2 0,1 0,1 0,1 b) \(n_{CH3COOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\) ⇒ \(m_{CH3COOH}=0,2.60=12\left(g\right)\) \(C_{ddCH3COOH}=\dfrac{12.100}{200}=6\)0/0 \(n_{\left(CH3COO\right)2Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\) ⇒ \(m_{\left(CH3COO\right)2Mg}=0,1.142=14,2\left(g\right)\) \(m_{ddspu}=8,4+200-\left(0,1.44\right)=204\left(g\right)\) \(C_{dd\left(CH3COO\right)2Mg}=\dfrac{14,2.100}{204}=6,96\)0/0 Chúc bạn học tốt nFe = 0,1 mol; nS = 0,05 mol a) Phương trình phản ứng: Fe + S → FeS (1) nFe dư = 0,1 – 0,05 = 0,05 nên hỗn hợp chất rắn A có Fe và FeS. Fe + 2HCl → FeCl2 + H2↑ (2) FeS + 2HCl → FeCl2 + H2S↑ (3) b) Dựa vào phương trình phản ứng (2) và (3), ta có: nHCl= 0,1 + 0,1 = 0,2 mol VHCl = 0,2 /1 = 0,2 lít. a) Đặt công thức oxít M2On Ptpư: M2On + nH2SO4 → M2(SO4)n + nH2O mol 1 n 1 mddH2SO4 = n.98.100/10 = 980n gam mdd muối = 2M + 996n (gam) → C% muối = (2M + 96n) : (2M + 996n) = 0,11243 → M = 9n → M = 27 (Al) → Công thức oxít: Al2O3 b) ptpứ: Al2O3 ---> 2Al + 3/2O2 Al2O3 + 2NaOH ---> 2NaAlO2 + H2O Al2(SO4)3 + 3Na2CO3 + 3H2O ---> 2Al(OH)3 + 3Na2SO4 + 3CO2
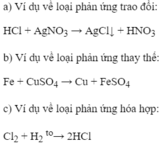
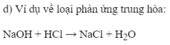

2CO2
CO2 + Cu
2CO2
CO2 + Cu

2Cu + CO2
2Pb + CO2
2CO
2Fe + CO2

khối lượng thanh kim loại tăng -> nguyển tử khối của KL phải nhỏ hơn Ag
=> KL cần tìm là Zn


