Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nH2=0,6mol
PTHH: 2Al+6HCl=>2AlCl3+3H2
0,4<-1,2<--0,4 <- 0,6
=> mAl=0,4.27=10,8g
=> m AL2O3=21-10,8=10,2g
=> nAl2O3=0,1mol
PTHH: Al2O3+6HCl=> 2AlCl3+3H2O
0,1--->0,6------>0,2----->0,3
PTHH: AlCl3+3NaOH=> Al(OH)3+3NaCl
nAl(OH)3=0,4mol
nAlCl3=0,4+0,2=0,6mol
ta có : 0,6 : 0,4
=> n AlCl3 dư theo n nAl(OH)3
p/ư: 0,4<-1,2<------0,4--->1,2
=> V (NaOH) cần dùng là : V=1,2:0,5=2,4l

Na + H2O ---> NaOH + 1/2H2;
x x x/2
NaOH + HCl ---> NaCl + H2O;
0,1 0,1
Dung dịch X gồm NaCl và NaOH dư;
Số mol NaOH dư = x - 0,1 mol; lượng NaOH dư được trung hòa bằng 0,02 mol HCl nên: x - 0,1 = 0,02 hay x = 0,12 mol.
Vậy: m = 23.0,12 = 2,76 g; V = 0,06.22,4 = 1,344 lít.

Chọn A
\(\hept{\begin{cases}\text{Mg, Al, Zn : x mol}\\\text{Fe : y mol}\end{cases}}\)\(\Rightarrow\)\(\hept{\begin{cases}\text{nx + 2y = 0,05.2}\\\text{nx + 2y = 2.}\left(\frac{\text{5,763 - 2}}{71}\right)\end{cases}}\)
\(\Rightarrow\)y = 0,006\(\Rightarrow\) %m\(_{Fe}\) = 16,8 %

k bt mik đúng ko nhưng kệ:
Ta giải theo các bước sau.
- Tính số mol \(N O_{2}\):
- Khi kim loại \(M\) bị oxi hoá từ \(M\) → \(M^{z +}\) thì mỗi nguyên tử \(M\) nhường \(z\) electron. Mỗi phân tử \(N O_{3}^{-}\) nhận 1 electron để thành \(N O_{2}\). Vậy mỗi nguyên tử \(M\) sinh ra z phân tử \(N O_{2}\).
Nếu số mol kim loại là \(n_{M}\) thì:
- Gọi \(A\) là khối lượng nguyên tử của \(M\). Ta có:
Do đó:
\(0,9 = z \cdot \frac{16,8}{A} \Rightarrow \frac{A}{z} = \frac{16,8}{0,9} = 18,666 \ldots = \frac{56}{3} .\)Vì \(z\) là số nguyên dương, thử \(z = 3\) ta được \(A = 3 \cdot \frac{56}{3} = 56\). Khối lượng nguyên tử xấp xỉ 56 ứng với Fe (sắt).
- Kiểm tra: \(n_{F e} = \frac{16,8}{56} = 0,3\) mol và \(z = 3\) nên \(n_{N O_{2}} = 3 \cdot 0,3 = 0,9\) mol — khớp với đã cho.
Vậy kim loại \(M\) là sắt (Fe). (Phương trình tương ứng có thể viết:
\(\textrm{ }\textrm{ } F e + 6 H N O_{3} \rightarrow F e \left(\right. N O_{3} \left.\right)_{3} + 3 N O_{2} + 3 H_{2} O\).)
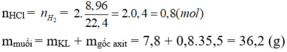


Đáp án C