Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Tính số mol các khí trong B:
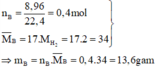
Đặt số mol các khí trong B là NO : a mol ; NO2 : b mol
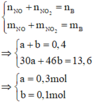
Số mol của M là: n M = 32 M m o l
Gọi n là hóa trị của M
Sơ đồ phản ứng:


a)
M + 2HCl → MCl2 + H2
nH2 = \(\dfrac{3,584}{22,4}=\)0,16 mol => nM = 0,16 mol
<=> MM = \(\dfrac{3,84}{0,16}\)= 24 (g/mol) => M là magie (Mg).
b) 8Mg + 20HNO3 → 8Mg(NO3) + 2NO + N2 + 10H2O
Từ tỉ lệ phương trình , gọi số mol N2 là x => nNO = 2x mol
=> V(NO + N2) =3x.22,4 =1,344
<=> x =0,02
=> VN2 = 0,02.22,4 =0,448 lít , VNO= 0,04.22,4 = 0,896 lít

Ta có: \(\left\{{}\begin{matrix}n_{NO}+n_{N_2}=\dfrac{5,6}{22,4}\\30n_{NO}+28n_{N_2}=7,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,1\left(mol\right)\\n_{N_2}=0,15\left(mol\right)\end{matrix}\right.\)
Giả sử M có số oxi hóa n.
BT e, có: n.nM = 3nNO + 10nN2
\(\Rightarrow n_M=\dfrac{1,8}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{21,6}{\dfrac{1,8}{n}}=12n\left(g/mol\right)\)
Với n = 2 thì MM = 24 (g/mol) là thỏa mãn.
Vậy: M là Mg.

Hòa tan hoàn toàn 15,2 gam hỗn hợp gồm Fe và Cu trong dung dịch HNO3, thu được dung dịch X và 4,48 lút khí NO. Cho 3,96 gam kim loại Mg vào X đến khi phản ứng xảy ra hoàn toàn, thu được 224ml khí NO và m gam chất rắn không tan. biết NO là sản phẩm khử duy nhất của N+5. Gía trị cảu m là
A. 6,4 B.12,8 C.9,6 D.4,8

Kim loại M có hóa trị n (n= 1,2,3)
nN2O = 6,72/22,4 = 0,3 mol => ne nhận = 0,3.8 = 2,4 mol
Áp dụng định luật bảo toàn electron => ne kim loại M nhường = 2,4 mol
Quá trình oxi hóa Quá trình khử
M → M+n + ne 2N+5 + 8e → N+12
\(\dfrac{2,4}{n}\) <----- 2,4 2,4<---- 0,3
=> nM = 2,4/n và phân tử khối M = \(21,6:\dfrac{2,4}{n}\) = 9n
=> n =3 và MM = 27 , kim loại M là nhôm (Al)

k bt mik đúng ko nhưng kệ:
Ta giải theo các bước sau.
- Tính số mol \(N O_{2}\):
- Khi kim loại \(M\) bị oxi hoá từ \(M\) → \(M^{z +}\) thì mỗi nguyên tử \(M\) nhường \(z\) electron. Mỗi phân tử \(N O_{3}^{-}\) nhận 1 electron để thành \(N O_{2}\). Vậy mỗi nguyên tử \(M\) sinh ra z phân tử \(N O_{2}\).
Nếu số mol kim loại là \(n_{M}\) thì:
- Gọi \(A\) là khối lượng nguyên tử của \(M\). Ta có:
Do đó:
\(0,9 = z \cdot \frac{16,8}{A} \Rightarrow \frac{A}{z} = \frac{16,8}{0,9} = 18,666 \ldots = \frac{56}{3} .\)Vì \(z\) là số nguyên dương, thử \(z = 3\) ta được \(A = 3 \cdot \frac{56}{3} = 56\). Khối lượng nguyên tử xấp xỉ 56 ứng với Fe (sắt).
- Kiểm tra: \(n_{F e} = \frac{16,8}{56} = 0,3\) mol và \(z = 3\) nên \(n_{N O_{2}} = 3 \cdot 0,3 = 0,9\) mol — khớp với đã cho.
Vậy kim loại \(M\) là sắt (Fe). (Phương trình tương ứng có thể viết:
\(\textrm{ }\textrm{ } F e + 6 H N O_{3} \rightarrow F e \left(\right. N O_{3} \left.\right)_{3} + 3 N O_{2} + 3 H_{2} O\).)
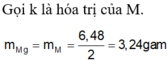

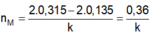
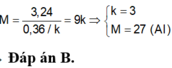
Quá trình oxi hóa
M0 -> M+n + n.e
a -------------> a.n .e
Quá trình khử
N+5 +3e ---------> N+2
mol 0,168 <------- 0,056
Theo định luật bảo toàn e :
0,168 = a . n
⇒ 0.168 = \(\dfrac{3,304}{M}\) . n
⇒ M = \(\dfrac{19}{3}\).n
Thay n ∈ {1; 2; 3} vào nhưng mà mình cứ thấy nó sai sai, bạn xem lại đề bài hộ mình ạ