Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
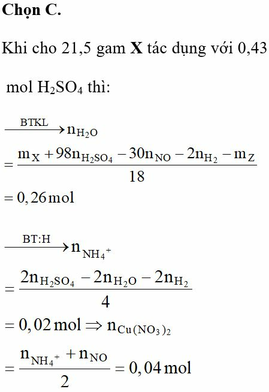
- Khi cho 21,5 gam X tác dụng với 0,43 mol H2SO4 thì:
![]()
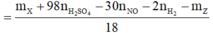
= 0,26 mol


= 0,04 mol
- Ta có
![]()

- Xét hỗn hợp X ta có:
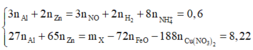
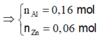
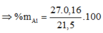
= 20,09

Đáp án C
- Khi cho 21,5 gam X tác dụng với 0,43 mol H2SO4 thì :
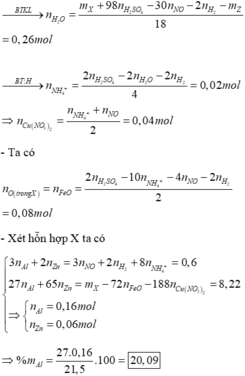

Đáp án C
- Khi cho 21,5 gam X tác dụng với 0,43 mol H2SO4 thì:

- Xét trong hỗn hợp X ta có:
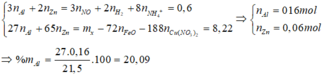

- Khi cho 21,5 gam X tác dụng với 0,43 mol H2SO4 thì:

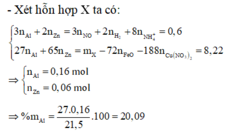
Đáp án C

Đáp án A
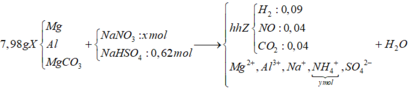
BTNT C: => nMgCO3 = nCO2 = 0,04 (mol)
BTNT: N => x = y + 0,04 (1)
BTNT : H => nH2O = ( 0,62 – 4y – 0,09.2)/2 = 0,22- 2y
BTNT: O => 3n MgCO3 + 3nNaNO3 = nH2O + nNO + 2nCO2
=> 3. 0,04 + 3x = (0,22- 2y) + 0,04 + 2.0,04
=> 3x + 2y = 0,22 (2)
Từ (1) và (2) => x = 0,06 và y = 0,02 (mol)
Bảo toàn khối lượng ta có:
mY = m(Mg2+, Al3+) + mNa+ + mNH4+ + mSO42-
= (7,98 – 0,04.60) + ( 0,06 + 0,62).23 + 0,02.18 + 0,62.96
= 81,1(g)
%mNa2SO4 = [(0,34.142):81,1].100% = 59,53% ≈ 59,5 %
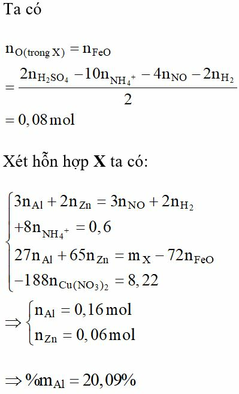

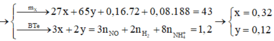
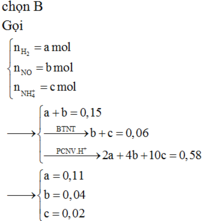
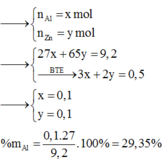


hình như là B
mình chỉ làm 1 trong 4 trường hợp nên ko biết đúng hay sai
mk làm ra câu C.
làm sao vậy?
Gọi Al:x, Zn:y, Feo:z Cu(NO3)3:t
-> 27x+65y+72z+188t=21.5 (1)
X+H2SO4-> dd Z: Al3+:x, Zn2+:y, Fe2+:z, Cu2+: t, NH4+ có thể, SO4 2-: 0.43
BTNT N: 2t=0.06+nNH4+
mhhmuối= mhhmuối+mSO42-= 50.9
<-> 27x+65y+56z+64t+18(2t-0.06)+96.0,43=56,9(2)
BTĐT trong dd Z: 3x+2y+2z+2t-0.06= 0,43.2 (3)
Bte: 3x+2y=0,06.3+0,13.2+8.(2t-0.06)
(1)(2)(3): x=0.16,y=0.06, z=0.08, t=0.04
%AL=0,16.27/21,5.100=20.09%
Gần với giá trị 20.5%
cậu tự giải bài này ak!!!!
mình làm TH có Fe3+ và ko có NH4+ vẫn có kết quả!!!!! nhìn đáp số cũng khá đẹp
cậu giải hệ 4PT 4 ẩn ghê quá
bái phục!!!!
mk cũng nhờ tiền bối gợi ý mới làm được bn à. câu này cũng là một câu khó đó.
câu nào có giá trị gần nhất đều khó cả
oh... trong đề thi nào hầu cũng có
Sao k có e nhường của Fe2+ vậy bạn
Theo mình trong dung dung có NO3- và H+ thì như có HNO3 nên có thể có Fe3+ chứ.
sai quá bạn gì đó ơi:)) rân có Fe3+ được, sản phẩm có H2 nên NO3- phải hết trước khi Fe tác dụng chứ
Đầu tiên các bạn bảo toàn khối lượng như sau:
mhỗn hợp + mH2SO4- m khí- mmuối=mH2O => mH2O=4.68g=> nH2O=0.26 mol
bảo toàn H+ như sau : nH+= 2nH2O +2nH2+4nNH4+ => nNH4+=0.02 mol
bảo toàn H+ tiếp ta có: 2nH2SO4=10nNH4+ + 4nNO +2nFeO +2nH2
=> nFeO=0.08 mol. Vấn đề còn lại ở đây là còn Fe3+ hay không hay thậm chí là cả Fe2+ trong dung dịch. Thật ra Bộ cũng đã ra kiểu bài tập có cả Fe3+ và khi vẫn có H2 . Tuy nhiên đối với kiểu bài này ta hãy mạnh giạn chọn Fe2+ trong dung dịch. => bảo toàn điện tích ta có:
3xAl +2 yZn = 0.6 kết hợp với phương trình muối hoặc phương trình khối lượng ban đầu ta tìm đc nAl=0.16 mol và %mAl=20.9 % và gần nhất với đáp ánC
vì sao bỏ fe3+ được vậy bạn, liệu nó có sai số không?
sinh ra khí H2 thì làm gì còn no3- mà ra fe3+ bạn ưi ^^
sao ko có fe+3 vậy bạn
bạn ơi bạn cho mình hỏi là tại sao lại có nh4+ vậy ạ?