Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
Gọi a và b lần lượt là số mol của Fe và Cu. Xét hỗn hợp chứa 20 gam Fe2O3 và CuO ta có :
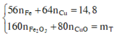
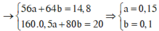
Dung dịch T gồm K+, Na+, OH- và NO3-. Khi nung chất rắn khan T thì :
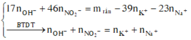

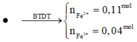
Dung dịch X gồm Fe2+, Fe3+, Cu2+(0,2 mol) và NO3- (với ). Xét X có:
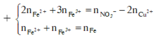
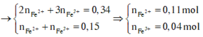
![]()
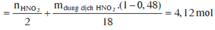
![]()
![]()

Đáp án C
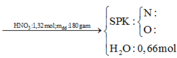
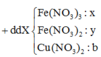
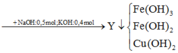
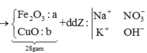
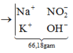
Trường hợp 1: Nếu trong dung dịch Z, số mol NO3− > số mol OH−
Vậy mran > 0,5. 85+0,4.101 = 82,9 > 66,18 → loại → Trong muối, NO3− thiếu, OH−dư.
Trường hợp 2: Hệ:
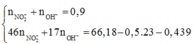
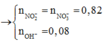
→ OH−dư, toàn bộ Fe, Cu đã kết tủa hết.
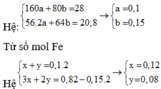
Ta có hh KL + HNO3 → Muối (Fe2+,Fe3+,Cu2+,NO3−) + Khí NxOy+ H2O
BTNT: nN trong khí = 1,32 – 0,82 = 0,5; nO trong khí = (1,32 – 0,82).3 – 0,66 = 0,84
BTKL: mddsau = 180 + 20,8 – 0,5.14 – 0,84.16 = 180,36 gam
![]()

-\(n_{Fe}=\frac{11,2}{56}=0,2mol\) \(n_{Al}=\frac{m}{27}mol\) |
-khi thêm \(Fe\) vào cốc đựng \(HCl\) ( cốc A ) có phản ứng: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) 0,2 0,2 |
theo định luật bảo toàn khối lượng, khối lượng cốc \(HCl\) tăng thêm: \(11,2-\left(0,2.2\right)=10,8g\) |
khi thêm \(Al\) vào cốc đựng dd \(H_2SO_4\) có phản ứng: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\) \(\frac{m}{27}mol\) \(\rightarrow\) \(\frac{3.m}{27.2}mol\) |
| khi cho \(m\) gam \(Al\) vào cốc B, cốc B tăng thêm : \(m-\frac{3.m}{27.2}mol\) |
để cân thăng bằng, khối lượng ở cốc đựng \(H_2SO_4\) cũng phải tăng thêm 10,8g.Có: \(m-\frac{3.m}{27.2}.2=10,8\)
|
| giải ra được \(m=\) \(\left(g\right)\) |

Chọn đáp án C
Giả sử KOH tác dụng với X thì KOH hết ⇒ n KNO 3 = n KOH = 0 , 5 mol.
⇒ m KNO 3 = 0 , 5 x 101 = 50 , 5 gam gam > 41,05 gam ⇒ vô lí ⇒ KOH dư.
Đặt n KOH dư = x mol; n KNO 3 = y mol
![]()
Phản ứng:
![]()
Giải hệ có: x = 0,05 mol; y = 0,45 mol
![]()
Đặt n Fe = a mol; n Cu = b mol ⇒ m A = 56 a + 64 b = 11 , 6 gam.
Do KOH dư ⇒ kết tủa hết ion kim loại ⇒ nung T thì rắn gồm Fe2O3 và CuO.
⇒ mrắn = 41,05 = 0,5a × 160 + 80b. Giải hệ có: a = 0,15 mol; b = 0,05 mol.
Quy hỗn hợp B về N và O. Bảo toàn nguyên tố nitơ có nN spk = 0,7 – 0,45 = 0,25 mol.
![]()
⇒ dung dịch chứa ion Fe2+, Fe3+ và H+ hết.!
Bảo toàn nguyên tố hidro có n H 2 O = 0 , 7 ÷ 2 = 0 , 35 mol.
⇒ bảo toàn nguyên tố oxi có nO sk = 0,7 × 3 – 0,45 × 3 – 0,35 = 0,4 mol.
⇒ BTKL mdung dịch sau phản ứng = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2 gam.
![]()
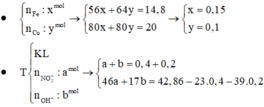
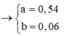


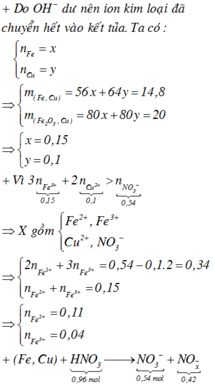
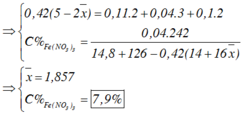




Chọn A.
Gọi a và b lần lượt là số mol của Fe và Cu. Xét hỗn hợp chứa 20 gam Fe2O3 và CuO ta có:
Dung dịch T gồm K+, Na+, OH- và NO3-. Khi nung chất rắn khan T thì:
Dung dịch X gồm Fe2+, Fe3+, Cu2+(0,2 mol) và NO3-
(với n C O 3 - = n N O 2 - = 0 , 54 m o l ).
+ Xét X có: