Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{FeO}=\dfrac{0,36}{72}=0,005\left(mol\right)\)
\(n_{H_2SO_4}=2n_{FeO}=0,01\left(mol\right)\\ \Rightarrow m_{ddH_2SO_4}=\dfrac{0,01.98}{98\%}=1\left(g\right)\\ n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{FeO}=0,0025\left(mol\right)\\ \Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,0025.400=1\left(g\right)\)

Đáp án C
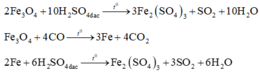
Coi oxit sắt ban đầu là hỗn hợp gồm Fe và O với nFe = a và nO = b.

Với lần thí nghiệm thứ nhất, có sự tham gia của O. Áp dụng định luật bảo toàn mol electron, ta có:
![]()
Với lần thí nghiệm thứ hai, không có sự tham gia của O. Áp dụng định luật bảo toàn mol
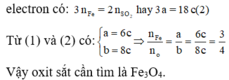

Đáp án C
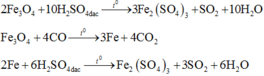
Coi oxit sắt ban đầu là hỗn hợp gồm Fe và O với nFe = a và nO = b.
Gọi thì ![]()
Các quá trình nhường và nhận electron diễn ra như sau:
Quá trình nhường electron:



\(n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)\\ \Rightarrow n_{Fe_2(SO_4)_3} = \dfrac{1}{2}n_{Fe} = 0,1(mol)\\ \Rightarrow m_{Fe_2(SO_4)_3} = 0,1.400 = 40(gam) \)
\(m_{O_2}=14.4-11.2=3.2\left(g\right)\)
\(n_{O_2}=\dfrac{3.2}{32}=0.1\left(mol\right)\)
\(O_2+4e\rightarrow2O^{2-}\)
\(0.1....0.4\)
\(S^{+6}+2e\rightarrow S^{+4}\)
\(.......0.4.....0.2\)
\(n_{H_2SO_4}=2\cdot0.2=0.4\left(mol\right)\)
\(n_{H_2O}=\dfrac{1}{2}n_{H_2SO_4}=\dfrac{0.4}{2}=0.2\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=14.4+0.4\cdot98-0.2\cdot64-0.2\cdot18=37.2\left(g\right)\)

a,\(3Fe+2O_2\rightarrow Fe_3O_4\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Fe_3O_4+8HCl\rightarrow2FeCl_3+FeCl_2+4H_2O\)
\(n_{H2}=\frac{0,448}{22,4}=0,02\left(mol\right)\)
\(\Rightarrow n_{Fe}=n_{H2}=0,02\left(mol\right)\)
\(\Rightarrow\%_{Fe}=\frac{6,72-0,02.56}{6,72}.100\%=83,33\%\)
b,\(n_{Fe3O4}=\frac{1}{30}\left(mol\right)\)
\(m_{FeCl3}=\frac{1}{15}.162,5=10,83\left(g\right)\)
\(\Rightarrow m_{FeCl2}=\left(\frac{1}{30}+0,02\right).127=6,773\left(g\right)\)

`a)`
`Fe + H_2 SO_[4(l)] -> FeSO_4 + H_2↑`
`0,02` `0,02` `(mol)`
`n_[Fe] = [ 1,12 ] / 56 = 0,02 (mol)`
`=> V_[H_2] = 0,02 . 22,4 = 0,448 (l)`
_______________________________________________
`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2 (SO_4)_3 + 6H_2 O + 3SO_2↑`
`0,02` `0,03` `(mol)`
`=> V_[SO_2] = 0,03 . 22,4 = 0,672 (l)`
a)
\(n_{Fe}=\dfrac{1,12}{56}=0,02\left(mol\right)\\ pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,02 0,02
\(V_{H_2}=0,02.22,4=0,448\left(l\right)\)
b) \(PTHH:2Fe+6H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,02 0,03
=> \(V_{SO_2}=0,03.22,4=0,672\left(l\right)\)



gọi hóa trị của Fe của oxit sắt là:x
\(Fe_2O_x+xH_2SO_4\rightarrow Fe_2\left(SO_4\right)_x+xH_2O\)
dựa vào phương trình ta thấy \(n_{Fe_2O_x}=n_{Fe_2\left(SO_4\right)_x}\):
\(\Leftrightarrow\dfrac{16}{56.2+16x}=\dfrac{40}{56.2+\left(32+64\right)x}\)
\(\Leftrightarrow x=3\)
vậy oxit sắt đó là:sắt (III) oxit (\(Fe_2O_3\)
Bạn ơi, cho mình hỏi nếu oxit sắt tác dụng với H2SO4 đặc nóng, làm sao mình biết sản phẩm nó là H2O được vậy?
vì theo định nghĩa thì axit +oxit bazo tạo thành muối và nước mà.H2SO4 ko ảnh hưởng tới nó cho dù đặc hay loãng.
sai rồi bạn
feo và fe3o4 nếu phản ứng với h2so4 đặc nóng thì tạo muối,nước và sinh ra khí so2
Mà sao bạn biết oxit sắt là fe2ox nó cx có thể là fe3o4 mà..
đề ko cho có khí tạo ra
mà đây là oxit chứ đâu phải muối sắt mà đưa lên hóa trị cao nhất