Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có 0,1 mol chất béo \(\Rightarrow\) tạo ra 0,1 mol glixerol.
\(\Rightarrow\) m = 0,1 x 92 = 9,2 gam.

Đáp án C
Nhận thấy b-c= 4a ⇒ trong X có 5 liên kết π trong đó có 3 liên kết π ở gốc –COO– và 2 liên kết π ở gốc hidrocacbon C=C.
Như vậy để hidro hóa hoàn toàn 1 mol X cần dùng 2 mol H2 ⇒ = 0,3 : 2 = 0,15 mol
Bảo toàn khối lương → m x = 39 - 0,3. 2= 38,4 gam
Khi tham gia phản ứng thủy phân ⇒
![]()
Bảo toàn khối lượng → mChất rắn =
![]()
⇒ mChất rắn = 38,4 + 0,7x40 – 0,15x92 = 52,6 gam

nH2 = 6,72/22,4 = 0,3 mol
Đốt với hợp chất hữu cơ chứa C, H và O ( nếu có) thì khi đốt cháy ta có:
nCO2 - nH2O = (k-1).nHCHC
→ k = 5 = 3pC = O + 2pC = C
Mặt khác: 1pC = C + 1H2 → nX = 1/2 nH2 = 0,15mol
Bảo toàn khối lượng: m1 = 39 – mH2= 39 - 0,3.2 = 38,4 g
Dễ thấy NaOH dư → nglixerol = nX = 0,15 mol
→ m2 = m1 + mNaOH – mglixerol = 38,4 + 0,7.40 – 0,15.92 = 52,6 g
→ Đáp án D

Đáp án D
► Đối với HCHC chứa C, H và có thể có O thì:
nCO2 – nH2O = (k – 1).nHCHC (với k là độ bất bão hòa của HCHC).
► Áp dụng: b – c = 4a ⇒ k = 5 = 3πC=O + 2πC=C.
⇒ nX = nH2 ÷ 2 = 0,15 mol || Bảo toàn khối lượng:
m1 = 39 – 0,3 × 2 = 38,4(g). Lại có: nNaOH ÷ nX > 3.
⇒ NaOH dư ⇒ nglixerol = nX = 0,15 mol. Bảo toàn khối lượng:
||⇒ m2 = 38,4 + 0,7 × 40 – 0,15 × 92 = 52,6(g)

Chọn đáp án B
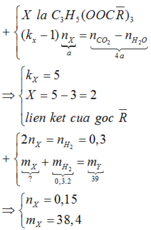
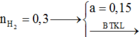
n N a O H n X > 3
Suy ra: NaOH dư, chất rắn bao gồm R C O O N a và NaOH dư
C 3 H 5 O O C R 3 + 3 N a O H → C 3 H 5 O H 3 + c h ấ t r ắ n
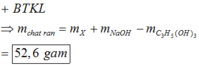

Chọn đáp án C
Nhận thấy b-c= 4a ⇒ trong X có 5 liên kết π trong đó có 3 liên kết π ở gốc –COO– và 2 liên kết π ở gốc hidrocacbon C=C.
Như vậy để hidro hóa hoàn toàn 1 mol X cần dùng 2 mol H2 ⇒ nX = 0,3 : 2 = 0,15 mol
Bảo toàn khối lương → mX = 39 - 0,3. 2= 38,4 gam
Khi tham gia phản ứng thủy phân ⇒ nC3H5(OH)3 = nX = 0,15 mol
Bảo toàn khối lượng → mChất rắn = mX + mNaOH - mC3H5(OH)3
⇒ mChất rắn = 38,4 + 0,7x40 – 0,15x92 = 52,6 gam