Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
![]()
![]()
Vì sau phản ứng thu được 0,75 gam chất rắn → có chưa Fe dư và Cu
Xét các quá trình cho ─ nhận electron
Fe →Fe2+ + 2e 4H+ + NO−3 + 3e → NO + H2O
0,08 0,04 → 0,06 → 0,02 mol
Cu2+ + 2e → Cu
0,04 → 0,08 → 0,04
V N O = 0 , 02 . 22 , 4 = 0 , 448 ( L )
Bảo toàn electron:
![]()

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến

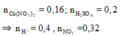
Vì thu được hỗn hợp bột kim loại nên Fe còn dư sau các phản ứng, trong dung dịch chứa Fe2+.
Coi các quá trình phản ứng xảy ra như sau:
3Fe + 8H+ + 2NO3- ⟶ 3Fe2+ + 2NO + 4H2O
Mol 0,15 0,4 0,1
Fe + Cu2+ ⟶ Fe2+ + Cu
Mol 0,16 0,16 0,16
⇒ 0,6m = m - 56(0,15 + 0,16) + 64.0,16
⇔ m = 17,8; V = 0,1.22,4 = 2,24 (lít)
Đáp án C

Đáp án B
Sau phản ứng thu được 0,6m gam hỗn hợp kim loại, chứng tỏ Fe dư. Suy ra dung dịch sau phản ứng chứa các ion
![]()
Áp dụng bảo toàn điện tích cho dung dịch sau phản ứng và bảo toàn electron, ta có :


Đáp án C
nCu2+ = 0,16 ; nNO3- = 0,32 ;
nH+ = 0,4 mol
Vì sau phản ứng thu được 0,6m gam hỗn hợp KL
=> là Cu, Fe dư => Chỉ tạo muối Fe2+
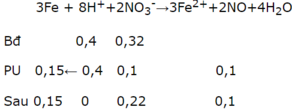
=> VNO(đktc) = 0,1.22,4 = 2,24 (lít)
Fe + Cu2+→ Fe 2++Cu↓
PƯ 0,16← 0,16
Độ giảm khối lượng kim loại = mFe pư - mCu
m – 0,6m = (0,15+0,16).56 – 0,16 .64
0,4m = 7,12 => m= 17,8g
Chú ý:
Fe dư chỉ tạo muối Fe2+

Đáp án C
Sơ đồ quá trình ta có:
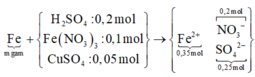
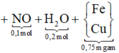
BTKL kim loại ta có:
![]() + 0,75 m
+ 0,75 m
⇔ m = 43,2 gam
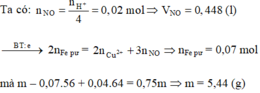

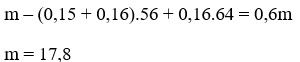
Đáp án C
Phương pháp: Viết PTHH. Chú ý do sau phản ứng thu được hỗn hợp kim loại nên Fe dư, phản ứng không tạo Fe3+, chỉ tạo Fe2+.
mchất rắn = m Fe dư + mCu => m - 0,07.56 + 64.0,04 = 0,75m => m
Hướng dẫn giải:
H+: 0,08
NO3-: 0,08
Cu2+: 0,04
3Fe + 8H+ + 2NO3-→3Fe2+ + 2NO+4H2O
0,03 0,08 0,02
Fe + Cu2+→ Fe2++Cu
0,04 0,04 0,04
m chất rắn = m Fe dư + mCu => m - 0,07.56 + 64.0,04 = 0,75m
=> m = 5,44 gam
VNO = 0,02.22,4 = 0,448 lít