Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{A_2O}=\dfrac{9,4}{2M_A+16}\left(mol\right)\)
PTHH: A2O + 2HCl --> 2ACl + H2O
\(\dfrac{9,4}{2M_A+16}\)-->\(\dfrac{9,4}{M_A+8}\)
=> \(\dfrac{9,4}{M_A+8}\left(M_A+35,5\right)=14,9\Rightarrow M_A=39\left(g/mol\right)\)
=> A là K
CTHH: K2O

gọi cthh : AO
pthh
AO+H2SO4--->ASO4+H2O
n H2O=0,5 mol
theo pthh n AO=n H2O=nH2SO4=nMSO4=0,5 mol
=> M AO= 20:0,5=40 g
=> M A=40-16=24 g
=> M là Mg
c, m H2SO4=98.0,5=49 g
d, m MgSO4=120.0,5=60 g

TL
1/ nAl = 5,4 : 27 = 0,2(mol)
4Al + 3O2 ---> 2Al2O3
0,2 ----> 0,1 (mol)
=> mAl2O3 = 0,1 x ( 27 x 2 + 16 x 3 ) = 0,2 x 102 = 20.4 (g)
2/ nAl2O3 = 30,6 : 102 = 0,3 (mol)
4Al + 3O2 ---> 2Al2O3
0,6 <---- 0,3 (mol)
=> mAl = 0,6 x 27 = 16,2 (g)
3/ B1 : Viết phương trình
B2 : Tính số mol các chất
B3 : Dựa vào phương trình hóa học tính được số mol chất cần tìm
B4 : Tính khối lượng.
Áp dụng: 1. C
2. B
3. B
Khi nào rảnh vào kênh H-EDITOR xem vid nha!!! Thanks!

a) PTHH: MO + 2HCl -> MCl2 + H2O
Ta có:
\(n_{HCl}=\frac{3,65}{36,5}=0,1\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{MO}=\frac{0,1}{2}=0,05\left(mol\right)\)
=> \(M_{MO}=\frac{4}{0,05}=80\left(\frac{g}{mol}\right)\)
Mặt khác, ta lại có:
\(M_{MO}=M_M+M_O\\ < =>M_{MO}=M_M+16\\ =>M_M=80-16=64\left(\frac{g}{mol}\right)\)
Vậy: kim loại M là đồng (KHHH là Cu)
CTPT của oxit kim loại cần tìm là CuO (đồng II oxit).

Gọi công thức hóa học của oxit là RO
→Phương trình hóa học: RO+2HCl→RCl2+H2O
nRO:8,1\(R+16nRO)= nRCl2: 13,6\R+35,5.2
⇔ 8,1.(R+71)=13,6.(R+16)
⇔ 8,1R+575,1=13,6R+217,6
⇔ 8,1R−13,6R=−575,1+217,6
⇔ −5,5R=−357,5
⇔ R=65 (Zn)
→ R là nguyên tố Kẽm (Zn)
công thức hóa học: ZnO

a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)

a/ \(3H_2+X_2O_3\rightarrow2X+3H_2O\)
b/ \(n_{H_2O}=\dfrac{m_{H_2O}}{M_{H_2O}}=\dfrac{2,7}{18}=0,15\left(mol\right)\)
Theo PTHH: \(n_{X_2O_3}=\dfrac{1}{3}n_{H_2O}=\dfrac{1}{3}.0,15=0,05\left(mol\right)\)
\(\Rightarrow M_{X_2O_3}=\dfrac{m_{X_2O_3}}{n_{X_2O_3}}=\dfrac{8}{0,05}=160\left(g/mol\right)\)
\(\Rightarrow2M_X+16.3=2M_X+48=160\)
\(\Leftrightarrow2M_X=160-48\)
\(\Leftrightarrow2M_X=112\)
\(\Leftrightarrow M_X=\dfrac{112}{2}=56\left(Fe\right)\)
Vậy kim loại đó là Fe
\(\Rightarrow CTHH:Fe_2O_3\)
c/ Theo PTHH: \(n_{Fe}=\dfrac{1}{2}n_{H_2O}=\dfrac{1}{2}0,15=0,075\left(mol\right)\)
Khối lượng kim loại tạo thành:
\(m_{Fe}=n_{Fe}.M_{Fe}=0,075.56=4,2\left(g\right)\)

Đối với những bài mà đã cho biết hoá trị của nguyên tố thì em cứ gọi nguyên tố là R, rồi viết PTHH của R (hoặc hợp chất của R) phản ứng với chất đã cho.
Gọi kim loại đó là R (hoá trị II). Suy ra oxit của R có dạng RO.
PTHH: RO + 2HCl --> RCl2 + H2O
Theo PTHH: nRO = 1/2nHCl = 0,05
=> MRO = 4/0,05 = 80
=> MR = 80-16=64
Vậy R là Cu, công thức oxit là CuO.
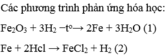
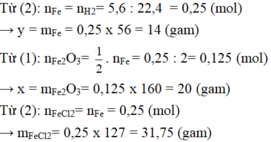
a) RO + 2HCl → RCl2 + H2O
b) Theo PT: \(n_{RO}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}\times0,1=0,05\left(mol\right)\)
\(\Rightarrow M_{RO}=\dfrac{4}{0,05}=80\left(g\right)\)
Ta có: \(M_R+16=80\)
\(\Leftrightarrow M_R=64\left(g\right)\)
Vậy R là kim loại đồng Cu
Vậy CTHH của oxit là CuO