Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Quy đổi hỗn hợp về Fe (x mol); Cu (y mol) và S (z mol)
Bảo toàn S có
nS = n↓ = 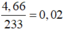 (mol)
(mol)
mX = 2,72 gam → 56x + 64y + 0,02.32 = 2,72 → 56x + 64y = 2,08 (1)
Do Y có thể hòa tan được Cu, bảo toàn electron có:
3.nFe + 2.nCu + 6.nS = 3.0,07 → 3x + 2y = 0,09 (2)
Từ (1) và (2) có: x = 0,02 và y = 0,015.
Dung dịch Y gồm: Fe3+: 0,02 mol; Cu2+: 0,015 mol; SO42- = 0,02 mol; NO3- = (0,5 – 0,07 = 0,43 mol) và có thể có H+
Bảo toàn điện tích → nH+ = 0,38 mol
Cho Cu vào Y có phản ứng:
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
0,1425 ← 0,38 0,43 mol
Cu + 2Fe3+ → Cu2+ + 2Fe2+
0,01 ← 0,02 mol
m = (0,01 + 0,1425).64 = 9,76 gam.

Dung dịch X chứa :HCl ,FeCl2 ,CuCl2
\(n_{NO} = 0,05(mol)\)
Suy ra: \(n_{HCl\ dư} = 4n_{NO} = 0,2(mol)\)
\(\Rightarrow n_{HCl\ pư} = 0,8.1,25 - 0,2 = 0,8(mol)\\ 2H^+ + O^{2-} \to H_2O\)
Suy ra : \(n_{O(oxit)} = 0,5n_{H^+} = 0,4(mol)\)
BTNT với O : \(n_{Fe_3O_4} = \dfrac{1}{4} n_{Fe_3O_4} = 0,1(mol)\\ \Rightarrow n_{FeCl_2} = 3n_{Fe_3O_4} = 0,3(mol)\\ \Rightarrow n_{Ag} = 0,3(mol)\)
BTNT với Cl : \(n_{AgCl} = n_{HCl} = 1(mol)\)
Vậy m = 0,3.108 + 1.143,5 = 175,9(gam)

Đáp án B
Thoạt nhìn đây có vẻ là một bài toán khó vì chỉ cho hai dữ liệu là số mol và dung dịch thu được chỉ chứa hai muốn sunfat. Ta cũng có thể bị mắc bẫy vì cho rằng nhưng công thức này chỉ áp dụng cho trường hợp kim loại phản ứng với HNO3. Tuy nhiên, đây là một bài toán khá đơn giản.
Vì dung dịch thu được chỉ chứa hai muối sunfat nên hết
![]()

Thoạt nhìn đây có vẻ là một bài toán khó vì chỉ cho hai dữ liệu là số mol và dung dịch thu được chỉ chứa hai muốn sunfat. Ta cũng có thể bị mắc bẫy vì cho rằng ![]() nhưng công thức này chỉ áp dụng cho trường hợp kim loại phản ứng với HNO3. Tuy nhiên, đây là một bài toán khá đơn giản.
nhưng công thức này chỉ áp dụng cho trường hợp kim loại phản ứng với HNO3. Tuy nhiên, đây là một bài toán khá đơn giản.
Vì dung dịch thu được chỉ chứa hai muối sunfat nên hết

Đáp án B
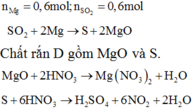
![]()
![]()
Khi cho Ba(OH)2 vào Y thu được kết tủa gồm Mg(OH)2 và BaSO4
![]()

đây ạ
nFe = 8.4/56=0.15 mol
nCu = 6.4/64=0.1 mol
nAgNO3 = 0.35*2=0.7 mol
Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag
0.15___0.3________0.15_____0.3
Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag
0.1____0.2________0.1_______0.2
nAgNO3( còn lại ) = 0.7 - 0.3 - 0.2 = 0.2 mol
Vì : AgNO3 còn dư nên tiếp tục phản ứng với Fe(NO3)2
Fe(NO3)2 + AgNO3 --> Fe(NO3)3 + Ag
Bđ: 0.15________0.2
Pư: 0.15________0.15_______________0.15
Kt: 0___________0.05_______________0.15
Chất rắn : 0.65 (mol) Ag
mAg = 0.65*108 = 70.2g
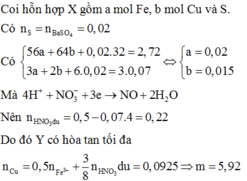

Helo ah
`=>` Chọn `C`
`Cu: 0,15 + `{(H^+: 0,4),(Fe^(3+): 0,015),(Na^+: 0,02),(NO_3: 0,065),(Cl^-: 0,4):}` `->` `X` `{(Cu^(2+)),(Fe^(2+)),(Cl^-),(Na^+),(H^+):}` `+` `NO + H_2O`
.......
??
là j thế này???
?
:)?
C
Chọn C nha
\(\left\{{}\begin{matrix}n_{HCl}=0,4\left(mol\right)\\n_{Fe\left(NO_3\right)_3}=0,015\left(mol\right)\\n_{NaNO_3}=0,02\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{H^+}=0,4\left(mol\right)\\n_{NO_3^-}=0,065\left(mol\right)\end{matrix}\right.\)
\(n_{Cu}=\dfrac{9,6}{64}=0,15\left(mol\right)\)
Gọi số mol Fe3+ pư là x (mol)
Gọi số mol Cu pư là a (mol)
Cu0 - 2e --> Cu+2
a--->2a----->a
4H+ + NO3- + 3e --> NO + 2H2O
0,26<-0,065->0,195
(Nếu NO3- dư => \(2a< 0,195\) => a < 0,0975 => Cu dư (vô lí) => Cu tác dụng với Fe3+)
Fe+3 + 1e --> Fe+2
- Nếu trong X còn Fe3+
Gọi số mol Fe3+ pư là x (mol)
=> \(x< 0,015\left(mol\right)\)
Bảo toàn e: 2a = 0,195 + x < 0,21
=> a < 0,105 < 0,15 => Cu dư
=> vô lí do Cu sẽ tác dụng với lượng Fe3+ còn lại
=> dd X không còn Fe3+(tức là Fe3+ pư hết )
Bảo toàn e: 2a = 0,195 + 0,015
=> a = 0,105 (mol)
=> X chứa \(\left\{{}\begin{matrix}Cu^{2+}:0,105\left(mol\right)\\Fe^{2+}:0,015\left(mol\right)\end{matrix}\right.\)
Kết tủa thu được gồm \(\left\{{}\begin{matrix}Cu\left(OH\right)_2:0,105\left(mol\right)\\Fe\left(OH\right)_2:0,015\left(mol\right)\end{matrix}\right.\)
=> mkt = 0,105.98 + 0,015.90 = 11,64 (g)
=> C
C
cách tính khi làm trắc nghiệm á nhưng chỉ mình ông hiểu
Lỗi Latex chứ dell phải nhầm
Chọn C nha bạn