(1,0 điểm) Lấy 2 ví dụ về phản ứng oxi hóa - khử trong thực tiễn. Viết phương trình hóa học của các phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ý 1:
\(Đ_r=\dfrac{V_r}{V_r+V_{H_2O}}.100=\dfrac{50}{50+125}.100=28,57\)
Ý 2:
\(\dfrac{25.500:100}{500+V_{nước.thêm\left(ml\right)}}=16\%\\\Leftrightarrow V_{nước.thêm\left(ml\right)}=281,25\left(ml\right)\\ \Rightarrow V_{r\left(sau.pha\right)}=500+281,25=781,25\left(ml\right)\)


`#1194`
Qtr sx thép:
- Nguyên liệu: gang, sắt, thép phế liệu, khí oxygen
- Cách thực hiện:
+ Khí oxy được thổi từ dưới lò lên để đốt cháy tạp chất trong gang
+ Các oxide tạo thành ở dạng khí \(\left(\text{CO}_2;\text{ }\text{ SO}_2;...\right)\) sẽ thoát ra theo khí thải, các oxide dạng rắn \(\left(\text{SiO}_2;\text{ MnO}_2;...\right)\) sẽ tạo ra xỉ nhẹ, nổi lên trên thép nóng.
- Xỉ được tách ra để thu lấy thép.

Ở t2 độ tan 34,2g nghĩa là 34,2g CuSO4 tan trong 100g H2O, vậy 134,2g dung dịch bão hòa gồm 34,2g CuSO4 và 100g H2O
Hạ xuống t1 độ tan 20g nên trong 100g H2O chỉ hòa tan tối đa 20g CuSO4, do đó lượng CuSO4 tách ra khỏi dung dịch là 34,2 − 20 = 14,2g
Gọi công thức tinh thể là CuSO4.nH2O
Số mol CuSO4 kết tinh là 14,2/160 = 0,08875 mol
Khối lượng tinh thể tách ra là 25g nên khối lượng nước trong tinh thể là 25 − 14,2 = 10,8g
Số mol H2O là 10,8/18 = 0,6 mol
Tỉ lệ mol H2O : CuSO4 = 0,6 : 0,08875 ≈ 6,76 ≈ 7
Vậy công thức tinh thể là CuSO4.7H2O

Lượng nước cần cung cấp cho Hà Nội mỗi ngày là: V H 2 O = 8000000 . 200 = 1600000000 ( l ) = 1600000 ( m 3 ) Lượng clo cần xử lý là: m C l 2 ( C a n x u l y ) = 5 . 160000 = 8000000 ( g ) = 8000 k g


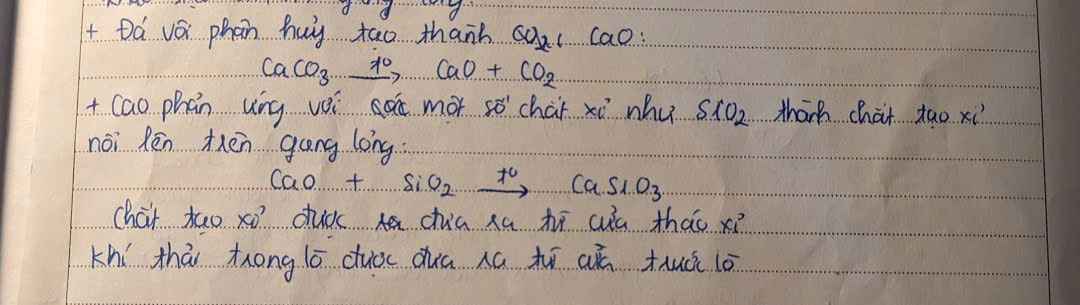
1 sự gỉ sét của sắt
PTTH :
H2O
4Fe+3O2 ---> 2Fe2O3
2 sự cháy của khí gas
PTTH:
t°
CH4 + 2O2 ---> CO2 + 2H2O
Hai ví dụ thực tế về phản ứng oxi hóa khử là đốt cháy nhiên liệu (như metan) để tạo năng lượng và sự ăn mòn kim loại (như sắt bị gỉ); phương trình ví dụ: CH4 + 2O2 -> CO2 +2H2O
4FE+3O2 +6H2O -> 4FE(OH)3