Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Este etyl axetat là chất lỏng, không tan trong nước hay các dung môi phân cực như dung dịch H2SO4, dung dịch NaOH nên sau bước 1, chất lỏng trong cả 3 ống nghiệm đều phân thành hai lớp.
→ phát biểu (d) sai, phát biểu (e) đúng.
Ở bước 2, xảy ra phản ứng thủy phân este ở hai ống nghiệm chứa axit và kiềm:
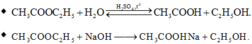
Ở ống nghiệm còn lại, phản ứng este hóa không xảy ra → Phát biểu (g) sai.
Kết thúc bước 3, như phân tích trên thì ống nghiệm chỉ có nước cất và etyl axetat thì chất lỏng vẫn phân hai lớp; ống nghiệm chứa axit H2SO4 do phản ứng xảy ra thuận nghịch, sau phản ứng vẫn còn este dư nên chất lỏng cũng phân lớp; chỉ có ống nghiệm chứa kiềm thu được muối CH3COONa nên thu được dung địch đồng nhất → có 2 ống nghiệm chất lỏng phân lớp, 1 ống nghiệm đồng nhất.
→ Các phát biểu (a), (b). (c) đều sai.
Theo đó, chỉ có duy nhất một phát biểu đúng.

Đáp án D
Đặt công thức phân tử trung bình của các chất trong X là ![]()
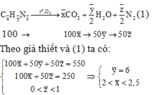
Trong X có đimetylamin (CH3)2NH, có nguyên tử H và nguyên tử C
- Với![]() , ta loại được phương án A và B (vì các hidrocacbon và amin đều có số nguyên tử H lớn hơn hoặc bằng 6)
, ta loại được phương án A và B (vì các hidrocacbon và amin đều có số nguyên tử H lớn hơn hoặc bằng 6)
- Với ![]() , ta loại được phương án C (vì các hidrocacbon và amin đều có số nguyên tử C nhỏ hoặc bằng 2).
, ta loại được phương án C (vì các hidrocacbon và amin đều có số nguyên tử C nhỏ hoặc bằng 2).
Vậy hai hidrocacbon là: C2H4 và C3H6

Gọi công thức phân tử trung bình của 2 hidrocacbon là C n H 2 n + 2 - 2 k (vì 2 hidrocacbon thuộc cùng dãy đồng đẳng nên k ∈ N ). Giả sử có X mol C2H7N và y mol CnH2n+2-2k

Vì 2 hidrocacbon là đồng đẳng kế tiếp nên 2 hidrocacbon có số nguyên tử C trong phân tử là 2 và 3.
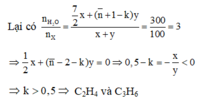
Đáp án B

Đáp án B
Gọi công thức chung của 2 hidrocacbon là CxHy . Gọi V C 2 H 7 N = a; V C x H y = b
Ta có: a + b = 100 ⇒ a = 100 – b
Khi cho Y qua H2SO4 đặc ⇒ H2O bị giữ lại
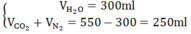
Mà = 0,5.(7a + by) ; = 2a + xb ; = 0,5a
Do vậy ⇒ 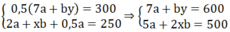
+) Từ 5a + 2xb = 500, mà a = 100 – b
⇒ 5.(100 – b) + 2xb = 500 ⇒ x = 2,5
⇒ Hai hidrocacbon đồng đẳng kế tiếp có số mol bằng nhau (vì số C trung bình = 2,5)
⇒ Số H phải là số lẻ (là trung bình cộng của 2 số chẵn liên tiếp)
+) Từ 7a + by = 600 ⇒ 7.(100 – b) + by = 600 ⇒ (7 – y)b = 100 ⇒ y < 7
Do đó, y = 3 hoặc y = 5
⇒ Hai hidrocacbon là: C2H4 và C3H6 (y = 5)
hoặc C2H2 và C3H4 (y = 3)

Đáp án B
Gọi công thức chung của 2 hidrocacbon là CxHy . Gọi V C 2 H 7 N = a; V C x H y = b
Ta có: a + b = 100 ⇒ a = 100 – b
Khi cho Y qua H2SO4 đặc ⇒ H2O bị giữ lại
V H 2 O = 300 m l V C O 2 + V N 2 = 550 - 300 = 250 m l
Mà V H 2 O = 0,5.(7a + by) ; V C O 2 = 2a + xb ; V N 2 = 0,5a
Do vậy ⇒ 0 , 5 ( 7 a + b y ) = 300 2 a + x b + 0 , 5 a = 250 ⇒ 7 a + b y = 600 5 a + 2 x b = 500
+) Từ 5a + 2xb = 500, mà a = 100 – b
⇒ 5.(100 – b) + 2xb = 500 ⇒ x = 2,5
⇒Hai hidrocacbon đồng đẳng kế tiếp có số mol bằng nhau (vì số C trung bình = 2,5)
⇒ Số H phải là số lẻ (là trung bình cộng của 2 số chẵn liên tiếp)
+) Từ 7a + by = 600 ⇒ 7.(100 – b) + by = 600 ⇒ (7 – y)b = 100 ⇒ y < 7
Do đó, y = 3 hoặc y = 5
⇒ Hai hidrocacbon là: C2H4 và C3H6 (y = 5)
hoặc C2H2 và C3H4 (y = 3)

Ta có: V H 2 O = 375 – 175 = 200 m l ; V C O 2 + V N 2 = 175 m l
V H 2 O − V H 2 O − V N 2 = 25 m l = 1 2 n h h
→ 2 hiđrocacbon chỉ có thể là anken và V a m i n = V a n k e n = 25 m l
Đặt công thức chung của 2 anken là C n ¯ H 2 n ¯ + 2
V C O 2 = 25 n ¯ + 3.25 = 25 n ¯ + 75 ; V N 2 = 0 , 5.25 = 12 , 5
→ 25 n ¯ + 75 + 12,5 = 175 → n ¯ = 3,5
Vậy 2 hiđrocacbon là C 3 H 6 v à C 4 H 8
Đáp án cần chọn là: C

\(2A\left(x\right)\rightarrow B\left(0,5x\right)+2C\left(x\right)+4D\left(2x\right)\)
Gọi số mol của A là x ta có
\(M_A=\frac{m}{x}\Rightarrow m=M_Ax\)
Theo định luật bảo toàn khối lượng ta có:
\(m=0,5xB+xD+2xE\)
Khối lượng mol trung bình của hỗn hợp khí là: 22,86g/mol nên ta có
\(\frac{0,5xB+xD+2xE}{0,5x+x+2x}=22,86\)
\(\Leftrightarrow\frac{m}{0,5x+x+2x}=22,86\)
\(\Leftrightarrow\frac{M_Ax}{0,5x+x+2x}=22,86\)
\(\Leftrightarrow\frac{M_A}{3,5}=22,86\Leftrightarrow M_A=80\)
Vậy khối lượng mol của A là: 80 g/mol
rung chị ơi
xa zậy,bth má đi học kiủ j :)))