
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nguyên tử heli có 2 proton, mỗi proton mang điện tích dương +1 nên tổng điện tích dương là +2. Phần vỏ có 2 electron, mỗi electron mang điện tích âm – 1, tổng điện tích âm là – 2. Do tổng điện tích dương và âm bằng nhau, tổng điện tích của nguyên tử heli bằng 0 nên nguyên tử heli trung hòa về điện.



6.
tổng số p của chúng là 22=> ZA + ZB= 22 (1)
ta có 4<22<32 thì A,B thuộc chu kì nhỏ: ZB - ZA=8 (2)
từ (1) và (2) =>giải hệ pt được A=7; B=15 rồi viết cấu hình bình thường
bài 7 tượng tự nhé!!!
5.theo đề bài ,ta có hệ phương trình: \(\begin{cases}2Z+N=52\\-Z+N=1\end{cases}\)
giải hệ trên,ta được:\(\begin{cases}Z=17\\N=18\end{cases}\) => Z=17(Clo)
a)kí hiệu nguyên tử \(\frac{35}{17}Cl\)
b)Cấu hình electron: \(\left[Ne\right]3s^23p^5\)
Vậy Clo nằm ở chu kì 3(3 lớp),nhóm VIIA (có 7 e ngoài cùng)
bài 6 từ từ anh giải nhé

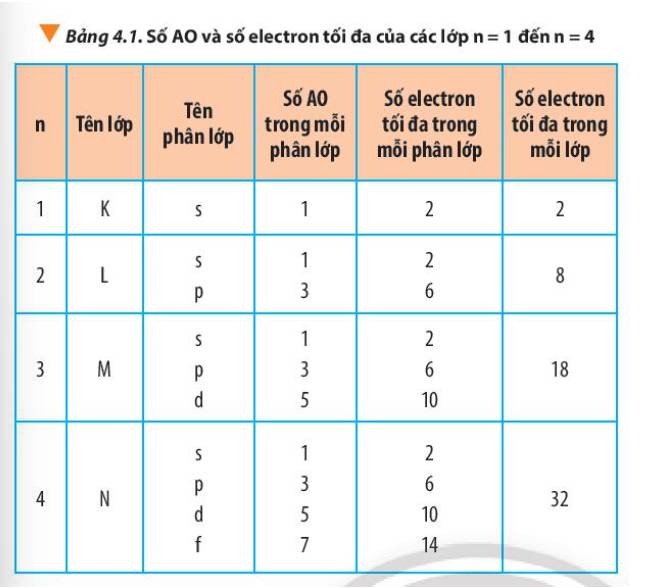
- Lớp 1 có tối đa 2 electron = 2.12
- Lớp 2 có tối đa 8 electron = 2.22
- Lớp 3 có tối đa 18 electron = 2.32
- Lớp 4 có tối đa 32 electron = 2.42
=> Số electron tối đa trong lớp n là 2n2








 ai giải cho e bài 10 vs ạaa :<
ai giải cho e bài 10 vs ạaa :< 




Hòa tan $14,\text{g Fe}$ vào dung dịch $H_2SO_4$ loãng, dư:
$Fe + H_2SO_4 \rightarrow FeSO_4 + H_2$
Số mol sắt:
$n_{Fe} = \dfrac{14}{56} = 0{,}25\ \text{mol}$
$\Rightarrow n_{FeSO_4} = 0{,}25\ \text{mol}$
Phản ứng oxi hóa – khử trong môi trường axit:
$10FeSO_4 + 2KMnO_4 + 8H_2SO_4 \rightarrow 5Fe_2(SO_4)_3 + 2MnSO_4 + K_2SO_4 + 8H_2O$
Tỉ lệ mol:
$\dfrac{n_{FeSO_4}}{n_{KMnO_4}} = \dfrac{10}{2} = 5$
Số mol $KMnO_4$ cần dùng:
$n_{KMnO_4} = \dfrac{0{,}25}{5} = 0{,}05\ \text{mol}$
Dung dịch $KMnO_4$ có nồng độ $1,M$:
$V_{KMnO_4} = \dfrac{n}{C} = \dfrac{0{,}05}{1} = 0{,}05\ \text{lít}$
$\Rightarrow V = 50\ \text{ml}$
Vậy thể tích dung dịch $KMnO_4\ 1M$ cần dùng là $50,\text{ml}$
tui ko nhìn ra gì hết