Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
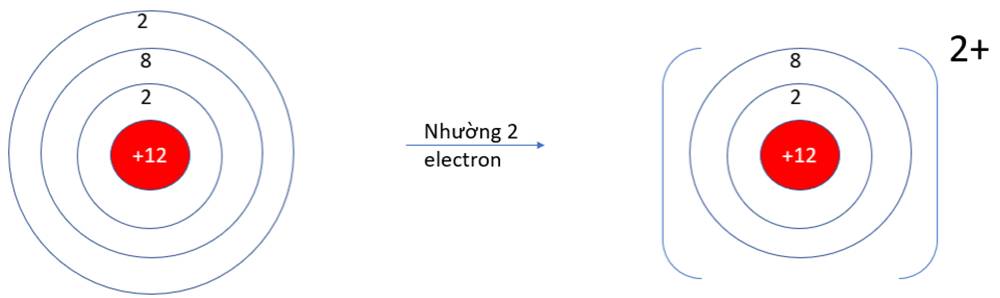
- Ở dạng nguyên tử, Na và Mg đều có 3 lớp electron. Ở dạng ion Na+, Mg2+ chỉ có 2 lớp electron
=> Bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b, Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion nên ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion nên ở điều kiện thường MgO tồn tại ở thể rắn.
c, Tá có:
+ Bán kính ion Na+ < bán kính ion Mg2+.
+ Điện tích ion Mg2+ < điện tích ion Na+.
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.

Tìm phát biểu sai trong các phát biểu sau: *
A. HF có nhiệt độ nóng chảy và nhiệt độ sôi cao bất thường.
B. Từ HCl đến HI: nhiệt độ nóng chảy và nhiệt độ sôi tăng dần theo chiều tăng phân tử khối.
C. Hiđro halogenua tan rất nhiều trong nước.
D. Tất cả các hiđro halogenua đều là chất lỏng, không màu.
=> Hầu hết ở nhiệt độ thường , các hidro halogenua đều là chất khí
Tìm phát biểu sai trong các phát biểu sau: *
A. HF có nhiệt độ nóng chảy và nhiệt độ sôi cao bất thường.
B. Từ HCl đến HI: nhiệt độ nóng chảy và nhiệt độ sôi tăng dần theo chiều tăng phân tử khối.
C. Hiđro halogenua tan rất nhiều trong nước.
D. Tất cả các hiđro halogenua đều là chất lỏng, không màu.


Đặc điểm hợp chất ion:
+ Các hợp chất ion thường là tinh thể rắn ở điều kiện thường
+ Hợp chất ion có nhiệt độ nóng chảy và nhiệt độ sôi rất cao
=> Phát biểu (b) và (c) đúng

Lực hút tĩnh điện giữa các ion ngược dấu trong tinh thể ion rất lớn. Các hợp chất ion đều khá rắn, khó bay hơn, khó nóng chảy.

Dùng criolit cấu trúc của Al2O3 bị phá vỡ nhanh hơn và nó sụp đổ nhanh hơn `->` cần ít năng lượng để nóng chảy. Cụ thể nó chỉ cần đến `900` độ chưa tới `2000` độ.
Đúng vì criolit là chất có tính acid mạnh và hấp phụ Al2O3 tăng độ bền nhiệt của hợp chất và giảm nhiệt độ nóng chảy của nó, và thêm criolit làm cho hỗn hợp trở nên dễ chảy hơn. Ngoài ra, criolit và nhôm oxit kết hợp tạo thành hợp chất có nhiệt độ nóng chảy cao hơn nhưng lại ít dễ bay hơi hơn.

Lực Van der Waals là một loại tương tác giữa các phần tử có tiếp xúc với nhau, được đặt tên của nhà vật lý người Hà Lan Johannes Diderik van der Waals, mô tả một loại tương tác phụ thuộc vào khoảng cách giữa các phần tử, công bố đầu tiên vào năm 1873. Các phần tử tham gia vào lực này thường là phân tử.
Thực chất, lực Van der Waals là lực tĩnh điện, thường xuất hiện giữa các phân tử chất khí, khí hóa lỏng hoặc hóa rắn, và trong hầu hết các chất lỏng và chất rắn hữu cơ.
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất. Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng.
-Tương tác van der Waals làm tăng nhiệt độ sôi và nhiệt độ nóng chảy. ⟹ Khí hiếm có nhiệt độ nóng chảy thấp nhất là He và cao nhất là Xe.

Nhiệt độ nóng chảy, nhiệt độ sôi tăng từ F2 đến I2 do:
- Tương tác van der Waals giữa các phân tử tăng.
- Khối lượng phân tử tăng.

Bởi vì lực hút tĩnh điện giữa các ion ngược dấu trong tinh thể ion rất lớn. Các hợp chất ion đều khá rắn, khó bay hơn, khó nóng chảy.

So sánh nhiệt độ nóng chảy: Lực hút tĩnh điện giữa các ion ngược dấu lớn nên tinh thể ion rất bền vững. Các hợp chất ion đều khá rắn,khó bay hơi,khó nóng chảy.
Lực liên kết cộng hóa trị trong tinh thể nguyên tử rất lớn, vì vậy tinh thể nguyen tử đều bền vững, khá cững, khó nóng chảy, khó bay hơi.
Trong tinh thể phân tử các phân tử hút nhau bằng lực tương tác yếu giữa các phân tử. Vì vây tinh thể phân tử dễ nóng chảy, dễ bay hơi.
Dễ
tại vì NaCl có liên kết icon, còn HCl có liên kết cộng hoá trị, mà liên kết ion có nhiệt độ nóng chảy cao hơn liên kết cộng hoá tị nên NaCl có nhiệt độ nóng chảy cao hơn HCl