
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Mình hệ thống lại tính chất hóa học của các loại oxit để bạn dễ học nhé 👇
1. Oxit axit (thường là oxit của phi kim hoặc kim loại có số oxi hoá cao, ví dụ: SO₂, CO₂, P₂O₅, N₂O₅, …)
- Tác dụng với nước → tạo dung dịch axit.
\(S O_{3} + H_{2} O \rightarrow H_{2} S O_{4}\) - Tác dụng với bazơ → tạo muối và nước.
\(C O_{2} + C a \left(\right. O H \left.\right)_{2} \rightarrow C a C O_{3} \downarrow + H_{2} O\)
2. Oxit bazơ (thường là oxit của kim loại, ví dụ: Na₂O, CaO, CuO, Fe₂O₃, …)
- Tác dụng với nước → tạo dung dịch bazơ (nếu oxit tan).
\(C a O + H_{2} O \rightarrow C a \left(\right. O H \left.\right)_{2}\) - Tác dụng với axit → tạo muối và nước.
\(C u O + 2 H C l \rightarrow C u C l_{2} + H_{2} O\)
3. Oxit lưỡng tính (ZnO, Al₂O₃, Cr₂O₃, …)
- Tác dụng với axit → tạo muối và nước.
\(Z n O + 2 H C l \rightarrow Z n C l_{2} + H_{2} O\) - Tác dụng với bazơ mạnh (khi nung nóng hoặc dung dịch kiềm đặc) → tạo muối và nước.
\(Z n O + 2 N a O H \rightarrow N a_{2} Z n O_{2} + H_{2} O\)
4. Oxit trung tính (CO, NO, N₂O, …)
- Không tác dụng với axit, bazơ, muối, cũng không tác dụng với nước.
✅ Tóm gọn:
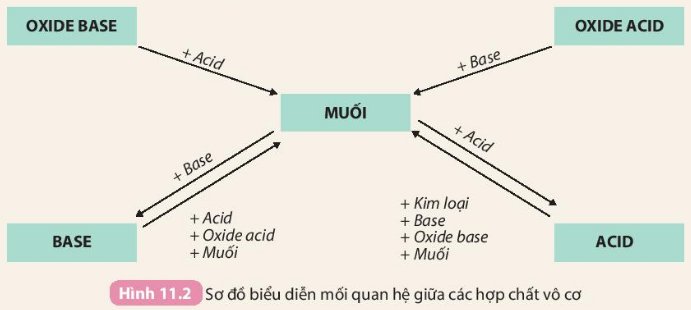
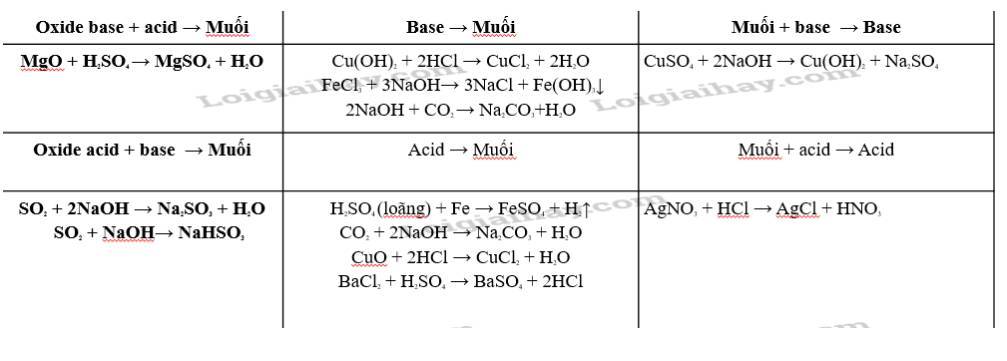
- Oxit axit + bazơ → muối + nước.
- Oxit bazơ + axit → muối + nước.
- Oxit lưỡng tính + axit/bazơ → muối + nước.
- Oxit trung tính: hầu như không phản ứng.

- muối tác dụng với kim loại tạo ra muối mới và kim loại mới (với kim loại tham gia phản ứng mạnh hơn kim loại có trong muối)
- muối tác dụng với aicd tạo thành muối mới và acid mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với base tạo thành muối mới và base mới (với sản phảm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với muối tạo thành 2 muối mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)

Tóm tắt về axit (acid):
- Khái niệm axit:
Axit là những hợp chất phân tử chứa nguyên tử hydrogen liên kết với gốc axit. Khi tan trong nước, axit giải phóng ion \(H^{+}\). - Cấu tạo:
Công thức phân tử axit gồm một hoặc nhiều nguyên tử hydrogen và một gốc axit (gốc phần còn lại của phân tử). - Tính chất:
- Dung dịch axit làm giấy quỳ tím chuyển sang màu đỏ.
- Một số kim loại phản ứng với dung dịch axit, tạo ra muối và khí hydrogen \(H_{2}\).
- Ứng dụng:
Các axit như sulfuric acid (H₂SO₄), hydrochloric acid (HCl), acetic acid (CH₃COOH) có nhiều ứng dụng quan trọng trong sản xuất và đời sống hàng ngày.

oxide base: \(Na_2O\) (tác dụng với nước tạo base)
oxide acid: \(SO_3\) (tác dụng với nước tạo acid)
oxide lưỡng tính: \(Al_2O_3\) (tác dụng được với `H_2O`, acid, base)
oxide trung tính: \(N_2O\) (không có tính chất base, acid)
Oxit bazo: Na2O
Oxit Axit: SO3
Oxit lưỡng tính: Al2O3
Oxit trung tính: N2O

- Tính chất hoá học của oxide base:
+ Tác dụng với oxide acid: MgO + CO2 -> MgCO3
+ Tác dụng với dung dịch acid: MgO + 2HCl -> MgCl2 + H2O
+ Tác dụng với nước tạo dung dịch base: MgO là oxide base không tan nên không có phản ứng với nước.
- Tính chất hoá học của oxide acid:
+ Tác dụng với oxide base: SO2 + K2O -> K2SO3
+ Tác dụng với dung dịch base: SO2 + 2 KOH -> K2SO3 + H2O
+ Tác dụng với nước tạo dung dịch acid: \(SO_2+H_2O⇌H_2SO_3\)

Oxide acid: CO2 , SO2, SO3
Oxide bazo: CuO, Na2O,
Oxide lưỡng tính: Al2O3
Để nhận biết axit và bazơ (base) trong phòng thí nghiệm hoặc trong sách hóa học, có một số cách cơ bản dựa vào tính chất hóa học và chất chỉ thị. Mình sẽ tóm tắt dễ hiểu:
1️⃣ Dùng giấy quỳ tím
2️⃣ Dùng chất chỉ thị khác
3️⃣ Dựa vào tính chất hóa học
4️⃣ Lưu ý
Nếu muốn, mình có thể làm cho bạn bảng tổng hợp nhanh nhận biết axit – bazơ thật ngắn gọn, dễ nhớ, có thể dán trong vở. Bạn có muốn mình làm không?
nếm thử là dc
nếm có chết ko hay sống thọ hơn
thử mà xem
chịu lỡ die thì sao