
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Fe.pu}=x\)
\(n_{Fe}=\frac{8}{56}=\frac{1}{7}\left(mol\right)\)
\(PTHH:Fe+CuSO_4\rightarrow Cu+FeSO_4\)
(mol) x x x x
Theo đề bài ta có:
\(64x-56x=8,8-8\Leftrightarrow x=\frac{0,8}{8}=0,1\left(mol\right)\)
\(m_{Cu}=64x=64.0,1=6,4\left(g\right)\\ m_{Fe.du}=\left(\frac{1}{7}-0,1\right).56=2,4\left(g\right)\)
\(V_{ddspu}=22,4.0,1+0,5-22,4.0,1=0,5\left(l\right)\)
\(C_{M_{FeSO_4}}=\frac{0,1}{0,5}=0,2\left(M\right)\)
\(C_{M_{CuSO_4}}=\frac{\left(2.0,5\right)-0,1}{0,5}=1,8\left(M\right)\)

Bài 2: PTHH: FeO + 2HCl → FeCl2 + H2O
Fe + 2HCl → FeCl2 + H2 ↑
Số mol của H2 là: 2,24 : 22,4 = 0,1 mol
Số mol của Fe là: 0,1 mol
Khối lượng của Fe trong hỗn hợp là: 0,1 . 56 = 5,6 gam
1) btoàn klg=>mCO2=mcr ban đầu-m cr sau=20-15,6=4,4 gam
=>nCO2=0,1 mol
=>VCO2=2,24 lit

PTHH: 3Fe+2O2--->Fe3O4
nO2=4,48:22,4=0,2mol
theo PTHH: 2molO2---->3molFe
0,2molO2---->0,3molFe
==>mFe=0,3.56=16,8g
theo PTHH: 2molO2--->1molFe3O4
0,2molO2--->0,1molFe3O4
==>mFe3O4=0,1.232=23,2g
Cô nghĩ là bài này áp dụng ở đktc, e cứ áp dụng đktc để tính nhé.

Do HNO3 nóng dư nên Fe, Cu pứ hết --> Fe3+ & Cu2+
M(B) = 36 --> nNO : nNO2 = 5:3
Khi cho đ sau pứ tác dụng vs NH3 dư thì --> Fe(OH)3 ko tan, Cu(NH3)4(OH)2 tan
--> Chất rắn sau nung: Fe2O3: n = 0,05 --> nFe = 0,1 -->mFe = 5,6, mCu = 6,4g
Từ nFe, nCu, bảo toàn electron --> nNO, nNO2 --> V
c, Dung dịch kiềm> Vì trong dd D có NH4NHO3, nên cho kiềm vào sẽ sinh ra NH3.

Gọi số mol SO2 là x thì nS là x và nO là 2x.
Gọi số mol SO3 là y thì nS là y và nO là 3y.
Theo đề bài ta có hệ phương trình:
(x+y)x32=2,4
và (2x+3y)x16=2,8
Giải hệ phương trình ta được x=0,05 và y=0,025
Vậy nSO2/nSO3= x/y =0,05/0,025 = 2/1
gọi số mol so2 là x thì ns là x và no là 2x.
gọi số mol so3 là y thì ns là y và no là 3y.
theo đề bài ta có hệ phương trình:
(x+y)x32=2,4
và (2x+3y)x16=2,8
giải hệ phương trình ta được x=0,05 và y=0,025
vậy nso2/nso3= x/y =0,05/0,025 = 2/1

Tham khảo:
nNO2 = 0,2 mol. Gọi nCu = x, nCuO = y (mol)
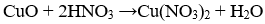
Có hệ phương trình:
mCu = 64.0,1= 6,4g; mCuO = 8,0g
Cu + 4HNO3---- > Cu(NO3)2 + 2NO2 +2H2O
CuO +2HNO3--->Cu(NO3 )2 + H2O
Gọi n\(_{Cu}=x\Rightarrow m_{Cu}=64x\)
n\(_{CuO}=y\Rightarrow m_{CuO}=80y\)
=> 64x +80y=14,4(1)
Mặt khác
n\(_{NO2}=\frac{4,48}{22,4}=0,2\left(mol\right)\left(2\right)\)
Từ 1 và 2 ta có hệ pt
\(\left\{{}\begin{matrix}64x+80y=14,4\\2x=0,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
m\(_{CuO}=80.0,1=8\left(g\right)\)
m\(_{Cu}=64.0,1=6,4\left(g\right)\)
Chúc bạn học tốt

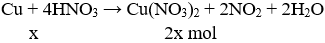
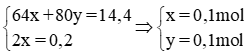
Có chán á:)
:))))
Tôi thấy chán quá vì đi học