Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2KMnO4-to>K2MnO4+MnO2+H2O
a)khí thu đc ko màu ,ko mùi , ko vị
b) do đẩy nước nên khi nào khí đấy hết nước ra khỏi ông thì sẽ ống sẽ đầy oxi

thí nghiệm 2
ko thể ẩn pít tong đc
mk chỉ bt thế thôi (mới hc qua)

Hình dạng:
| Thể rắn | Thể lỏng | Thể khí |
Hình dạng | Hình dạng cố định | Hình dạng theo vật chứa
| Hình dạng theo vật chứa |
Khả năng chịu nén | Rất khó nén | Khó nén | Dễ nén |

Tham khảo
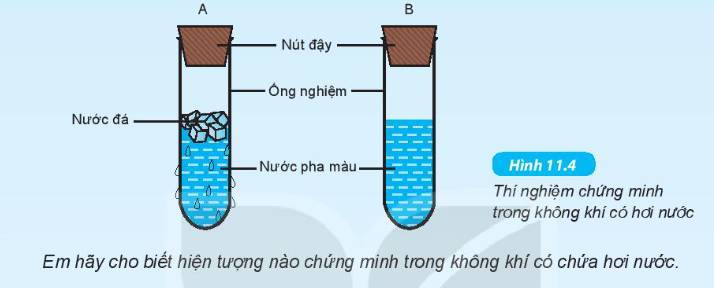
Hiện tượng xuất hiện các giọt nước bám bên ngoài ống nghiệm A cho thấy trong không khí chứa hơi nước.
Vì ống A chứa nước đá nên nhiệt độ thấp khiến cho hơi nước bên ngoài bị ngưng tụ, bám vào thành ống nghiệm tạo thành các giọt nước.

Chất tan trong nước: muối ăn, đường
Chất không tan trong nước: đá vôi

Ống nghiệm them một thìa ethanol: có hòa tan thành hỗn hợp đồng nhất
Ống nghiệm them một thìa dầu ăn: không hòa tan, tách lớp

Cho dầu ăn vào nước thu được hỗn hợp không đồng nhất
Cho etanol vào nước thu được hỗn hợp đồng nhất
Ethanol là chất tan hoàn toàn trong nước. Hỗn hợp thu được là hỗn hợp đồng nhất.

Bước 1: Xác định phản ứng hóa học
Đốt nóng đồng trong không khí (chỉ xét phản ứng với O\(_{2}\)):
\(2 \text{Cu} + \text{O}_{2} \rightarrow 2 \text{CuO}\)
Bước 2: Tính số mol đồng
Khối lượng đồng: \(m_{\text{Cu}} = 0,5 \&\text{nbsp};\text{g}\)
Khối lượng mol Cu: \(M_{\text{Cu}} = 63,5 \&\text{nbsp};\text{g}/\text{mol}\)
\(n_{\text{Cu}} = \frac{0,5}{63,5} \approx 0,00787 \&\text{nbsp};\text{mol}\)
Bước 3: Tính số mol O\(_{2}\) tham gia phản ứng
Phản ứng: \(2 \text{Cu} + \text{O}_{2} \rightarrow 2 \text{CuO}\)
\(n_{\text{O}_{2}} = 0 , 5 \cdot n_{\text{Cu}} = 0 , 5 \cdot 0,00787 \approx 0 , 003935 \&\text{nbsp};\text{mol}\)
Bước 4: Tính thể tích khí O\(_{2}\) tiêu thụ
Ở đktc, 1 mol khí ≈ 22,4 L
V_{\text{O}_2,tiêu}} = 0,003935 \cdot 22,4 \approx 0,0882\ \text{L} \approx 88,2\ \text{ml}
Bước 5: Dự đoán tổng thể tích khí còn lại
\(V_{\text{kh} \overset{ˊ}{\imath} ,\&\text{nbsp};\text{c} \overset{ˋ}{\text{o}} \text{n}} \approx 100 - 88 , 2 \approx 11 , 8 \&\text{nbsp};\text{ml}\)
✅ Kết luận
1️⃣ Số mol Cu ban đầu
\(n_{C u} = \frac{0,5}{63,5} = 7,87 \times 10^{- 3} \&\text{nbsp};\text{mol} .\)
2️⃣ Lượng O₂ bị Cu phản ứng
Theo PTHH,
\(2 C u + O_{2} \rightarrow 2 C u O \Rightarrow n_{O_{2}} = \frac{n_{C u}}{2} = 3,93 \times 10^{- 3} \&\text{nbsp};\text{mol} .\)
3️⃣ Kiểm tra lượng O₂ có đủ không
Không khí gồm khoảng 20% O₂ và 80% N₂ (theo thể tích).
Tổng thể tích ban đầu 100 mL → thể tích O₂ ban đầu:
\(V_{O_{2} , 0} = 0,2 \times 100 = 20 \&\text{nbsp};\text{mL} .\)
Số mol O₂ trong 20 mL (ở đkc hoặc cùng điều kiện với không khí):
\(n_{O_{2} , 0} = \frac{20}{22,4 \times 10^{3}} = 8,93 \times 10^{- 4} \&\text{nbsp};\text{mol} .\)
So sánh:
⟹ Không khí không đủ O₂ — toàn bộ O₂ trong không khí bị phản ứng hết.
Do đó Cu chỉ phản ứng một phần, dùng hết lượng O₂ sẵn có.
4️⃣ Khi phản ứng hết O₂
Sau khi nung và phản ứng hoàn toàn:
Ban đầu 100 mL không khí = 20% O₂ + 80% N₂
→ \(V_{O_{2} , 0} = 20 \&\text{nbsp};\text{mL}\), \(V_{N_{2} , 0} = 80 \&\text{nbsp};\text{mL}\).
Sau phản ứng, khí còn lại chỉ có N₂.
5️⃣ Khi nguội về nhiệt độ ban đầu
Sau khi nguội, thể tích tỉ lệ với số mol khí (nếu cùng P, T ban đầu).
Ban đầu tổng thể tích = 100 mL
O₂ chiếm 20 mL, bị mất → thể tích khí còn lại:
\(V_{\text{c} \overset{ˋ}{\text{o}} \text{n}} = 100 - 20 = 80 \&\text{nbsp};\text{mL} .\)
✅ Kết luận:
\(V_{\text{c} \overset{ˋ}{\text{o}} \text{n}} = 80 \&\text{nbsp};\text{mL} .\)
hóa học sách nào vậy bạn
silicon là gì?