Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Nguyên tử của nguyên tố có 6 electron ở lớp ngoài cùng.
b) Cấu hình electron lớp ngoài cùng nằm ở lớp thứ ba.
c) Cấu hình electron của nguyên tố: 1s22s22p63s23p4.

a) Nguyên tử của nguyên tố có 6 electron ở lớp ngoài cùng.
b) Cấu hình electron lớp ngoài cùng nằm ở lớp thứ ba.
c) Cấu hình electron của nguyên tố: 1s22s22p63s23p4.

a) 9X : 1s2 2s2 2p5 Đây là F có độ âm điện là 3,98.
19A : 1s2 2s2 2p6 3s2 3p6 4s1 Đây là K có độ âm điện là 0,82.
8Z: 1s2 2s2 2p4 Đây là O có độ âm điện là 3,44.
b) Cặp X và A, hiệu số độ âm điện là: 3,98 – 0,82 = 3,16 , có liên kết ion.
Cặp A và Z, hiệu số độ âm điện là: 3,44 – 0,82 = 2,62, có liên kết ion.
Cặp X và Z, hiệu số độ âm điện là: 3,98 – 3,44 = 0,54, có liên kết cộng hóa trị có cực.

a) Tổng số electron là 7, suy ra số thứ tự của nguyên tố là 7. Có 2 lớp electron suy ra nguyên tố ở chu kì 2. Nguyên tố p có 5 electron ở lớp ngoài cùng nên thuộc nhóm VA. Đó là ni tơ. Công thức phân tử hợp chất với hidro là NH3
b) Công thức electron và công thức cấu tạo của phân tử NH3
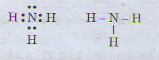

bạn xem câu trả lời của mình nhà :
Tỉ số về khối lượng của electron so với proton
Tỉ số về khối lượng của electron với nơtron
a) Viết cấu hình electron của nguyên tử Oxygen
Ta có Z = 8 vì nguyên tử trung hòa về điện nên => số e = 8
Cấu hình: 1s²2s²2p⁴
b) Viết cấu hình electron của theo ô orbital của Oxygen
Ta có cấu hình: 1s²2s²2p⁴
=> 1s 2s 2p
|↑↓| |↑↓| |↑↓|↑ |↑ |
a) 1s2 2s2 2p4
b)
a) 1s2 2s2 2p4
b)1s2 2s2 2p4
a. (1s^{2}2s^{2}2p^{4}\)
b(\frac{\mathbf{1\downarrow }}{1s}\frac{\mathbf{1\downarrow }}{2s}\frac{\mathbf{1\downarrow }}{2p_{x}}\frac{\mathbf{1\uparrow }}{2p_{y}}\frac{}{2p_{z}}\)
a.Cấu hình electron của O: 1s² 2s² 2p⁴
b. Cấu hình electron theo ô orbital :
1s: ↑↓
2s: ↑↓
2p: ↑↓ ↑ ↑