Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[}}{{\rm{H}}_{\rm{2}}}{\rm{]}}}^{\rm{3}}}{\rm{[CO]}}}}{{{\rm{[C}}{{\rm{H}}_{\rm{4}}}{\rm{][}}{{\rm{H}}_{\rm{2}}}{\rm{O]}}}} = \frac{{{{1,150}^3}.0,126}}{{0,126.0,242}} \approx 6,285\]
b) CH4 (g) + H2O (g) ⇌ 3H2 (g) + CO (g)
Ban đầu: x x
Phản ứng: 0,2 ← 0,2 ← 0,6 → 0,2
Cân bằng: (x – 0,2) (x - 0,2) 0,6 0,2
Ở 760 °C:
\[\begin{array}{l}{{\rm{K}}_{\rm{C}}}{\rm{ = }}6,285\\ \Leftrightarrow \frac{{{{{\rm{[}}{{\rm{H}}_{\rm{2}}}{\rm{]}}}^{\rm{3}}}{\rm{[CO]}}}}{{{\rm{[C}}{{\rm{H}}_{\rm{4}}}{\rm{][}}{{\rm{H}}_{\rm{2}}}{\rm{O]}}}} = 6,285\\ \Leftrightarrow \frac{{{{0,6}^3}.0,2}}{{(x - 0,2)(x - 0,2)}} = 6,285\\ \Rightarrow x \approx 0,283(M)\end{array}\]

`1>{1,2}/3->H` tính theo `H_2.`
Tại TTCB: `[H_2]=3/{2}[NH_3]=0,3M`
`->C_{H_2\ pu}=1,2-0,3=0,9M`
`->H={0,9}/{1,2}.100\%=75\%`
Không có đáp án đúng.

`N_2(g)+3H_2` $\leftrightharpoons$ `2NH_3(g)`
`K_C={[NH_3]^2}/{[N_2].[H_2]^3}={0,3^2}/{0,5.0,1^3}=180`
Không đáp án đúng.

CM(I2)=0.02M
gọi nồng độ iot chuyển hóa là x
I2(k) <=> 2I(k)
pư: x 2x
cb: 0.02-x 2x
Ta có: (2x)^2/ 0.02-x = 3,80*10^-5
=> x=4,311*10^-4
=> [I2] = 0.02-4,311*10^-4=0,019M
=>[I] = 9,5*10^-3(M)

............ ....... C... + ..CO2 <=> 2CO
Ban đầu:.. 0,2 mol......1
p.ư:............a mol.........a..............2a
Lúc cân =:0,2-a.........1-a.............2a
Kc=[CO]^2/[CO2] =(2a/22,4)^2 / [(1-a)/22,4) =0,002
Giải ra ta có a=0,1
=>Ở trạng thái cân bằng:
nCO=2.0,1=0,2 mol
nCO2=1-0,1=0,9 mol
nC=0,2-0,1=0,1 mol
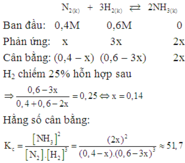

Phản ứng:
\(C H_{4} \left(\right. g \left.\right) + H_{2} O \left(\right. g \left.\right) \rightleftharpoons 3 H_{2} \left(\right. g \left.\right) + C O \left(\right. g \left.\right)\)
a) Tính \(K_{c}\) ở \(760^{\circ}\)C
\(K_{c} = \frac{\left[\right. H_{2} \left]\right.^{3} \left[\right. C O \left]\right.}{\left[\right. C H_{4} \left]\right. \left[\right. H_{2} O \left]\right.}\)Thay số: \(\left[\right. C H_{4} \left]\right. = 0.126 , \textrm{ }\textrm{ } \left[\right. H_{2} O \left]\right. = 0.242 , \textrm{ }\textrm{ } \left[\right. H_{2} \left]\right. = 1.150 , \textrm{ }\textrm{ } \left[\right. C O \left]\right. = 0.126\)
\(K_{c} = \frac{\left(\right. 1.150 \left.\right)^{3} \cdot 0.126}{0.126 \cdot 0.242} = \frac{1.150^{3}}{0.242}\)Tính ra:
\(1.150^{3} = 1.520875 , K_{c} = \frac{1.520875}{0.242} \approx 6.285\)Vậy \(K_{c} \approx 6.29\) (làm tròn 3 chữ số nghĩa).
b) Tính \(x\) khi ban đầu \(\left[\right. C H_{4} \left]\right._{0} = \left[\right. H_{2} O \left]\right._{0} = x\) và ở cân bằng \(\left[\right. H_{2} \left]\right. = 0.6\) M
Gọi \(y\) là lượng (M) CH₄ phản ứng. Từ hệ số phản ứng: \(\left[\right. H_{2} \left]\right._{e q} = 3 y\).
Vì \(3 y = 0.6 \Rightarrow y = 0.2\) M.
Vậy ở cân bằng:
\(\left[\right. C H_{4} \left]\right._{e q} = x - 0.2 , \left[\right. H_{2} O \left]\right._{e q} = x - 0.2 , \left[\right. C O \left]\right._{e q} = 0.2\)Dùng \(K_{c}\) đã tìm:
\(6.2846 \approx K_{c} = \frac{\left(\right. 0.6 \left.\right)^{3} \cdot 0.2}{\left(\right. x - 0.2 \left.\right)^{2}}\)Suy ra
\(\left(\right. x - 0.2 \left.\right)^{2} = \frac{0.6^{3} \cdot 0.2}{6.2846} \approx 0.00687394\) \(x - 0.2 = \pm \sqrt{0.00687394} \approx \pm 0.08291\)Chọn nghiệm hợp lý (vì \(x - 0.2\) phải ≥ 0) ⇒ \(x - 0.2 = 0.08291\)
\(x \approx 0.2829 \&\text{nbsp};\text{M}\)Vậy \(x \approx 0.283 \&\text{nbsp};\text{M}\).
Tóm tắt:
a) \(K_{c} \approx 6.29\).
b) \(x \approx 0.283 \&\text{nbsp};\text{M}\).
a) Tính hằng số cân bằng K
Hằng số cân bằng về nồng độ:
\(K_{c} = \frac{\left[\right. \text{CO} \left]\right. \left[\right. \text{H}_{2} \left]\right.^{3}}{\left[\right. \text{CH}_{4} \left]\right. \left[\right. \text{H}_{2}\text{O} \left]\right.}\)Thay số liệu đã cho:
\(\left[\right. \text{CH}_{4} \left]\right. = 0.126 , \left[\right. \text{H}_{2}\text{O} \left]\right. = 0.242 , \left[\right. \text{CO} \left]\right. = 0.126 , \left[\right. \text{H}_{2} \left]\right. = 1.150\) \(K_{c} = \frac{\left(\right. 0.126 \left.\right) \cdot \left(\right. 1.150 \left.\right)^{3}}{0.126 \cdot 0.242}\)Bước tính:
- \(1.150^{3} = 1.150 \cdot 1.150 \cdot 1.150 \approx 1.522\)
- Tử số: \(0.126 \cdot 1.522 \approx 0.1918\)
- Mẫu số: \(0.126 \cdot 0.242 \approx 0.0305\)
\(K_{c} \approx \frac{0.1918}{0.0305} \approx 6.29\)✅ Vậy \(K_{c} \approx 6.3\) ở 760°C.
b) Tìm nồng độ ban đầu x
Giả sử ban đầu chỉ có CH₄ và H₂O, nồng độ bằng nhau là \(x\).
Gọi mức thay đổi cân bằng là \(y\) (mol/l). Phản ứng: 1 CH₄ + 1 H₂O ⇌ 1 CO + 3 H₂.
- Nồng độ cân bằng:
\(\left[\right. \text{CH}_{4} \left]\right. = x - y , \left[\right. \text{H}_{2}\text{O} \left]\right. = x - y , \left[\right. \text{CO} \left]\right. = y , \left[\right. \text{H}_{2} \left]\right. = 3 y\)- Theo đề bài: \(\left[\right. \text{H}_{2} \left]\right. = 0.6 \&\text{nbsp};\text{M}\)
\(3 y = 0.6 \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } y = 0.2\)- Thế vào biểu thức nồng độ cân bằng:
\(\left[\right. \text{CH}_{4} \left]\right. = x - 0.2 , \left[\right. \text{H}_{2}\text{O} \left]\right. = x - 0.2 , \left[\right. \text{CO} \left]\right. = 0.2\)- Biết \(K_{c} = 6.29\), ta có:
\(K_{c} = \frac{\left[\right. \text{CO} \left]\right. \left[\right. \text{H}_{2} \left]\right.^{3}}{\left[\right. \text{CH}_{4} \left]\right. \left[\right. \text{H}_{2}\text{O} \left]\right.} = \frac{0.2 \cdot \left(\right. 0.6 \left.\right)^{3}}{\left(\right. x - 0.2 \left.\right)^{2}}\) \(6.29 = \frac{0.2 \cdot 0.216}{\left(\right. x - 0.2 \left.\right)^{2}} = \frac{0.0432}{\left(\right. x - 0.2 \left.\right)^{2}}\) \(\left(\right. x - 0.2 \left.\right)^{2} = \frac{0.0432}{6.29} \approx 0.00687\) \(x - 0.2 \approx \sqrt{0.00687} \approx 0.0829\) \(x \approx 0.2 + 0.0829 \approx 0.283 \&\text{nbsp};\text{M}\)✅ Vậy nồng độ ban đầu \(x \approx 0.283 \&\text{nbsp};\text{M}\).
Nếu muốn, mình có thể vẽ sơ đồ ICE cho bài này để dễ hình dung cách biến đổi nồng độ, đặc biệt ý b, cực trực quan. Bạn có muốn mình vẽ không?
có