Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. Trang bìa
- Tiêu đề: “Quan sát và phân biệt một số loại tế bào: vảy hành, trứng cá”
- Tên học sinh, lớp, ngày tháng.
- Có thể thêm hình minh họa nhỏ: hình kính hiển vi, tế bào.
2. Mục tiêu
- Hiểu khái niệm tế bào và cấu trúc cơ bản.
- Quan sát được tế bào hành và tế bào trứng cá dưới kính hiển vi.
- Phân biệt được sự khác nhau về hình dạng, cấu trúc giữa hai loại tế bào.
3. Chuẩn bị
- Dụng cụ: Kính hiển vi, lam kính, vật kính, giọt nước, kẹp gắp, đèn chiếu sáng.
- Mẫu vật:
- Hành tây (để quan sát tế bào vảy hành).
- Trứng cá (để quan sát tế bào trứng cá).
- Thuốc nhuộm: Lugol (iodine) để nhuộm tế bào hành.
4. Cách quan sát
Tế bào vảy hành:
- Lấy 1 mảnh mỏng của vảy hành.
- Đặt lên lam kính, nhỏ giọt nước hoặc thuốc nhuộm Lugol.
- Đặt lam kính dưới kính hiển vi và quan sát.
- Vẽ hình tế bào: nhìn thấy màng tế bào, nhân tế bào rõ ràng.
Tế bào trứng cá:
- Lấy một ít trứng cá, đặt lên lam kính, nhỏ giọt nước.
- Quan sát dưới kính hiển vi.
- Vẽ hình tế bào: hình tròn, có nhân ở giữa và bào tương trong suốt.
5. Nhận xét và phân biệt
Tiêu chí | Tế bào hành | Tế bào trứng cá |
|---|---|---|
Hình dạng | Hình chữ nhật | Hình tròn |
Nhân | Rõ ràng, nằm gần giữa | Rõ ràng, nằm giữa |
Bào tương | Trong suốt, dễ quan sát | Trong suốt, đồng nhất |
Màng tế bào | Rõ nét | Rõ nhưng mỏng |
- Kết luận: Hai loại tế bào khác nhau về hình dạng và cấu trúc, phản ánh chức năng khác nhau trong cơ thể.
6. Hình ảnh minh họa
- Chèn hình tế bào hành và tế bào trứng cá dưới kính hiển vi.
- Vẽ sơ đồ đơn giản để dễ nhớ.
7. Kết luận
- Tế bào là đơn vị cơ bản của sự sống.
- Quan sát tế bào giúp em hiểu cấu tạo, chức năng và phân biệt được các loại tế bào.
- Thí nghiệm đơn giản nhưng rất quan trọng trong sinh học.
💡 Mẹo trình bày:
- Mỗi slide: 1 ý chính + hình minh họa.
- Dùng màu sắc nhẹ nhàng, chữ dễ đọc.
- Khi thuyết trình: Giải thích bằng lời cho từng hình ảnh.
bạn làm theo như bạn ''Vũ Trường An'' sẽ hiểu hơn

Để tính khối lượng nguyên tử, ta cộng khối lượng của các hạt proton, neutron và electron trong nguyên tử đó nếu bn không hiểu có thể xem video dạy học khoa học lopws7 nha bn 🙃🙃

ngoại trừ He, các nguyên tố khí hiếm còn lại đều có số e lớp ngoài cùng là 8

Vì hạt nhân mang điện tích dương, lớp vỏ Electron mang điện tích âm

ở câu b) có ''hkí'' thì mọi người bỏ nhá vì cái đó mik viết nhầm
hình như là chữ ''hkí hiệu'' hình như hai chữ nó bn viết bị thừa ak

- Mô hình nắp chai nhựa: Sử dụng 118 nắp chai nhựa tái chế để đại diện cho các nguyên tố. Bạn có thể dán nhãn tên nguyên tố, số nguyên tử lên bề mặt nắp. Ưu điểm là rẻ, dễ tìm và có màu sắc đa dạng để phân loại nhóm nguyên tố (kim loại, phi kim, khí hiếm...).
- Bảng tuần hoàn dạng "Tổ ong": Thay vì hình vuông truyền thống, bạn có thể cắt bìa carton thành các hình lục giác và ghép lại như tổ ong để tạo hiệu ứng 3D độc đáo.
- Bảng tuần hoàn tương tác (Flip-flap): Sử dụng các ô giấy có thể mở ra (như cửa sổ). Mặt ngoài ghi ký hiệu nguyên tố, mặt trong ghi thông tin chi tiết hoặc hình ảnh ứng dụng của nguyên tố đó trong thực tế.
- Sử dụng khối lập phương (Cube): Mỗi nguyên tố là một khối lập phương nhỏ (bằng giấy hoặc gỗ), mỗi mặt hiển thị một thông tin khác nhau như cấu hình electron, khối lượng nguyên tử hoặc hình ảnh thực tế.
- Tái chế: Nắp chai, bìa carton, que kem gỗ, hộp diêm cũ.
- Trang trí: Đất sét nặn (làm mô hình nguyên tử), màu nước, bút dạ quang để làm nổi bật các quy luật biến đổi.
- Tính chính xác: Đây là yếu tố hàng đầu. Cần kiểm tra kỹ số hiệu nguyên tử, ký hiệu và vị trí của các nguyên tố trong bảng tuần hoàn hiện hành.
- Mã hóa màu sắc: Sử dụng màu sắc thống nhất để phân biệt các nhóm nguyên tố (ví dụ: nhóm kim loại kiềm một màu, khí hiếm một màu) giúp bảng trông khoa học và dễ học hơn.
- Tính ứng dụng: Điểm nhấn của dự án STEM là liên hệ thực tế. Bạn có thể dán kèm hình ảnh nhỏ minh họa cho ứng dụng của nguyên tố, ví dụ: dán hình viên pin vào ô Lithium (Li), hình cái đinh vào ô Sắt (Fe).
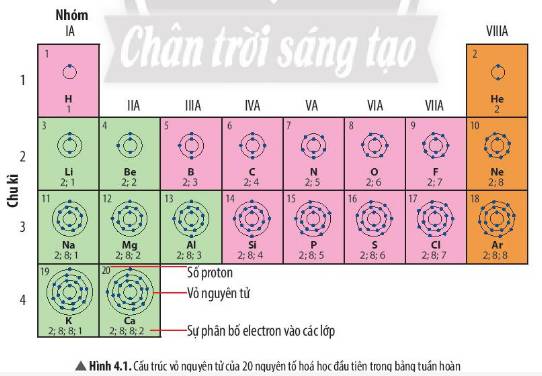
Hiểu về nguyên tử là một trong những khái niệm quan trọng trong hóa học, và nó có thể hơi khó hiểu nếu không làm quen với các khái niệm cơ bản. Mình sẽ giải thích một cách đơn giản để bạn dễ hiểu hơn nhé!
Nguyên tử là gì?
Nguyên tử là đơn vị nhỏ nhất của chất mà vẫn giữ được tính chất của chất đó. Mỗi nguyên tử có một hạt nhân ở trung tâm và các electron xung quanh. Bạn có thể tưởng tượng nguyên tử giống như một hành tinh nhỏ, trong đó hạt nhân giống như Mặt Trời và các electron là các hành tinh quay xung quanh.
Cấu tạo của nguyên tử
Lớp electron trong nguyên tử
Nguyên tử không phải là một khối vật chất đặc, mà các electron quay xung quanh hạt nhân trong các lớp (hay còn gọi là quỹ đạo electron). Các lớp này được ký hiệu là Lớp 1, Lớp 2, Lớp 3, v.v. Mỗi lớp có thể chứa một số lượng electron nhất định:
Các lớp này giống như các tầng trong một tòa nhà, mỗi lớp càng cao thì càng có thể chứa nhiều electron.
Vì sao các lớp lại quan trọng?
Ví dụ minh họa
Hãy lấy nguyên tử carbon (C) làm ví dụ:
Vậy, carbon có 4 electron ở lớp ngoài cùng. Điều này giải thích tại sao carbon có khả năng kết hợp với nhiều nguyên tử khác để tạo ra các hợp chất như CO2, CH4, v.v.
Tóm tắt
Hi vọng là bạn đã hiểu phần cơ bản về nguyên tử và các lớp electron! Nếu có câu hỏi gì thêm hoặc cần giải thích kỹ hơn, cứ hỏi mình nhé! 😊
khoa hoc 7 kho qu:[
sao bat mua vip vay?
ko cho xem het vd
SOLO FF KO BN
BÀI TRƯỚC LÀ BÀI NÀO VẬY MỌI NGƯỜI
do em ngu
Cô ơi cho em sao đi ạ