Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

A thì Si chu kì 3, còn lại chu kì 2
B tất cả chu kì 3
C có K và Fe chu kì 4, Ar chu kì 3
D có B chu kì 2 còn Al chu kì 3
=> Chọn B

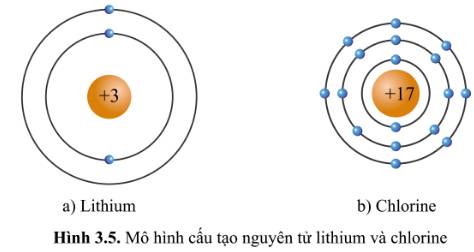
- Xét mô hình cấu tạo của nguyên tử lithium: có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp vỏ ngoài cùng => Thuộc nhóm IA
- Xét mô hình cấu tạo của nguyên tử chlorine: có 7 hình tròn xanh ở vòng tròn ngoài cùng => Có 7 electron ở lớp vỏ ngoài cùng => Thuộc nhóm VIIA

1:
Nguyên tử Li, Na có cũng số electron ở lớp ngoài cùng
Nguyên tử F, Cl có cũng số electron ở lớp ngoài cùng
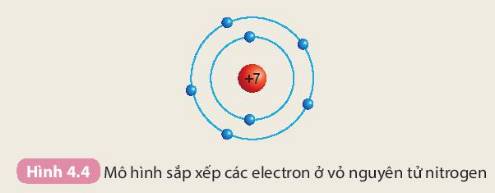
2: Số electron lớp ngoài cùng của nguyên tử các nguyên tố chính là số thứ tự nhóm của các nguyên tố

Trong phân tử \(CO\left(NH_2\right)_2\) có 2 nguyên tử N.
Trong phân tử \(\left(NH_4\right)_2SO_4\) có 2 nguyên tử N.
Trong phân tử \(NH_4NO_3\) có 2 nguyên tử N.
Trong phân tử \(Ca\left(NO_3\right)_2\) có 2 nguyên tử N.
Vậy trong cùng 1 phân tử, các chất trên đều cùng số nguyên tử N, vậy nên bác nông dân chọn loại nào cũng được.
b phải tính phần trăm nito trong đó chứ ko p tính số nguyên tử :))

3 nguyên tố Li,C,O có cùng số lớp electron trong nguyên tử là 2

Để cân bằng các phương trình hóa học trên, chúng ta sẽ sử dụng phương pháp cân bằng bán phản ứng (cân bằng oxi hóa – khử). Dưới đây là cách cân bằng từng phương trình một:
1. Phương trình: Fe²⁺ + MnO₄⁻ → Fe³⁺ + Mn²⁺
Bước 1: Viết các bán phản ứng oxi hóa và khử
(Fe²⁺ mất 1 electron)
(MnO₄⁻ nhận 5 electron)
Bước 2: Cân bằng electron
Để cân bằng số electron, ta nhân bán phản ứng oxi hóa với 5 và bán phản ứng khử với 1:
Bước 3: Cân bằng nguyên tố và điện tích
Kết hợp cả hai bán phản ứng:
Bước 4: Cân bằng phương trình
Phương trình đã được cân bằng:
\(5 F e^{2 +} + M n O_{4}^{-} + 8 H^{+} \rightarrow 5 F e^{3 +} + M n^{2 +} + 4 H_{2} O\)2. Phương trình: Cl⁻ + MnO₄⁻ → Cl₂ + Mn²⁺
Bước 1: Viết các bán phản ứng oxi hóa và khử
(Cl⁻ mất 2 electron)
(MnO₄⁻ nhận 5 electron)
Bước 2: Cân bằng electron
Để cân bằng số electron, ta nhân bán phản ứng oxi hóa với 5 và bán phản ứng khử với 2:
Bước 3: Cân bằng nguyên tố và điện tích
Kết hợp cả hai bán phản ứng:
Bước 4: Cân bằng phương trình
Phương trình đã được cân bằng:
\(5 C l^{-} + M n O_{4}^{-} + 8 H^{+} \rightarrow 5 C l_{2} + M n^{2 +} + 4 H_{2} O\)3. Phương trình: Cr₂O₇²⁻ + I⁻ → Cr³⁺ + I₂
Bước 1: Viết các bán phản ứng oxi hóa và khử
(I⁻ mất 2 electron)
(Cr₂O₇²⁻ nhận 6 electron)
Bước 2: Cân bằng electron
Để cân bằng số electron, ta nhân bán phản ứng oxi hóa với 3 và bán phản ứng khử với 1:
Bước 3: Cân bằng nguyên tố và điện tích
Kết hợp cả hai bán phản ứng:
Bước 4: Cân bằng phương trình
Phương trình đã được cân bằng:
\(6 I^{-} + C r_{2} O_{7}^{2 -} + 14 H^{+} \rightarrow 3 I_{2} + 2 C r^{3 +} + 7 H_{2} O\)4. Phương trình: NO₃⁻ + Zn → NO + Zn²⁺
Bước 1: Viết các bán phản ứng oxi hóa và khử
(Zn mất 2 electron)
(NO₃⁻ nhận 3 electron)
Bước 2: Cân bằng electron
Để cân bằng số electron, ta nhân bán phản ứng oxi hóa với 3 và bán phản ứng khử với 2:
Bước 3: Cân bằng nguyên tố và điện tích
Kết hợp cả hai bán phản ứng:
Bước 4: Cân bằng phương trình
Phương trình đã được cân bằng:
\(3 Z n + 2 N O_{3}^{-} + 10 H^{+} \rightarrow 3 Z n^{2 +} + 2 N O + 5 H_{2} O\)Tóm lại, các phương trình đã được cân bằng như sau: