Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Xét phân tử khí chlorine
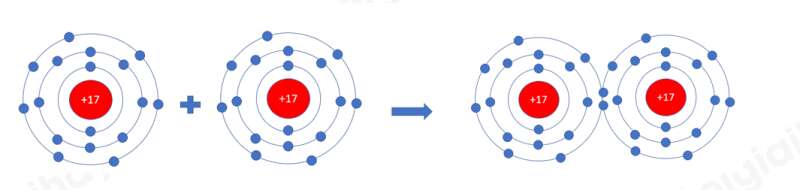
=> Mỗi nguyên tử Cl có 7 electron ở lớp ngoài cùng. Để có cấu trúc electron bền vững của khí hiếm Ar, khi hình thành phân tử chlorine, hai nguyên tử Cl đã liên kết với nhau bằng cách mỗi nguyên tử Cl góp chung 1 electron tạo thành 1 cặp electron dùng chung
- Xét phân tử khí amonia
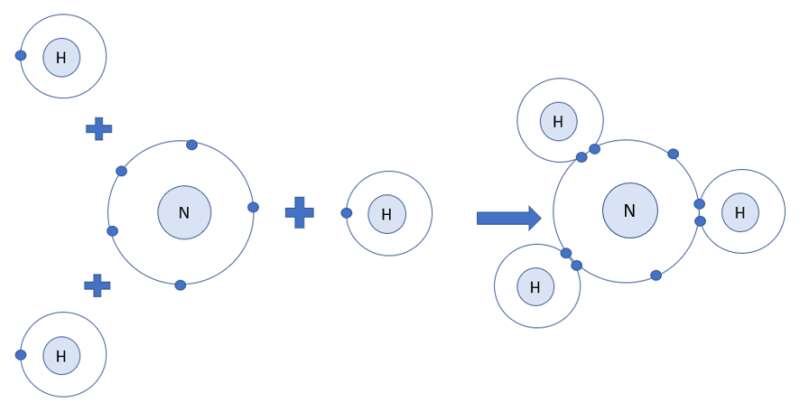
- Nguyên tử H có 1 electron ở lớp ngoài cùng
- Nguyên tử N có 5 electron ở lớp ngoài cùng
=> Nguyên tử H cần thêm 1 electron và N cần thêm 3 electron để đạt cấu hình electron bền vững của khí hiếm
=> Khi 3 nguyên tử H và 1 nguyên tử N liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử N góp ra 3 electron để tạo ra 3 đôi electron dùng chung

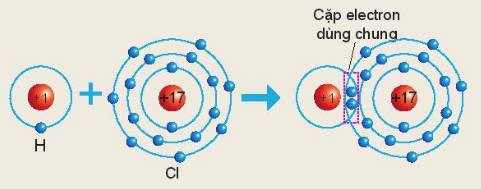
Nguyên tử `Cl` dùng chung `1` cặp electron với nguyên tử `H`
`->` Trong phân tử muối `HCl,` nguyên tử nguyên tố `Cl` sẽ có hóa trị là `I`.

Sulfur (S) nằm ở chu kì 3, nhóm VIA (hoặc nhóm 16) trong bảng tuần hoàn các nguyên tố hóa học.
Sulfur (S) nằm ở chu kì 3, nhóm VIA trong bảng tuần hoàn

Câu trả lời là Có. Nguyên tắc sắp xếp các nguyên tố hóa học để dễ nhận ra tính chất của chúng được thể hiện rõ nhất trong Bảng tuần hoàn các nguyên tố hóa học (thường được gọi tắt là Bảng tuần hoàn).

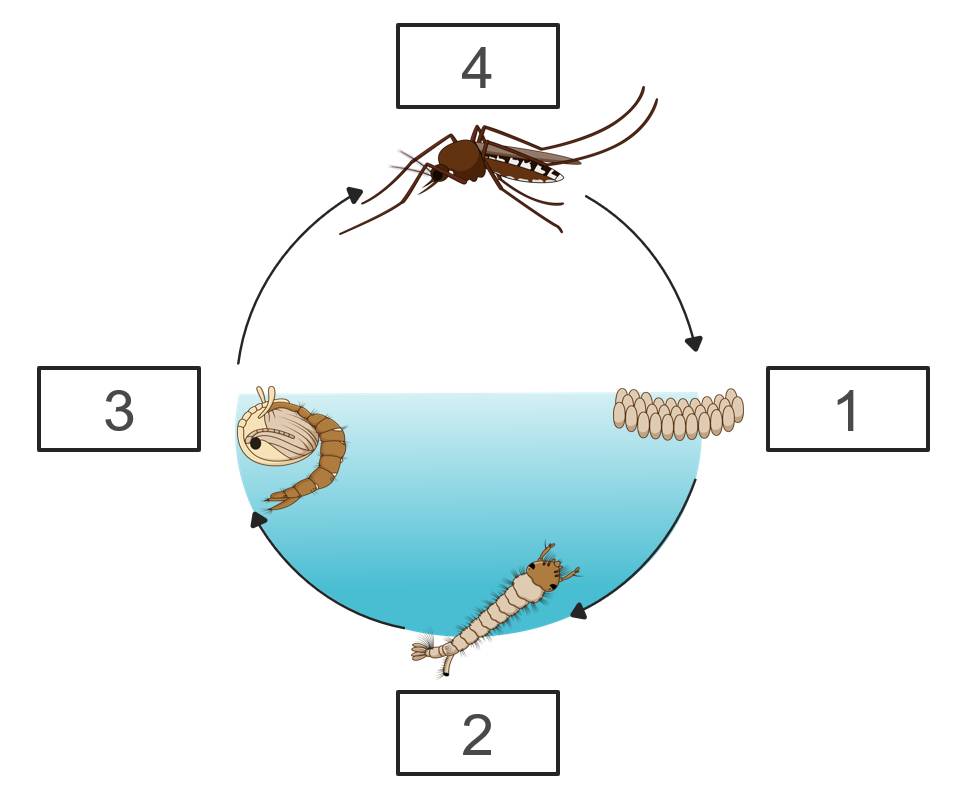
a, Giai đoạn trứng: Muỗi cái đẻ trứng trên mặt nước, thường xếp thành bè.
Giai đoạn ấu trùng (bọ gậy): Trứng nở thành ấu trùng (bọ gậy), sống trong nước, ăn các chất hữu cơ và phát triển.
Giai đoạn nhộng: Ấu trùng lột xác thành nhộng, không ăn nhưng vẫn sống trong nước và chuẩn bị biến đổi thành muỗi trưởng thành.
Giai đoạn muỗi trưởng thành: Nhộng nở thành muỗi trưởng thành, rời khỏi mặt nước để sống trên cạn, bắt đầu chu kỳ sinh sản mới.
b,
-Nên tiêu diệt muỗi ở giai đoạn ấu trùng (bọ gậy) là hiệu quả nhất.
Lý do:
-Dễ kiểm soát: Ấu trùng sống tập trung trong nước (ao, hồ, dụng cụ chứa nước), giúp dễ dàng xử lý bằng cách vệ sinh và loại bỏ môi trường nước đọng.
-Ngăn chặn số lượng lớn: Tiêu diệt ở giai đoạn này sẽ ngăn chặn chúng phát triển thành muỗi trưởng thành, giảm nguy cơ lây truyền bệnh.
-Chi phí thấp: Các biện pháp như thả cá ăn bọ gậy, sử dụng hóa chất hoặc làm sạch môi trường ít tốn kém hơn so với việc phun thuốc diệt muỗi trưởng thành.
-Tiêu diệt muỗi ở giai đoạn trưởng thành cũng hiệu quả nhưng khó khăn hơn do chúng di chuyển nhiều và lây lan nhanh.




Dưới đây là cách vẽ sơ đồ hình thành liên kết cộng hóa trị trong phân tử O₂ cùng mô tả quá trình:
1.Cấu hình electron lớp ngoài cùng của nguyên tử Oxy (O)
2.Quá trình tạo liên kết cộng hóa trị trong phân tử O₂
3.Sơ đồ mô tả liên kết cộng hóa trị trong phân tử O₂
Nếu bạn muốn, mình có thể giúp vẽ sơ đồ chi tiết hơn hoặc giải thích thêm về liên kết cộng hóa trị trong các phân tử khác!