Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
Ta có: ne = 0,12 mol ® Tại anot có khí Cl2 (x mol) và O2 (y mol) và tại catot có Cu (0,06 mol).
mà mdd giảm = 71x + 32y + 0,06.64 = 6,45 và 2x + 4y = 0,12 Þ x = 0,03 ; y = 0,015.
Dung dịch Y có chứa H2SO4 (0,015.2 = 0,03 mol) ; Na2SO4 (0,03 mol).
Khi cho 0,05 mol Fe(NO3)2 vào Y thì:
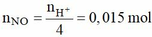
Dung dịch Z chứa Fen+ (0,05), Na+ (0,06), SO42- (0,06), NO3- (0,1 – 0,015 = 0,085) Þ m = 15,21 (g)

Đáp án B
ne = It/F = 5.(96,5.60)/96500 = 0,3 mol
nCl- (0,5) > ne (0,3) => Cl- chưa bị điện phân ở anot.
Giả sử Cu2+ chưa bị điện phân hết => nCu = 0,3/2 = 0,15 mol
nCl2 = 0,3/2 = 0,15 mol
m dung dịch giảm = mCu+mCl2 = 0,15.64 + 0,15.71 = 20,15 gam => Loại
=> Cu2+ bị điện phân hết, H2O đã bị điện phân ở catot.
Catot:
Cu2+ + 2e → Cu
x → 2x →x
H2O + 1e → OH- + 0,5H2
0,3-2x → 0,15-x
Anot:
Cl- - 1e → 0,5Cl2
0,3→ 0,15
m dung dịch giảm = mCu + mH2 + mCl2 => 17,15 = 64x + 2(0,15-x) + 0,15.71 => x = 0,1mol
=> a = 0,1/0,5 = 0,2 mol/lít

Chọn B.
Khi thoát ra tại anot gồm Cl2 (0,15 mol) và O2 (0,05 mol) Þ ne = 0,5 mol và FeCl3: 0,1 mol (BT: Cl)
Dung dịch sau điện phân chứa FeSO4 (x mol), CuSO4 dư (x mol), H2SO4 (0,1 mol)
→ BT : S nCuSO 4 = 2 x + 0 , 1 → BT : e 0 , 1 + ( 2 x + 0 , 1 - x ) . 2 = 0 , 5 ⇒ x = 0 , 1 ⇒ m = 64 , 25 ( g )

∑ne trao đổi = 0,3 mol < 2nCu2+.
⇒ Cu chưa bị điện phân hết và khí thoát ra là Cl2 và có thể có cả O2.
Nếu chỉ có khí Cl2
⇒ Quy đổi mDung dịch giảm = mCuCl2 = 0,15×135 = 20,25 ≠ 14,75 ⇒ Loại.
+ Vậy có cả O2 thoát ra
⇒ mDung dịch giảm = mCuCl2 + mCuO.
+ Đặt số mol 2 chất lần lượt là a và b ta có:
a + b = 0,15 mol (PT bảo toàn Cu).
135a + 80b = 14,75 (PT theo m dung dịch giảm).
+ Giải hệ ⇒ a = nCuCl2 = 0,05 mol
⇒ nNaCl = 0,05×2 = 0,1 mol.
⇒ CM NaCl = 0 , 1 0 , 2 = 0,5M
Đáp án D

Đáp án D
∑ne trao đổi = 0,3 mol < 2nCu2+.
⇒ Cu chưa bị điện phân hết và khí thoát ra là Cl2 và có thể có cả O2.
Nếu chỉ có khí Cl2 ⇒ Quy đổi mDung dịch giảm = mCuCl2 = 0,15×135 = 20,25 ≠ 14,75 ⇒ Loại.
+ Vậy có cả O2 thoát ra ⇒ mDung dịch giảm = mCuCl2 + mCuO.
+ Đặt số mol 2 chất lần lượt là a và b ta có:
a + b = 0,15 mol (PT bảo toàn Cu).
135a + 80b = 14,75 (PT theo m dung dịch giảm).
+ Giải hệ ⇒ a = nCuCl2 = 0,05 mol ⇒ nNaCl = 0,05×2 = 0,1 mol.
⇒ CM NaCl = 0,1/0,2 = 0,5M

Đáp án D
Dun dịch X gồm AgNO3 dư (x mol) và HNO3 (x mol)
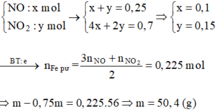
Dung dịch Y chứa Fen+ (0,05 mol) và NO3- (0,14 mol) => m = 11,48 (g).


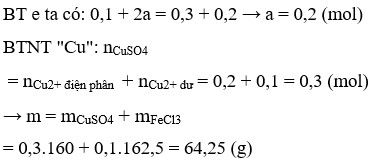

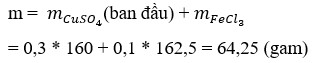

nNACL : 80÷50,8=1,3(mol)
Khối lượng naoh lý thuyết dược tạo thành
1,3 × 40=54,7
Khối lượng naoh thực tế được tạo thành
54,7× 0,8= 43,76
Phương trình điện phân dung dịch NaCl:
2NaCl + 2H₂O → 2NaOH + H₂ + Cl₂
Khối lượng NaCl trong 1 lít nước muối bão hòa = 300 g
Khối lượng mol của NaCl = 23 + 35.5 = 58.5 g/mol
Số mol NaCl = 300 g / 58.5 g/mol ≈ 5.128 mol
Theo phương trình điện phân, 2 mol NaCl tạo ra 2 mol NaOH. Vậy số mol NaOH tạo ra bằng số mol NaCl đã điện phân.
Số mol NaOH lý thuyết = Số mol NaCl = 5.128 mol
Số mol NaOH thực tế = 5.128 mol ×80% = 4.1024 mol
Khối lượng mol của NaOH = 23 + 16 + 1 = 40 g/mol
Khối lượng NaOH = 4.1024 mol × 40 g/mol ≈ 164.096 g
=>Với mỗi lít nước muối bão hoà ban đầu có thể sản xuất được khoảng 164.096 gam sodium hydroxide.
Với 1 lít nước muối bão hòa ban đầu, có thể sản xuất được khoảng 43,8 g NaOH.
nNACL : 80÷50,8=1,3(mol) Khối lượng naoh lý thuyết dược tạo thành 1,3 × 40=54,7 Khối lượng naoh thực tế được tạo thành 54,7× 0,8= 43,76
Mỗi lít ôic muố bão hoà ban đầu, có thể sản xuất đc khoang 43,76 g sodium hydro
Khối lượng sodium hydroxide sản xuất được là 43.76 gam.
Fhkuhkygi
43,76 gam.
43,67
NaCl phản ứng :
300 - 220 = 80 g
Theo PTHH : NaCl /NaOH = 1/1
m NaOH = 80 * 40/58,7 g
Tính hiệu suất 80% :
54,7 * 0,8 = 44 g
Đáp án : Khoảng 44 g NaOH
Với mỗi lít nước muối bão hòa ban đầu, có thể sản xuất được khoảng 43,76 gam sodium hydroxide (NaOH).
Khối lượng sodium hydroxide có thể sản xuất được là 43,59g
Với mỗi lít nước muối bão hoà ban đầu có thể sản xuất được khoảng 43,76 gam sodium hydroxide.
.
- Khối lượng NaCl đã phản ứng:
- mNaClphn ng=300g−220g=80g𝑚𝑁𝑎𝐶𝑙phnng=300g−220g=80g.
- Số mol NaCl phản ứng:
- nNaCl=8058.5≈1.3675mol𝑛𝑁𝑎𝐶𝑙=8058.5≈1.3675mol.
- Số mol NaOH lý thuyết (theo phương trình 2NaCl→2NaOH2𝑁𝑎𝐶𝑙→2𝑁𝑎𝑂𝐻):
- nNaOHLT=nNaCl=1.3675mol𝑛𝑁𝑎𝑂𝐻LT=𝑛𝑁𝑎𝐶𝑙=1.3675mol.
- Khối lượng NaOH lý thuyết:
- mNaOHLT=1.3675×40=54.7g𝑚𝑁𝑎𝑂𝐻LT=1.3675×40=54.7g.
- Khối lượng NaOH thực tế (hiệu suất 80%):
- mNaOHTT=54.7×80%=43.76g𝑚𝑁𝑎𝑂𝐻TT=54.7×80%=43.76g.
Làm tròn kết quả, mỗi lít nước muối bão hoà sản xuất được khoảng 43.8−43.943.8−43.9 gam NaOH𝑁𝑎𝑂𝐻.43,76
Tính khối lượng NaCl phản ứng trong 1 lít nước muối bão hòa.Khối lượng NaCl ban đầu trong 1 lít nước muối bão hòa là 300g.Khối lượng NaCl còn lại trong 1 lít nước muối nghèo là 220g.Khối lượng NaCl phản ứng trong 1 lít nước muối bão hòa là 300g - 220g = 80g.
Với mỗi lít nước muối bão hòa ban đầu, có thể sản xuất được khoảng 43,76 gam sodium hydroxide.
Với mỗi lít nước muối bão hòa ban đầu có thể sản xuất được khoảng 43,76 gam sodium hydroxide(NaOH).
nNACL : 80÷50,8=1,3(mol)
Khối lượng naoh lý thuyết dược tạo thành
1,3 × 40=54,7
Khối lượng naoh thực tế được tạo thành
54,7× 0,8= 43,76
*Tính khối lượng NaCl đã phản ứng
- Khối lượng NaCl ban đầu trong 1 lít dung dịch bão hòa là 300g300g.- Khối lượng NaCl còn lại trong 1 lít "nước muối nghèo" là 220g220g.
- Khối lượng NaCl đã phản ứng trong quá trình điện phân là:
64
Số mol của Nal phản ứng là
(300-220):(23+35,5)=160:117mol
Số mol NaOH = số mol NaCl pu=160:117mol
-> khối lượng của NaOH là (160:117)*40*80%=43,76
mNaCl=300-220=80
nNaCl=80:58,5=1,368(mol)
2NaCl+H2O điện phân có màng ngăn 2NaOH +H2+Cl2
nNaOH lý thuyết=nNaCl=1,368(mol)
nNaOH thực tế =1,368x0.8=1,094(mol)
mNaOH thực tế =1,094x40=43,8g
50
Với mỗi lít nước muối bão hòa (300 g/L), lượng NaCI phản ứng là 80 g (300 – 220). Số mol NaCI phản ứng là 80/58, 5 ≈ 1, 3675 mol. Với hiệu suất 80%, số mol NaOH tạo ra là 1, 3675 × 0, 8 × 1 = 1, 094 mol. Khối lượng NaOH là 1, 094 × 40 = 43, 76 gam.
43,776 gam
Lượng NaCl đã tham gia phản ứng trong 1 L dung dịch là:
m_{NaCl\ phản\ ứng} = 300 - 220 = 80\ (g)
Số mol NaCl đã điện phân:
n_{NaCl} = \frac{80}{58,5} \approx 1,37\ (mol)
Phương trình điện phân:
2NaCl + 2H2O -> 2NaOH + H2 + Cl2
Theo phương trình phản ứng, tỉ lệ mol:
n_{NaCl} = n_{NaOH}
Vậy số mol NaOH tạo thành:
n_{NaOH} = 1,37\ (mol)
Khối lượng NaOH theo lí thuyết:
m_{NaOH} = 1,37 \times 40 = 54,8\ (g)
Hiệu suất quá trình là 80%, nên khối lượng NaOH thực tế:
m_{NaOH} = 54,8 \times 0,8 = 43,84\ (g)
Vậy với 1 lít nước muối ban đầu có thể sản xuất được khoảng 43,84 g NaOH.
43,76