Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng thu nhiệt là: phản ứng (1)
Phản ứng tỏa nhiệt là: phản ứng (2)

mai thanh nhàn
Bổ sung nốt phần còn thiếu bạn nhé!
M: MgO và Cu.
PT \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)

Gọi x (%) là % số nguyên tử \(^1H\)
y (%) là % số nguyên tử \(^2H\)
Ta có : \(\left\{{}\begin{matrix}x+y=100\\\overline{A}=\dfrac{1x+2y}{100}=1,008\end{matrix}\right.\)
⇔ \(\left\{{}\begin{matrix}x+y=100\\x+2y=100,8\end{matrix}\right.\)
⇔ \(\left\{{}\begin{matrix}x=99,2\left(\%\right)\\y=0,8\left(\%\right)\end{matrix}\right.\)
\(m_{H_2O}\)= V . D= 1 . 1 = 1 (g)
\(n_{H_2O}\)= \(\dfrac{1}{2.1,008+16}\)= 0,05 (mol)
⇒ \(n_H\)= 0,05 . 2= 0,1 (mol)
\(n^1H\)= \(\dfrac{0,1.99,2}{100}\)= 0,0992 (mol)
Số nguyên tử \(^1H\)= n . 6,023.\(10^{23}\)=0,0992 . 6,023.\(10^{23}\)=5,974.\(10^{22}\)
\(n^2H\)= \(\dfrac{0,1.0,8}{100}\)= 8.\(10^{-4}\)(mol)
Số nguyên tử \(^2H\) = n . 6,023.\(10^{23}\)= 8.\(10^{-4}\). 6,023. \(10^{23}\)=4,8184.\(10^{20}\)

Biến thiên enthalpy chuẩn của phản ứng trên là:
\(\Delta_rH^0_{298}=\) \(2.\Delta_fH^0_{298}\left(CO_2\right)+3.\Delta_fH^0_{298}\left(H_2O\right)-\Delta_fH^0_{298}\left(C_2H_6\right)-\Delta_fH^0_{298}\left(O_2\right)\)
\(=2.\left(-393,50\right)+3\left(-285,84\right)-\left(-84,70\right)=-1559,82\left(kJ\right)\)
ΔfH298=ΣΔ fH298(sp) - ΣΔfH298 (cd) = 2.(-393,5) + 3.(-285,84) - (-84,7) = -1559,82 kJ.

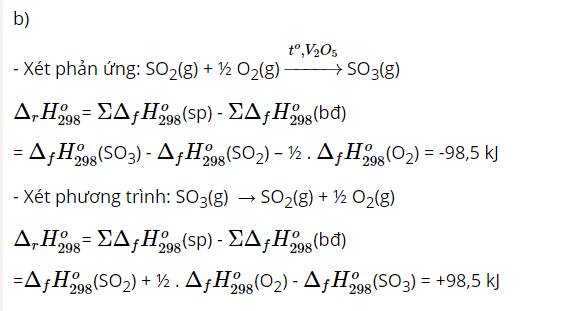
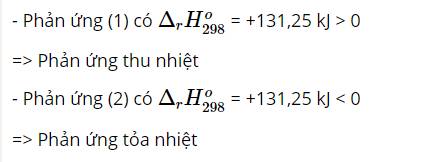
cậu sai rồi Hảo ạ.
Gia đình sẽ dùng hết bình gas trong khoảng 99,5 ngày (hoặc xấp xỉ 100 ngày tùy quy tròn).
100 ngày
Gia đình sẽ dùng hết bình gas sau khoảng 100 ngày (làm tròn số).
Gọi thể tích hỗn hợp là 10 phần Tỉ lệ thể tích (cũng là tỉ lệ mol): Propan: 3 phần Butan: 7 phần Gọi tổng số mol hỗn hợp là
nC3H8=0,3
Bình ga 12kg dùng được khoảng 100 ngày
~100 ngày
Gọi số mol propane và butane lần lượt là 3x và 7x.
Ta có: 3x·44 + 7x·58 = 12000 ⇒ x ≈ 22,3.
Nhiệt lượng tỏa ra:
Q = 66,9·2220 + 156,1·2874 ≈ 5,97·10^5 kJ.
Số ngày dùng gas:
5,97·10^5 / 6000 ≈ 100 ngày.
Tỉ lệ thể tích = tỉ lệ mol:
Propane : Butane = 3 : 7
Gọi tổng số mol khí là 10 mol →
Nhiệt tỏa ra:
Nhiệt của hỗn hợp 10 mol:
Q = 3 \times 2220 + 7 \times 2874
Q = 6660 + 20118 = 26778\ kJ
Khối lượng 10 mol hỗn hợp:
m = 3 \times 44 + 7 \times 58
m = 132 + 406 = 538\ g
→ 538 g khí tạo 26778 kJ
Nhiệt của 12 kg = 12000 g:
Q = \frac{12000}{538} \times 26778
Q \approx 597356\ kJ
Mỗi ngày dùng 6000 kJ
\text{Số ngày} = \frac{597356}{6000} \approx 99.6
✅ Khoảng 100 ngày.