Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng tỏa nhiệt: Sulfuric acid (H2SO4) + Đường, Xăng cháy trong không khí, Củi cháy trong không khí, Phản ứng tạo gỉ sắt, Nến cháy trong không khí …
Phản ứng thu nhiệt: Băng tan, Nước lỏng bay hơi, Luộc trứng, Nấu canh, Nung gốm…

Vì các phản ứng A, B, C điều không toả nhiệt nên phản ứng toả nhiệt là D
Chọn D
Chọn B
Quá trình đóng băng nước là quá trình toả nhiệt vì tạo ra thêm nhiều liên kết mới, vững chắc giữa các phân tử nước là liên kết hydrogen.

2Na(s) + ½ O2(g) → Na2O(s) ${\Delta _f}H_{298}^0 = - 417,98$kJ.mol-1
Na(s) + ¼ O2(g) → ½ Na2O(s) ${\Delta _f}H_{298}^0 = \frac{{ - 417,98}}{2} = 208,99$kJ.mol-1

Đáp án C
1. Sai: cân bằng hóa học là cân bằng động
2. đúng: phản ứng nghịch thu nhiệt, khi tăng nhiệt độ cân bằng sẽ chuyển về phía làm giảm nhiệt độ (thu nhiệt).
3. đúng
4. đúng
5. sai, nồng độ thay đổi không làm thay đổi hằng số cân bằng. Hằng số cân bằng chỉ thay đổi khi thay đổi nhiệt độ.
6. sai: chỉ tính những chất khí hoặc những chất tan trong dung dịch, nếu là chất rắn thì không được tính.
=> Đáp án C

1. sai: cân bằng hóa học là cân bằng động
2. đúng: phản ứng nghịch thu nhiệt, khi tăng nhiệt độ cân bằng sẽ chuyển về phía làm giảm nhiệt độ (thu nhiệt).
3. đúng
4. đúng
5. sai, nồng độ thay đổi không làm thay đổi hằng số cân bằng. Hằng số cân bằng chỉ thay đổi khi thay đổi nhiệt độ.
6. sai: chỉ tính những chất khí hoặc những chất tan trong dung dịch, nếu là chất rắn thì không được tính.
Đáp án C

\(a.E_r=839,0+2\cdot418,4+2\cdot432,0=2539,8kJ\\ b.E_p=343,3+6\cdot418,4=2853,7kJ\\ c.\Delta_rH^{^{ }0}=2539,8-3197=-313,9kJ\cdot mol^{-1}\\ \Delta H< 0:pư.thu.nhiệt\)
\(a.E_{reactants}=839,0+2\cdot432,0=1703kJ\\ b.E_{products}=343,3+6\cdot432,0=2935,3kJ\\ c.\Delta_rH^{^o}_{298}=E_r-E_p=1703-2935,3=1232,3kJ\cdot mol^{^{ }-1}.\)
\(\Delta H< 0\) => Phản ứng (1) thu nhiệt

a.Do \(\Delta H>0\) nên đây là phản ứng thu nhiệt.
-Phản ứng thuận là phản ứng thu nhiệt.
b.
-Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều nghịch.
-Khi tăng nồng độ CO2, cân bằng dịch chuyển theo chiều nghịch.
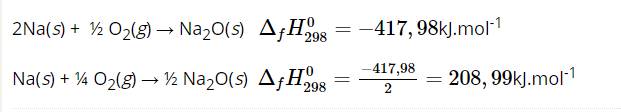
1) Phản ứng tỏa nhiệt:
- Đốt cháy than (C + O2 =(nhiệt độ)=> CO2)
- Đốt cháy cồn (C2H5OH + 3O2 =(nhiệt độ)=> 2CO2 + 3H2O)(
2) Phản ứng thu nhiệt:
- Đá viên tan chảy (MgO + C + Cl2 ==> NgCL2 + CO)
- Muối rắn nóng chảy
6𝐶𝑂2+6𝐻2𝑂+NănglngánhsángDiplc𝐶6𝐻12𝑂6+6𝑂2
- Đốt cháy than (carbon) trong không khí: C(s)+O2(g)→CO2(g)𝐶(𝑠)+𝑂2(𝑔)→𝐶𝑂2(𝑔)
- Đốt cháy khí gas (methane) trong bếp gas: CH4(g)+2O2(g)→CO2(g)+2H2O(l)𝐶𝐻4(𝑔)+2𝑂2(𝑔)→𝐶𝑂2(𝑔)+2𝐻2𝑂(𝑙)
Ví dụ về phản ứng thu nhiệt Phản ứng thu nhiệt là phản ứng hóa học hấp thụ năng lượng dưới dạng nhiệt.Phản ứng tỏa nhiệt (là phản ứng giải phóng năng lượng dưới dạng nhiệt):
Phản ứng thu nhiệt là:hòa tan 1 viên C sủi và sự hòa tan muối Amoni Nitrat
Phản ứng tỏa nhiệt là:đốt cháy khí Metan và phản ứng trung hòa axit mạnh với base mạnh
Phản ứng toả nhiệt: đốt cháy than , phản ứng trung hoà axit-bazơ
phản ứng thu nhiệt : quá trình quang hợp ở cây xanh, hòa tan nước đá
toả nhiệt:
-Đốt gas nấu ăn
-Đốt củi, than
thu nhiệt:
- hoà tan phân đạm vaof nước
- túi chườm lạnh y tế
2 phản ứng toả nhiệt : đốt nhiên liệu , hô hấp
2 phản ứng thu nhiệt : Quang hợp , hòa tan muối
phản ứng tỏa nhiệt (giải phóng nhiệt): Đốt cháy than: C + O₂ → CO₂ (tỏa nhiệt) Phản ứng giữa axit và bazơ (trung hòa): HCl + NaOH → NaCl + H₂O (tỏa nhiệt) phản ứng thu nhiệt (hấp thụ nhiệt): Nhiệt phân đá vôi: CaCO₃ → CaO + CO₂ (thu nhiệt) Phản ứng quang hợp của cây xanh: 6CO₂ + 6H₂O → C₆H₁₂O₆ + 6O₂ (thu năng lượng ánh sáng)
Phản ứng tỏa nhiệt:
C + O₂ → CO₂ (toả nhiệt).
HCl + NaOH → NaCl + H₂O (toả nhiệt).
Phản ứng thu nhiệt:
CaCO₃ → CaO + CO₂ (thu nhiệt).
6CO₂ + 6H₂O → C₆H₁₂O₆ + 6O₂ (thu năng lượng ánh sáng).
1 phản ứng cháy của than
C(s) + O2 (gì) \(-\) CO2 (g)
2 phản ứng nhiệt phân đá vôi
CaCO3 (s) \(-\) CaO (s) + CO2 (g)
Phản ứng toả nhiệt:
đốt cháy than,phản ứng giữa axit và bazơ
Phản ứng thu nhiệt:
Nhiệt phân đá vôi,Quang hợp của cây xanh
Phản ứng toả nhiệt :
Ví dụ 1: đốt cháy than
Ví dụ 2: hàn nhiệt nhôm
Phản ứng thu nhiệt :
Ví dụ 1: nung đá vôi
Ví dụ 2 : hoà tan muối amoni nitra
CH4 + 2O2 - CO2 +2H2O + nhiệt
CAO+ H2O - CA+(OH )2 + nhiệt
Ví dụ phản ứng tỏa nhiệt:
Ví dụ phản ứng thu nhiệt:
ví dụ về phản ứng toả nhiệt là đốt củi và đốt than
ví dụ của phản ứng thu nhiệt là đá viên tan chảy dưới nhiệt độ phòng hay phản ứng nung đá vôi
vi du ve phản ứng toả nhiệt là: đốt chay than củi, đốt lửa sưởi ấm,..
ví dụ về phản ứng thu nhiệt: Cho viên đá vào cốc nước , nung vôi, băng tan,...
-Phản ứng tỏa nhiệt: đốt than, củi cháy; phản ứng của axit với kim loại hoặc gỉ sét
-Phản ứng thu nhiệt: đá tan; pha viên sủi vào nước
1
-Phản ứng tỏa nhiệt:
+ Đốt than
+ Đốt giấy
-Phản ứng thu nhiệt:
+Máy sấy tóc
+Nung vôi
ví dụ về phản ứng toả nhiêt: đốt cháy than củi, đốt lửa sưởi ấm,..
ví dụ vè phản ứng thu nhiet: cho viên đá vào cốc nước ấm, băng tan,..
phản ứng toả nhiệt :
- đốt cháy than
- đốt rác
Phản ứng thu nhiệt :
- sự phân huỷ đá vôi
- nước lỏng bay hơi thành hơi nước
Phản ứng toả nhiệt:
+ đốt cháy than
+ đốt rác
Phản ứng thu nhiệt
+ sự phân huỷ đá vôi
+ nước lọc bay hơi thành hơi nước
Phản ứng thu nhiệt
CaCO3 - - ->CaO+CO2
6CO2+6H2O - - ->C6H12O6+6O2
Phản ứng tỏa nhiệt
C+O2- - ->CO2
CaO+H2O→Ca(OH)2
vd phản ứng toả nhiệt:
Phản ứng đốt cháy nhiên liệu tạo ra lượng lớn , làm nóng môi trường xung quanh .
phản ứng giữa:NaOH và HCL,toả nhiệt làm cốc phản ứng nóng lên
Vd phản ứng thu nhiệt
Nung đá vôi (caco3)ở nhiệt độ cao để tạo thành đá vôi sống (cao)và co2
Phản ứng tỏa nhiệt (tỏa năng lượng ra môi trường): Phản ứng đốt cháy than, củi hoặc xăng dầu. Phản ứng giữa axit và bazơ (phản ứng trung hòa). Phản ứng thu nhiệt (hấp thụ năng lượng từ môi trường): Phản ứng phân hủy đá vôi ( ) ở nhiệt độ cao. Phản ứng quang hợp của cây xanh.
Phản ứng đốt cháy than: Khi đốt than, năng lượng được giải phóng dưới dạng nhiệt và ánh sáng.
Phản ứng giữa axit và bazơ (Phản ứng trung hòa): Ví dụ, phản ứng giữa axit clohydric và natri hydroxit giải phóng nhiệt.
Phản ứng nung vôi: Cần cung cấp nhiệt lượng cao để phân hủy đá vôi thành vôi sống.
Phản ứng quang hợp: Cây xanh hấp thụ năng lượng ánh sáng mặt trời để chuyển hóa carbon dioxide và nước thành glucose và oxygen.
Tỏa nhiệt : đốt lửa,phản ứng ri sắt
Thu nhiệt: Nung đá vôi,hòa tan muối ăn