Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) ΔrHo298 = 24,7 kJ > 0 => Phản ứng thu nhiệt.
Vì vậy, khi xịt thuốc vào chỗ đau thì người ta cảm giác lạnh.
b) CH3CH3 + Cl2 → CH3CH2Cl + HCl

nHNO3 =0 ,3
NaNO3 => HNO3
0,3 <= 0,3
=> mNaNO3 = 0,3.85 = 25,5
mà chứa 25% tạp chất trơ => m NaNO3 cần = 25,5: 15% = 170 (g)

\({{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}\frac{{\rm{6}}}{{{\rm{60}}}}{\rm{ = 0,1 (mol); }}{{\rm{n}}_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}}}{\rm{ = }}\frac{{{\rm{5,2}}}}{{46}}{\rm{ }} \approx {\rm{ 0,113 (mol)}}\)
Phương trình hóa học:
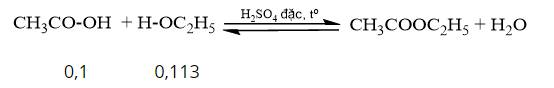
Ta có: \(\frac{{0,1}}{1} < \frac{{0,113}}{1}\) => acetic acid hết, ester tính theo acetic acid.
\(\begin{array}{l}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}}{\rm{ = }}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = 0,1 (mol) }}\\ \Rightarrow {{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}} = {\rm{0,1}} \times {\rm{88 = 8,8 (g)}}\\ \Rightarrow {\rm{H = }}\frac{{5,28}}{{8,8}} \times 100\% = 60\% \end{array}\)
- Phương trình phản ứng:
\(C H_{3} C O O H + C_{2} H_{5} O H \overset{H_{2} S O_{4}}{\rightarrow} C H_{3} C O O C_{2} H_{5} + H_{2} O\) - Số mol acetic acid: \(0 , 1\) mol
- Số mol ethanol: \(0 , 113\) mol
- Chất giới hạn: acetic acid (0,1 mol)
- Khối lượng ester lý thuyết: \(0 , 1 \times 88 = 8 , 8\) g
- Khối lượng ester thực tế: 5,28 g
- Hiệu suất:
\(\frac{5 , 28}{8 , 8} \times 100 \% = 60 \%\)
Kết quả: Hiệu suất = 60%.

Trong thí nghiệm điều chế ethyl acetate, không đun sôi hỗn hợp phản ứng vì nhiệt độ sôi của ethyl acetate thấp (77,1 oC), ethyl acetate sẽ bị bay hơi khi đun sôi hỗn hợp phản ứng.
Dung dịch sodium chloride bão hoà nặng hơn ethyl acetate, ethyl acetate nổi lên trên, do đó việc tách ester ra khỏi hỗn hợp sau phản ứng dễ hơn.

Để điều chế 25.8 gam ethyl chloride với hiệu suất 80%, cần sử dụng 11.2 lít khí ethylene (ở đkc).
cần sử dụng 12,395 lít khí ethylene
12,395
12,398
12,395 lít
C2H4 + HCl -> C2H5Cl
Khối lượng mol của C2H5Cl: M = 12*2 + 5 + 35,5 = 64,5 (g/mol)
Số mol C2H5Cl thu được theo thực tế: n tt = 25,8 / 64,5 = 0,4 (mol)
Số mol C2H4 cần dùng (nếu hiệu suất 100%): n lt = 0,4 (mol)
Số mol C2H4 thực tế cần dùng: n cần = 0,4 / 80% = 0,5 (mol)
Thể tích khí C2H4 ( đkc, 25°C, 1 bar): V = n * 24,79 = 0,5 * 24,79 = 12,395 (lít)
Để điều chế được 25,8 gam ethyl chloride với hiệu suất 80% thì cần dùng 12,395 lít khí ethylene
Cần sử dụng 12,395 lít khí ethylene (đkc) để điều chế lượng ethyl chloride trên với hiệu suất 80%.
35%