Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(1\le\dfrac{N}{Z}\le1,5\)
\(\Rightarrow Z\le N\le1,5Z\)
\(\Rightarrow3Z\le2Z+N\le3,5Z\)
Vậy ta có : \(3Z\le24\le3,5Z\)
=> \(6,86\le Z\le8\)
=>\(\left[{}\begin{matrix}Z=7\left(N\right)\\Z=8\left(O\right)\end{matrix}\right.\Rightarrow\left[{}\begin{matrix}N=10\\N=8\end{matrix}\right.\)
Mà theo đề bài : \(1\le\dfrac{N}{Z}\le1,5\)
=> Chỉ có O thỏa mãn
=> Z là O , số P= số E =8 , N=8
b) Cấu hình E: 1s22s22p4

X : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6
Số thứ tự bằng số proton và bằng số electron Z = 2 + 2 + 6 + 2 + 6= 18.

Nguyên tử X có 3 lớp electron, lớp ngoài cùng có 6 electron, vậy có cấu hình electron : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 4
Số thứ tự bằng số proton và bằng số electron : Z = 16.
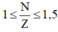
a) Ta có: p = e; p = 13
=> p = e = 13
- Cấu hình electron trong nguyên tử của nguyên tố Aluminium (Al) là:
+) Lớp thứ nhất: 2 electron
+) Lớp thứ hai: 8 electron
+) Lớp thứ ba: 3 3lectron
b) Vị trí của nguyên tố Aluminium trong bảng tuần hoàn các nguyên tố hóa học:
- Ô: 13
- Chu kì: 3
- Nhóm: IIIA
b)
Chu kì 3, nhóm IIIAb, Chu kỳ 3, nhóm IIIA.
a, 1s22s22p63s23p1
a)[Ne]3s23p1
b)
13e=>ô13
3 lớp e=>chu kì 3
3e lớp ngoài=>nhóm IIIA
a) Cấu hình electron của nguyên tử aluminium là: 1s² 2s² 2p⁶ 3s² 3p¹ b) Aluminium nằm ở chu kỳ 3, nhóm IIIA (hoặc nhóm 13) trong bảng tuần hoàn các nguyên tố hóa học.
1s2 2s2 2p6 3s2 3p1
a. 1s22s22p63s23p1
b. chu kì 3 nhóm IIIA
a) [Ne] 3s2 3p1
b)
Đáp án: Câu 1: B Câu 2: C Câu 3: B Câu 4: C Câu 5: B Câu 6: C Câu 7: C Câu 8: B Câu 9: C Câu 10:
a. 1𝑠22𝑠22𝑝63𝑠23𝑝1
b.
Cấu hình electron đầy đủ của nguyên tử Aluminium (Al) là:
1s^{2}2s^{2}2p^{6}3s^{2}3p^{1}
Chu kì 3
Nhóm 3A
a,Cấu hình của nguyên tử là: 1s¹2s²2p⁶3s²3p⁶
b, ô số 13, chu kỳ 3, nhóm 13
1s²2s²2p⁶3s²3p¹
nằm ở ô thứ 13 chu kì 3 nhóm IIIA
5373
a,
-cấu hình electron của nguyên tử Al là :
1s²2s²2p⁶3s²3p
b,
- vị trí của nguyên tố được sắp xếp trong bảng tuần hoàn như sau:
+chu kỳ 3
+nhóm IIIA
Cấu hình electron là:
a): 1s22s22p63s23p1 b): ô số 13 chu kì 3 nhóm 13, 1s22s22p63s23p1 vì có 3 electron ở lớp ngoài cùng
a,
1s²2s²2p⁶3s²3p¹(2-8-3)
b,
Chu kì 3, nhóm lllA ( nhóm 13 ) trong bảng tuần hoàn
Hzjs