
Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)

\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{64.50}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2

Công thức hóa học: S x O y
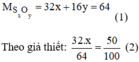
Giải phương trình (2) ta được: x = 1 thay vào pt (1) ⇒ y = 2.
Vậy công thức hóa học của oxit là S O 2

Câu 1 :
\(M_{K_2CO_3}=39.2+12+16.3=138\left(dvC\right)\)
\(\%K=\dfrac{39.2}{138}.100\%=56,52\%\)
\(\%C=\dfrac{12}{138}.100\%=8,69\%\)
\(\%O=100\%-56,52\%-8,69\%=34,79\%\)
Còn lại cậu làm tương tự nhá

Gọi \(x;y\) lần lượt là hóa trị của \(S;O\)
\(\dfrac{m_S}{m_O}=\dfrac{2}{3}\\ \Leftrightarrow\dfrac{32x}{16y}=\dfrac{2}{3}\\ \Leftrightarrow96x=32y\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{32}{96}=\dfrac{1}{3}\)
\(\Rightarrow x=1;y=3\)
\(\Rightarrow ChọnA\)

Khối lượng của các nguyên tố trong hợp chất là:
\(m_{FE}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=\dfrac{30.160}{100}=48\left(g\right)\)
Số mol có trong mỗi nguyên tố là:
\(n_{FE}=\dfrac{m_{FE}}{M_{FE}}=\dfrac{112}{56}=2\left(mol\right)\)
\(n_O=\dfrac{m_O}{M_O}=\dfrac{48}{16}=3\left(mol\right)\)
Vậy hợp chất có 2 nguyên tử Fe, 3 nguyên tử O
Công thức hóa học của hợp chất là: \(FE_2O_3\)

Bài 2:
Đặt công thức oxit của phopho là PxOy
Ta có: Phân tử khối của oxit là 142 đvC nên: 30x + 16y = 142 (1)
Thành phần phần trăm của Phopho là 43,66 % ta có:
\(\dfrac{30x}{30x+16y}.100=43,66\)
\(\Rightarrow1690,2x-698,56y=0\left(2\right)\)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{{}\begin{matrix}30x+16y=142\\1690,2x-698,56y=0\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=2\\y=5\end{matrix}\right.\)
Vậy oxit đó là P2O5

Phân tử khối của Đồng ôxit và Đồng sunfat có tỉ lệ 1/2
Mà phân tử khối của đồng sunfat (CUSO4) là 160 đvC
=> Phân tử khối của đồng oxit là :
160 * 1/2 = 80 (đvC)
Do đồng oxit gồm Cu và O nêncông thức hóa học của đồng oxit có dạng CuxOy
Ta có :
PTKđồng oxit = NTKCu * x + NTKO * y
=> 80 đvC = 64 * x + 16 * y
=> x < 2 vì nếu x = 2 thì 64 * 2 > 80
=> x = 1 , khi đó :
y = ( 80 - 64*1 ) : 16 = 1
Vậy công thức hóa học của đồng oxit là CuO
b) Gọi công thức của oxit là SxOy
x : y = nS : nO =
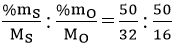
= 1,5625 : 3,125 = 1 : 2
Vậy công thức đơn giản của hợp chất M là: SO2
Ta có:
\(m_S=64.50\%=32g\)
\(m_O=64.50\%=32g\)
=> \(n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(n_O=\dfrac{32}{16}=2\left(mol\right)\)
Vậy CTHH của oxit đó là \(SO_2\)
SO2��2
Giải thích các bước giải:
Hợp chất tạo bởi S;O�;� nên có dạng SxOy����
→MSxOy=xMS+yMO=32x+16y=64→�����=���+���=32�+16�=64
→%mS=32x64=50%→x=1→y=2→%��=32x64=50%→�=1→�=2
Vậy hợp chất là SO2S
O2��2
Giải thích các bước giải:
Hợp chất tạo bởi S;O�;� nên có dạng SxOy
Đúng(0)
Gọi công thức hoá học của oxit lưu huỳnh cần tìm là SxOy.
Theo đề bài ta có:
+ SxOy có phân tử khối là 64 g/mol nên 32×�+16×�=64⇒16×�=64−32×�32×x+16×y=64⇒16×y=64−32×x
+ Phần trăm của lưu huỳnh trong oxit SxOy này là 50%
⇒%��=32×�32×�+16×�×100%=50%⇒%mS=32×x+16×y32×x×100%=50%
mà 16×�=64−32×�16×y=64−32×x thay vào biểu thức tính %mS ta tính được x = 1, y = 2.
Vậy công thức hoá học của oxit lưu huỳnh cần tìm là SO2.
Gọi công thức hoá học của oxit lưu huỳnh cần tìm là SxOy.
Theo đề bài ta có:
+ SxOy có phân tử khối là 64 g/mol nên 32×�+16×�=64⇒16×�=64−32×�32×x+16×y=64⇒16×y=64−32×x
+ Phần trăm của lưu huỳnh trong oxit SxOy này là 50%
⇒%mS=32×x+16×y32×x×100%=50%
mà 16×�=64−32×�16×y=64−32×x thay vào biểu thức tính %mS ta tính được x = 1, y = 2.
Vậy công thức hoá học của oxit lưu huỳnh cần tìm là SO2.
SO2��2
Giải thích các bước giải:
Hợp chất tạo bởi S;O�;� nên có dạng SxOy����
→MSxOy=xMS+yMO=32x+16y=64→�����=���+���=32�+16�=64
→%mS=32x64=50%→x=1→y=2→%��=32x64=50%→�=1→�=2
Vậy hợp chất là SO2
Gọi công thức hoá học của oxit lưu huỳnh cần tìm là SxOy.
Theo đề bài ta có:
+ SxOy có phân tử khối là 64 g/mol nên 32×�+16×�=64⇒16×�=64−32×�32×x+16×y=64⇒16×y=64−32×x
+ Phần trăm của lưu huỳnh trong oxit SxOy này là 50%
=> %mS= \(\dfrac{32\times x}{32\times x+16\times x}\times100\%=50\%\)
mà 16×�=64−32×�16×y=64−32×x thay vào biểu thức tính %mS ta tính được x = 1; y = 2
Vậy công thức hoá học của oxit lưu huỳnh cần tìm là SO2.
Công thức hóa học: SxOy
���
M
SxSxOy = 32x + 16y = 64 (1)
Theo bài ra ta có: 32x/64 = 50/100 (2)
giải phương trình (2) ta được: x = 1 thay vào phương trình (1) => y = 2
Giải phương trình (2) ta được: x = 1 thay vào pt 1) ⇒ y = 2.Vậy công thức hóa học của oxit là SO2
Ta có: {mS=64⋅50%=32(g)mO=64⋅50%=32(g)⇒⎧⎪ ⎪⎨⎪ ⎪⎩nS=3232=1(mol)nO=3216=2(mol){��=64⋅50%=32(�)��=64⋅50%=32(�)⇒{��=3232=1(���)��=3216=2(���)
Vậy CTHH là SO2