Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

HD:
CT oxit cao nhất của R với oxi là R2O5 (suy ra từ RH3).
Ta có: 80/(2R+80) = 0,5634 suy ra: R = 14 (N).
H:N:H H cấu tạo: H-N-H H
Hóa trị cao nhất vs khí H là 3
>> hóa trị cao nhất vs O là 8_3=5
>>hợp chất vs oxit cao nhất là R2O5
Có %mO=56.34%
Xét tỉ số MO/Mo+MR =%mo
Hay80/80+2×MR=0.5634
>>MR=14(N)
>>hợp chất vs oxit cao nhất là N2O5
b) hợp chất vs H là NH3

\(n_{CO_2}=\frac{V_{CO_2}}{22,4}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
-> \(n_{\left(C\right)}=0,1\left(mol\right)\)
-> \(n_{hh}=0,1\left(mol\right)\)

1. a) K hóa trị I
b) Mg hóa trị II
c) Cr hóa trị III
d) C hóa trị IV
2. a) Ba hóa trị II
b) Fe hóa trị III
c) Cu hóa trị II
d) Li hóa trị I
3. a) Gọi công thức là SiHn trong đó n là hóa trị Si
Vì KL riêng Si=28 nên n=28:87.5%-28=4
Vậy công thức là SiH4 , PTK=32
b) Si hóa trị IV
4. a) Gọi công thức là Fe2On trong đó n là hóa trị Fe.
Theo đề bài, n=56*2/7*3/16=3
Vậy công thức là Fe2O3 , PTK=160
b) Hóa trị của Fe là III.

Đề Nguyễn Gia Thiều năm 2017 - 2018
CT là H2O2
3) H2O2 + Ba(OH)2 ⇌ BaO2 + 2H2O
PUHH trên chứng tỏ H2O2 có tính oxi hóa ...
a. Công thức Lewis của CO2: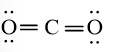
Công thức cấu tạo của CO2 là: O = C = O.
Công thức Lewis của NH3 là: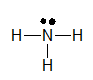
Công thức cấu tạo của NH3 là: \(H-N-H\)
\(|\)
H
b. Hợp chất tan trong nước: CO2 và NH3
Trong CO2CO2 chứa hai liên kết cộng hóa trị phân cực C=OC=O (đều phân cực về phía OO). Tuy nhiên, CO2CO2 có cấu trúc phân tử thẳng (O=C=OO=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử
- Carbon dioxide (CO 22):
- Công thức Lewis: Nguyên tử C có 4 electron hóa trị, O có 6. C liên kết với O bằng hai liên kết đôi.
- Công thức cấu tạo:
- Ammonia (NH 33):
- Công thức Lewis: Nguyên tử N có 5 electron hóa trị, H có 1. N liên kết với 3 nguyên tử H bằng 3 liên kết đơn và còn một cặp electron không liên kết trên N.
- Công thức cấu tạo:
b) Độ tan trong nước và giải thích∶O..∶∶C∶∶O..∶∶𝑂..∶∶𝐂∶∶𝑂..∶
O=C=O𝐎=𝐂=𝐎
N̈∶HHH𝑁̈∶𝐻𝐻H
H|H−N−HH|H−N−H
a) CO2
NH3
b)NH3 tan trong nước do NH3 tạo liên kết hydrogen với nước , còn CO2 không tan trong nước do CO2 không tạo liên kết hydrogen với H20
a) Công thức Lewis và công thức cấu tạo
1. CO (cacbon monoxit)
Tổng số e hoá trị:
C: 4e
O: 6e
→ Tổng: 10e
Công thức Lewis:
C và O liên kết với nhau bằng liên kết ba
Mỗi nguyên tử còn 1 cặp e không liên kết
Biểu diễn:
:C≡O:
Công thức cấu tạo:
C \equiv O
---
2. NH₃ (amoniac)
Tổng số e hoá trị:
N: 5e
3H: 3e
→ Tổng: 8e
Công thức Lewis:
N liên kết với 3 H bằng 3 liên kết đơn
N còn 1 cặp e không liên kết
Biểu diễn:
H
|
H–N:
|
H
Công thức cấu tạo:
\begin{matrix}
& H \\
H &–& N &–& H \\
&
\end{matrix}
---
b) Tính tan trong nước
NH₃ tan trong nước
Phân tử phân cực
Có khả năng tạo liên kết hiđro với H₂O
Khi tan, NH₃ còn phản ứng với nước:
NH_3 + H_2O \rightleftharpoons NH_4^+ + OH^-
👉 NH₃ tan tốt trong nước
---
CO không tan trong nước
Phân tử gần như không phân cực
Không tạo được liên kết hiđro với nước
Không phản ứng với H₂O
👉 CO hầu như không tan trong nước
---
✅ Kết luận:
NH₃ tan trong nước
CO không tan trong nước
Hợp chất tan trong nước: CO2 và NH3
Trong CO2CO2 chứa hai liên kết cộng hóa trị phân cực C=OC=O (đều phân cực về phía OO). Tuy nhiên, CO2CO2 có cấu trúc phân tử thẳng (O=C=OO=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử
Đáp án: Câu 1: B Câu 2: C Câu 3: B Câu 4: C Câu 5: B Câu 6: C Câu 7: C Câu 8: B Câu 9: C Câu 10:
Công thức:O:=C=:O:
Công thức cấu tạo O=C=O
Công thức.H-N:-H
Cấu tạo.H-N-H
B) NH3 tan nhiều
O::C::O
H-N-H-H
Nh3 tan con co2 it tan
a.CO2 C=O=C
NH3. H:N::H:H
b. NH3 tan trong nước. Vì NH3 phân cực và tạo nên hydrogen với nước.
CO2 ko tan trong nước . Vì CO2 ko phân cực nên khó hòa tan .
a,
CO2 :
Công thức Lewis : *O*=C=*O *
Công thức cấu tạo : O=C=O
NH3 : Công thức cấu tạo : N( -H)³
b. NH3 tan tốt trong nước , còn CO2 tan ít hơn . Vì NH3( tan rất tốt ) vì là phân tử không phân cực và có khả năng tạo liên kết hydrogen với nước . Còn CO2 là phân tử không phán cực , khó tương tác với các phân tử nước phân cực
công thức cấu tạo :
CO2 : C =O = C
NH3 : H-N-H-H
b
𝑁𝐻3có cấu trúc hinh chóp tam giác , tan rất nhiều trong nước
CO2 phân tử không phân cực vì nước là dung môi phân mạnh