Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy tắc octet: Khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm.
Ví dụ:
- Phân tử O2
Khi hình thành liên kết hoá học trong phân tử O2, nguyên tử oxygen có 6 electron hoá trị, mỗi nguyên tử oxygen cần thêm 2 electron để đạt cấu hình electron bão hoà theo quy tắc octet nên mỗi nguyên tử oxygen góp chung 2 electron.
Phân tử O2 được biểu diễn như sau:



Xung quanh mỗi nguyên tử fluorine đều có 8 electron
- Khi hình thành liên kết hóa học trong phân tử CCl4, nguyên tử carbon có 4 electron hóa trị, nguyên tử carbon cần thêm 4 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử chlorine góp chung một 1 electron. Phân tử CCl4 được biểu diễn

Xung quanh mỗi nguyên tử carbon và chlorine đều có 8 electron
- Khi hình thành liên kết hóa học trong phân tử NF3, nguyên tử nitrogen có 5 electron hóa trị, nguyên tử nitrogen cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử fluorine góp chung một 1 electron. Phân tử NF3 được biểu diễn
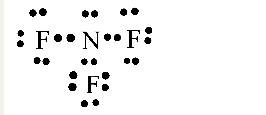
Xung quanh mỗi nguyên tử nitrogen và florine đều có 8 electron

- Khi hình thành liên kết hóa học trong phân tử PH3, nguyên tử phosphorus có 5 electron hóa trị, nguyên tử phosphorus cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử hydrogen góp chung một 1 electron. Phân tử PH3 được biểu diễn
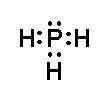
Xung quanh mỗi nguyên tử phosphorus đều có 8 electron.

tham khảo
- Nguyên tử O (Z = 8): 1s22s22p4 ⇒ Có 6 electron lớp ngoài cùng ⇒ Có xu hướng nhận 2 electron để đạt được cấu hình electron giống khí hiếm.
- Nguyên tử H (Z = 1): 1s1 ⇒ Có xu hướng nhận 1 electron để đạt được cấu hình electron giống khí hiếm.
⇒ Mỗi nguyên tử H sẽ góp chung 1 electron với nguyên tử O (góp chung 2 electron) tạo thành 2 cặp electron dùng chung
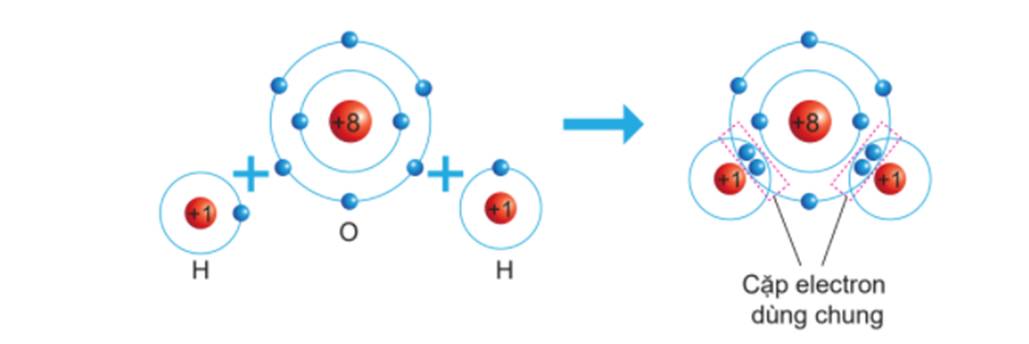

- Phân tử H2O được hình thành bởi 2 ion H+ và 1 ion O2-
- Nguyên tử nguyên tố hydrogen cho đi 1 electron tạo thành H+ để đạt cấu hình electron bền vững của khí hiếm
- Nguyên tử nguyên tố oxygen nhận 2 electron tạo thành O2- để đạt cấu hình electron bền vững của khí hiếm Ne

HD:
Độ âm điện của các nguyên tố như sau: H(2,2); F(3,98); Na(0,93); O(3,44).
HF: Hiệu độ âm điện giữa F và H = 3,98 - 2,2 = 1,78 > 1,7 nên liên kết H-F là liên kết ion.
Na2O: Hiệu độ âm điện giữa O và Na = 3,44 - 0,93 = 2,95 > 1,7 nên liên kết O-Na là liên kết ion.
NaOH: Hiệu độ âm điện O-H = 3,44 - 2,2 = 1,24 < 1,7 nên liên kết O-H là liên kết cộng hóa trị phân cực.
NaF: Hiệu độ âm điện = 3,98 - 0,93 = 3,05 > 1,7 nên liên kết Na-F là liên kết ion.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
\(P\left(z=15\right):1s^22s^22p^63s^23p^3\) . P có 5 electron hoá trị cần thêm 3 elctron để đạt octet
\(H\left(z=1\right):1s^1\) . H có 1 electron hoá trị cần thêm 1 electron để đạt octet
\(P\left(z=15\right):1s^22s^22p^63s^23p^3\) . P có 5 electron hoá trị cần thêm 3 electron để đạt octet
\(H\left(z=1\right):1s^1\). H có 1 electron hoá trị cần thêm 1 electron để đạt octet . Khi hình thành liên kết , P góp chung 3 electron với 3 electron của 3H => trong PH3 , xung quanh P có 8 electron giống khí hiếm Ar còn 3H đều có 2 electron giống khí hiếm He
- P (Z = 15): 1s22s22p63s23p3 ⇒ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
- H (Z = 1): 1s1 ⇒ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
- Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
P góp chung 3 electron với 3 electron của 3 H
-> Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 ⇒ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 ⇒ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
P nhận 3e và trở thành ion P3-
H3 cho 1e để trở thành cấu hình khí hiếm gần nó là He nên có ion H1+,
Từ đó hai ion trái dấu hút nhau
Sự tạo thành liên kết hóa học trong phân tử phosphine (
PH3PH3) được giải thích dựa trên sự góp chung electron giữa một nguyên tử Phosphorus và ba nguyên tử Hydrogen, hình thành ba liên kết cộng hóa trị
P−HP−H. Mỗi nguyên tử H đạt cấu hình 2 electron bền vững, và nguyên tử P đạt cấu hình 8 electron ở lớp vỏ ngoài cùng (octet) nhờ 3 cặp electron liên kết và 1 cặp electron không liên kết.
Để giải thích sự tạo thành liên kết hóa học trong phân tử phosphine (PH3) bằng quy tắc octet, ta cần xem xét cấu hình electron của các nguyên tử phosphorus (P) và hydrogen (H).
Xác định cấu hình electron của P và H.Phosphorus (P, Z=15): Cấu hình electron là 1s² 2s² 2p⁶ 3s² 3p³. Lớp ngoài cùng có 5 electron (3s² 3p³).Hydrogen (H, Z=1): Cấu hình electron là 1s¹. Lớp ngoài cùng có 1 electron.
Áp dụng quy tắc octet.Phosphorus cần thêm 3 electron để đạt được cấu hình octet (8 electron ở lớp ngoài cùng).Hydrogen cần thêm 1 electron để đạt được cấu hình bền vững (2 electron, giống helium).
Hình thành liên kết cộng hóa trị.Mỗi nguyên tử hydrogen góp 1 electron, và nguyên tử phosphorus góp 1 electron để tạo thành một liên kết cộng hóa trị.Vì có 3 nguyên tử hydrogen, phosphorus sẽ tạo 3 liên kết cộng hóa trị với 3 nguyên tử hydrogen.Sau khi tạo 3 liên kết, phosphorus có 3 electron từ 3 nguyên tử hydrogen và 5 electron ban đầu, tổng cộng là 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.Mỗi nguyên tử hydrogen có 2 electron (1 từ chính nó và 1 từ phosphorus), đạt cấu hình bền vững.
- (Z = 15): Cấu hình electron là [Ne]3s23p3[𝑁𝑒]3𝑠23𝑝3. Nguyên tử P có 5 electron ở lớp vỏ ngoài cùng. Để đạt cấu hình bền vững của khí hiếm gần nhất (Ar, 8 electron), P cần thêm 3 electron.
- H (Z = 1): Cấu hình electron là 1s11𝑠1. Nguyên tử H có 1 electron ở lớp vỏ ngoài cùng. Để đạt cấu hình bền vững của khí hiếm gần nhất (He, 2 electron - cấu hình duet), H cần thêm 1 electron.
Trong phân tử PH\textsubscript{3}, nguyên tử photpho (P) liên kết với ba nguyên tử hiđro (H):- Mỗi nguyên tử P góp 3 electron.
- Mỗi nguyên tử H góp 1 electron.
- Tổng cộng có 3 cặp electron dùng chung, tạo thành ba liên kết cộng hóa trị đơn (P-H).
- Lúc này, xung quanh nguyên tử P có 5+3=85+3=8 electron (đạt cấu hình octet) và xung quanh mỗi nguyên tử H có 1+1=21+1=2 electron (đạt cấu hình duet).
Sự hình thành liên kết trong PH\textsubscript{3} tuân theo quy tắc octet.- Nguyên tử P góp chung 3 electron với 3 nguyên tử H, đồng thời nhận về 3 electron từ H, tổng cộng P có 8 electron hóa trị (5 ban đầu + 3 góp chung).
- Mỗi nguyên tử H góp chung 1 electron với P, đồng thời nhận về 1 electron từ P, tổng cộng H có 2 electron hóa trị (1 ban đầu + 1 góp chung).
Kết quả là hình thành ba liên kết cộng hóa trị P-H trong phân tử PH3, đảm bảo quy tắc octet cho P và quy tắc duet (2 electron) cho H.Nguyên tử P và H góp chung electron để đạt cấu hình bền vững của khí hiếm
Sự hình thành liên kết trong phân tử PH
33tuân theo quy tắc octet. Nguyên tử P góp chung 3 electron với 3 nguyên tử H để tạo thành 3 liên kết cộng hóa trị đơn, giúp cả P và H đều đạt được cấu hình electron bền vững của khí hiếm.
Nguyên tử P : [Ne] 3s2 3p3 với 5 e hoá trị
Để đạt cấu hình bền vững khí Ar , P cần nhận thêm 3e
Voiws H ,để đạt cấu hình bền vững He,H cần nhận thêm 1e
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
H • • P • • H
:
H
PH3
Z=5