Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo Bảng 4.2 lithium có 1 electron ở lớp ngoài cùng
=> Lithium là nguyên tố kim loại

Theo đề bài, ta có:
n + p + e = 34 (1)
n + 10 = p + e (2)
số p = số e (3)
Thay (2) vào (1), ta có:
(1) => n + n + 10 = 34
2n = 34 - 10
2n = 24
n = 24 : 2
n = 12 (4)
Thay (4) và (3) vào (2), ta có:
(2) => p + p = 12 + 10
2p = 22
p = 22 : 2
p = 11
=> Nguyên tử R có số p = 11 là Natri - Na là nguyên tố kim loại có NTK = 23 đvC

ta co p+e+n=93 mà p=e=z => 2z+n=93
2z-n=23 ( vì số hạt mang điện nhiều hơn số hạt ko mang điện là 23)
tu 2 pt trên ta có z =29,,n=35
=> số hiệu nguyên tử của B = Z = 29
cấu hình electron
\(1s^22s^22p^63s^23p^64s^23d^9\)
đối với các dạng bài này , bạn cần nhớ kiến thức như sau :
Tổng số hạt trong nguyên tử = 2p + n ( gồm có 3 loại hạt : n , p, e trong đó p=e)
số hạt mang điện là 2p
số hạt không mang điện là n
số hiệu nguyên tử là Z= p = e = số thứ tự nhóm .
Sau khi xác định được p ,, tức là cũng xác định được e thì
cấu hình viết theo dãy trật tự các mức năng lượng
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10.......
Các nguyên tử có 1, 2, 3e ở lớp ngoài cùng là các nguyên tử kim loại, trừ H, He và B.Các nguyên tử có 5, 6, 7e ở lớp ngoài cùng thường là các nguyên tố phi kim. Các nguyên tử có 4e ở lớp ngoài cùng có thể là nguyên tử kim loại hoặc phi kim

a) Có \(\left\{{}\begin{matrix}p+n+e=2p+n=60\\p=n\end{matrix}\right.=>\left\{{}\begin{matrix}p=e=20\\n=20\end{matrix}\right.\)
=> R là Ca
b)
Cấu hình của Ca: 1s22s22p63s23p64s2
Có 20e => Ca nằm ở ô thứ 20
Có 4 lớp e => Ca thuộc chu kì 4
Có 2e lớp ngoài cùng => Ca thuộc nhóm IIA
c)
Nguyên tử Ca nhường 2e để đạt đến cấu hình bền của khí hiếm, tạo ra ion Ca2+
Cấu hình ion Ca2+ : 1s22s22p63s23p6
d) \(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2Ca + O2 --to--> 2CaO
_____0,4<--0,2
=> mCaO = 0,4.40 = 16 (g)

a) nguyên tử khối X= 28 => A=Z+N= 28(1)
số hạt không mang điện(N),nhiều hơn số hạt mang điện dương(Z) là 4 hạt. Ta có:
Z=N suy ra: Z-N=0(2)
Từ (1) và (2) suy ra ta có hệ phương trình:
\(\left\{{}\begin{matrix}Z+N=28\\Z-N=0\end{matrix}\right.\)=>\(\left\{{}\begin{matrix}Z=14\\N=14\end{matrix}\right.\)
Vậy nguyên tố đó là Si
Cấu hình e: 1s22s22p63s23p2

p+e+n=34
p=e
2p+n=34
2p=10+n
p=11 n=12 A=23
b, z=p=e=16 n=16
c,tinh phi kim

a) Có \(\left\{{}\begin{matrix}p+e+n=2p+n=52\\n=1,0588p\end{matrix}\right.=>\left\{{}\begin{matrix}p=e=17\\n=18\end{matrix}\right.\)
=> A = 17 + 18 = 35
=> X là Cl
b)
Cấu hình của Cl: 1s22s22p63s23p5
Cấu hình của ion Cl-: 1s22s22p63s23p6
c)
- Hợp chất oxit cao nhất là Cl2O7
Hiệu độ âm điện = 3,44 - 3,16 = 0,28
=> lk cộng hóa trị không phân cực
- Hợp chất khí với hidro là HCl
Hiệu độ âm điện = 3,16 - 2,2 = 0,96
=> lk cộng hóa trị phân cực

a) Cấu hình electron của Li: \(\rm 1s^22s^1\)
Do Li có 1 electron ở lớp cuối cùng, 2 lớp electron, số hiệu nguyên tử là 3
=> Thuộc ô thứ 3, chu kì 2, thuộc nhóm IA
b)
Các nguyên tử đồng vị bền: \(^6_3Li,^7_3Li\)
=> \(\overline{A}_{Li}=\dfrac{92,5.7+7,5.6}{100}=6,925\left(g\right)\)
c) \(n_{Li}=\dfrac{0,554}{6,925}=0,08\left(mol\right)\)
=> Số nguyên tử Li: \(0,08.6,02.10^{23}=4,816.10^{22}\) (nguyên tử)
=> Có 4,816.1022 quả cầu
a. Cấu hình electron của nguyên tử Li là 1s²2s¹. Li ở ô thứ 3, chu kì 2, nhóm IA trong bảng tuần hoàn
b. Nguyên tử khối trung bình của Li là 6,925
c. Trong 0,554 gam Li có khoảng 4,816 x 10²²
Cấu hình electron của nguyên tử extLi (Z = 3) là 1s^{2}2s^{1}.
Vị trí của extLi trong bảng tuần hoàn:
• Ô số 3
• Chu kì 2
• Nhóm IA
a. Li nằm ở chu kì 2, nhóm IV trong bảng tuần hoàn
b. Nguyên tử khối trung bình của Li là 6,925
c. Trong 0,554 gam Li có 4,816 x 10 quả cầu
a)- Nguyên tử Li (Z=3) có 3 electron.
-Cấu hình electoron của Li là :1s²2s¹
-Vị trí trong bảng tuần hoàn: ôthứ 3 (do Z=3).
- Chu kì 2 (do có 2 lớp electron).
-Nhóm IA (do có 1 electron hóa trị ở phân lớp s, thuộc nguyên tố s).
b)-Có hai đồng vị với số khối lần lượt là 6 và 7. Kí hiệu của chúng là ⁶Li và ⁷Li .
-Nguyên tử khối trung bình của Li là: 6,925 .
-c)Trong 0,554 gam Li có khoảng 4,816×10²² quả cầu (nguyên tử) Li.
A,Cấu hình electron của nguyên tử Li là \(1s{2}2s^{1}\). Li ở ô thứ 3, chu kì 2, nhóm IA trong bảng tuần hoàn.
a. Li nằm ở ô số 3, chu kì 2, nhóm lA là kim loại kiềm
b. À = 6 . 0,075 + 0,925
= 0,45 + 6,475 = 6,925 ≈ 6,94
c. N = n . NA = 0,0798 . 6,02 . 10³³
N ≈ 4,80 . 10²²
) Cấu hình Li laf 1s² 2s¹ Li nằm ở vị trí ô số 3 chu kì 2 nhóm IA trong bảng tuần hoàn b) 100% - 92,5% = 7,5% Nguyên tử khối trung bình của Li là 6,925 amu c) N = n x Na N = 0,08 x 6,02.10²³ N = 0,4816.10²³ N = 4,816.10²² nguyên t Trong đó 0,554 gam Li có khoảng 4,816.10²² quả cầu Li
) Cấu hình Li laf 1s² 2s¹ Li nằm ở vị trí ô số 3 chu kì 2 nhóm IA trong bảng tuần hoàn b) 100% - 92,5% = 7,5% Nguyên tử khối trung bình của Li là 6,925 amu c) N = n x Na N = 0,08 x 6,02.10²³ N = 0,4816.10²³ N = 4,816.10²² nguyên t Trong đó 0,554 gam Li có khoảng 4,816.10²² quả cầu Li
a) Cấu hình Li laf 1s² 2s¹ Li nằm ở vị trí ô số 3 chu kì 2 nhóm IA trong bảng tuần hoàn b) 100% - 92,5% = 7,5% Nguyên tử khối trung bình của Li là 6,925 amu c) N = n x Na N = 0,08 x 6,02.10²³ N = 0,4816.10²³ N = 4,816.10²² nguyên t Trong đó 0,554 gam Li có khoảng 4,816.10²² quả cầu Li
Bãi 1
CL)
_ Cấu hình decton của nguyên tử Lí :
15 25t
Vi
ti li tong bang tuch hoon
Chu kĩ 2, nhóm IA
b) Kí hiệu nguyên tử đồng vị bên của LI : ta thấy lithium co 2 đồng vị bển với số khải
là 6 và 7.
+ Kí hiệu đồng vị : 6Li
+ Kí hiệu đồng vị : tu
Nguyên tử khối trung bình của V Li là : ta thấy: Đồng vị Li : Chiếm 7,5%
Đồng vị 7 Li : chiếm 92,5 "%
Công thức tính nguyên từ thối trung bình :
106
trong đó : A =6,Ax = 7, %N = 7,5 , aM = 92,5
Ray : F = (6: 7,5)+ (7:92,5) = 6545 + 647,5
100
691,5
+0G
= 6. 925
Li
Vậy nguyên từ khối trung bình của Li là:
6,925 amu
c) Số mol Li (n)
*(Li)= M- =0,554
= n = 0,08 mc)
6,925 g09
Số nguyên tử Li (Id Natam) :
Natem
= 0,08 mo) x ( 6,02 1023) nguyên t /mal
Ma tom : 0,4816 * 1023 nguyên +
Vậy trong 0,554 gam Lí có 4,216- 10đ' quả cầu".
a) Cấu hình Li laf 1s² 2s¹ Li nằm ở vị trí ô số 3 chu kì 2 nhóm IA trong bảng tuần hoàn b) 100% - 92,5% = 7,5% Nguyên tử khối trung bình của Li là 6,925 amu c) N = n x Na N = 0,08 x 6,02.10²³ N = 0,4816.10²³ N = 4,816.10²² nguyên t Trong đó 0,554 gam Li có khoảng 4,816.10²² quả cầu Li
a) Cấu hình Li là 1s² 2s¹ Li nằm ở vị trí ô số 3 chu kì 2 nhóm IA trong bảng tuần hoàn b) 100% - 92,5% = 7,5% Nguyên tử khối trung bình của Li là 6,925 amu c) N = n x Na N = 0,08 x 6,02.10²³ N = 0,4816.10²³ N = 4,816.10²² nguyên t Trong đó 0,554 gam Li có khoảng 4,816.10²² quả cầu Li
a) Cấu hình electron và vị trí của Li trong bảng tuần hoàn
Nguyên tố lithium (Li, Z = 3) có 3 electron.
Cấu hình electron đầy đủ là: 1s22sl. •
Vị trí của Li trong bảng tuần hoàn:
b) Kí hiệu đồng vị bền và tính nguyên tử khối trung bình
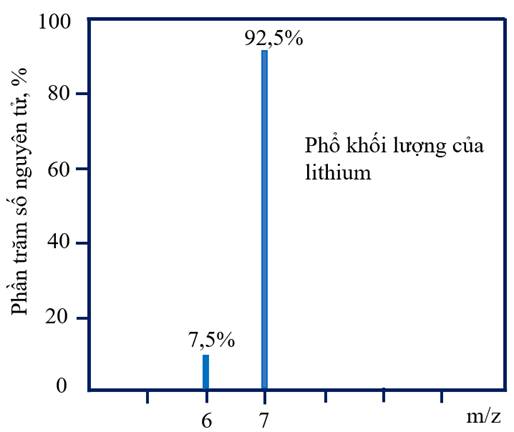
Trong tự nhiên, lithium có hai đồng vị bền. Dựa vào phổ khối lượng trên hình, hai đồng vị này có số khối (m/z) là 6 và 7, với tỉ lệ phần trăm số nguyên tử tương ứng là 7.5% và 92.5%.Kí hiệu hai đồng vị bền là:
Nguyên tử khối trung bình (A) của Li được tính bằng công thức:
A = (phn trăm đng v 1 X s khi 1) + (phn trăm đng
100%
A= (7.5% X6) + (92.5% X 7)
100%
A= 45 + 647.5 = 6.925
100
c) Tính số quả cầu (nguyên tử) Li trong
0,554 gam Li
Để tính số nguyên tử Li, ta sử dụng nguyên tử khối trung bình vừa tính được (A ~ 6.925) và hằng số
Avogadro (Ny = 6.02 × 1023). •
Bước 1: Tinh số moi của Li
Sử dụng công thức n =
m
A
trong đó m = 0,554
gam.
0.554
nLi =
~ 0.08 mol
6.925
Bước 2: Tính số nguyên tử Li
Sử dụng công thức N = n x NA•
N = 0.08 x (6.02 x 1023)
N ~ 4.816 x 1022 qu cu (nguyên t)
a)Cấu kính deckon của nguyên từ Lị :
18ª 251
trí li trong bảng tuần hoàn :
Vi
Cấu kính deckon của nguyên từ Lị :
18ª 251
trí li trong bảng tuần hoàn :
Chu kí 2, nhóm IA
b) Kĩ hiệu nguyên tử đồng vị bến của Li :
ta thấy lithium có 2 đồng vị bên với số Phôi
là 6 và 7:
+ Kí hiệu đồng vị : 6Li
+ Kí hiệu đồng vị : ti
Nguyên tử thối trung bình của V Li là :
ta thais : Dong ui i : Chiem 7,5 %
Đông vị 7Li: chiẩm 92,5 %
Công thức tính nguyên tư thối trung bình :
106
trong đó : A =6 , A, = 7, %M,= 7,5 , lM : 92,5
hãy : F. = (6• 7,51+ (7. 92,5) = V545 + 647,5
692, s
Li = 6. 925
100
10 G
Vậy nguyên từ khối trung bình của Li là:
6,925 amu
c) Số mol Li (n)
(Li) = m. : 0,554
=> n = 0,08 mol
6,925 g₽
Số nguyên tử Li (ld Na tom ):
Natem
: 0,08 mol • ( 6,02 :10ª3) nguyên t /mel
Matom : 0,4816 ° 10-3 nguyên +
Vậy trong 0,554 gam Li có 4, k16.1033 quả cầu".
a) Cấu hình electron của nguyên tử Li là \(1s^{2}2s^{1}\). Li ở ô thứ 3, chu kì 2, nhóm IA trong bảng tuần hoàn.
b)Dựa vào phổ khối lượng, có hai đồng vị bền của Li với số khối lần lượt là 6 và 7. Tỉ lệ phần trăm số nguyên tử tương ứng là 7,5% và 92,5%. Kí hiệu nguyên tử cho đồng vị là \({}_{Z}^{A}\mathbf{X}\). Với Li (\(Z=3\)), kí hiệu hai đồng vị là \({}_{3}^{6}\mathbf{Li}\) và \({}_{3}^{7}\mathbf{Li}\)
Công thức tính nguyên tử khối trung bình (\(\={A}\)): \(\={A}=\frac{(A_{1}\times \%A_{1})+(A_{2}\times \%A_{2})}{100}\) Thay số liệu vào công thức: \(\={A}=\frac{(6\times 7,5)+(7\times 92,5)}{100}\) \(\={A}=\frac{45+647,5}{100}\) \(\={A}=\frac{692,5}{100}\) \(\={A}=6,925\)
c)
Nguyên tử khối trung bình của Li là 6,925 g/mol. Số mol (n) được tính bằng công thức: \(n=\frac{m}{M}\) Trong đó \(m\) là khối lượng (0,554 g) và \(M\) là khối lượng mol (6,925 g/mol). \(n=\frac{0,554}{6,925}\approx 0,08\text{\ mol}\)
Số nguyên tử (N) được tính bằng công thức: \(N=n\times N_{A}\) Trong đó \(N_{A}\) là hằng số Avogadro, \(N_{A}\approx 6,02\times 10^{23}\) nguyên tử/mol. \(N=0,08\times (6,02\times 10^{23})\) \(N=0,4816\times 10^{23}\) \(N=4,816\times 10^{22}\text{\ nguyên\ t}\)