Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nFe = \(\frac{11,2}{56}=0,2mol\)
nAl = \(\frac{m}{27}mol\)
Cốc A : Fe + 2HCl -> FeCl2 + H2
0,2 0,2
Theo định luật bảo toàn khối lượng khối lượng HCl tăng thêm;
11,2 - 0,2.2 = 10,8 g
Cốc B : 2Al + 3H2SO4 -> Al2(SO4)3 + 2H2
\(\frac{m}{27}\) \(\frac{3m}{27.2}\)
Khi cho mg Al vào cốc B thì cốc B tăng thêm là ;
m - \(\frac{3m}{27.2}\).2 = 10,8
=> m = 12,15 g

Câu hỏi của Dịch Thiên Tổng - Hóa học lớp 8 | Học trực tuyến

\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow m_{Fe}+m_{H_2SO_4}=0,2\cdot56+0,2\cdot98=30,8g\)
Cả hai đĩa cân thăng bằng:
\(m_{Fe}+m_{H_2SO_4}=m_{Al}+m_{H_2SO_4}\)
\(\Rightarrow m_{Fe}=m_{Al}=11,2g\)

nFe =
nFe = 0.2 (mol).
nAl =
Xét thí nghiệm 1, ta có phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
0.2 0.4 0.2 0.2 (Mol)
Dung dịch sau phản ứng có chứa: FeCl2 - 0.2 mol và có thể có axit dư
Xét thí nghiệm 2, ta có phương trình phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
m/27 m/54 3m/54 (Mol)
Dung dịch sau phản ứng có chứa: Al2(SO4)3 hoặc có thể có axit còn dư
Vì sau khi phản ứng cái kim đồng hồ cân nặng vẫn ở vị trí cân bằng nên ta có thể suy luận như sau:
Khối lượng kim loại Nhôm khi cho vào cốc A trừ đi khối lượng đã mất đi là khí Hidro ở cốc A phải bằng Khối lượng kim loại Nhôm cho vào cốc B trừ đi lượng khí Hidro thoát ra ở cốc B
Vậy ta có phương trình cân bằng khối lượng của 2 cốc như sau:
Cốc A{mFe - mH2} = Cốc B{mAl - mH2}
11.2 - 0.2*2 = m - 6m/54
48m = 583.2
=>m = 12.15 (g)

Theo bài ra ta có:
nFe =
nFe = 0.2 (mol).
nAl =
Xét thí nghiệm 1, ta có phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
0.2 0.4 0.2 0.2 (Mol)
Dung dịch sau phản ứng có chứa: FeCl2 và có thể có axit dư
Xét thí nghiệm 2, ta có phương trình phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
m/27 m/54 3m/54 (Mol)
Dung dịch sau phản ứng có chứa: Al2(SO4)3 hoặc có thể có axit còn dư
Vì sau khi phản ứng cái kim đồng hồ cân nặng vẫn ở vị trí cân bằng nên ta có thể suy luận như sau:
Khối lượng kim loại Nhôm khi cho vào cốc A trừ đi khối lượng đã mất đi là khí Hidro ở cốc A phải bằng Khối lượng kim loại Nhôm cho vào cốc B trừ đi lượng khí Hidro thoát ra ở cốc B
Vậy ta có phương trình cân bằng khối lượng của 2 cốc như sau:
Cốc A{mFe - mH2} = Cốc B{mAl - mH2}
11.2 - 0.2.2 = m - 6m/54
48m = 583.2
m = 12.15 (g)

Ta có pthh Fe+HCl -> FeCl2+H2
2Al+3H2SO4-> Al2(SO4)3+ 3H2 theo pthh 56g Fe -> 127g FeCl2
vậy m g 11.2 g Fe -> 25.4g FeCl2
theo pthh 27 g Al-> 342 g Al2(SO4)3 vậy m g Al -> 38*m/3 (g) Al2(SO4)3 .Vì cho 11.2 g Fe vào cốc A và m g Al vào cốc B khi cả sắt và nhôm đều tan và cân đã ở vị trí cân bằng -> (38*m)/3=25.4-> m =2
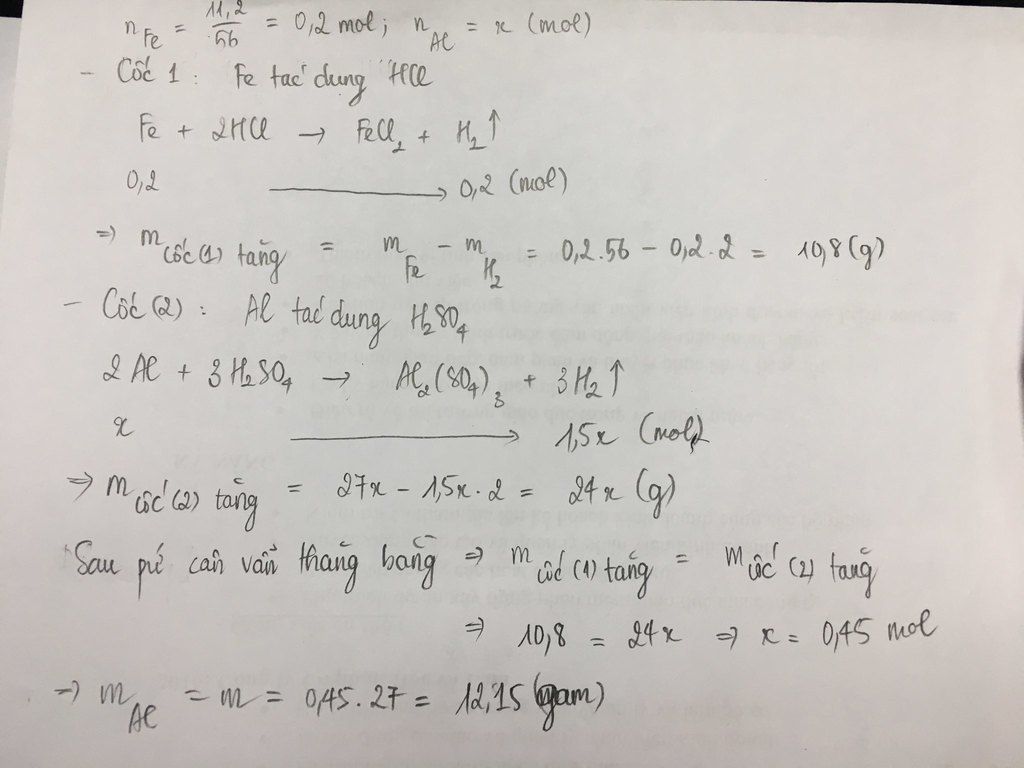
Câu hỏi đâu bạn?
trên đó
Bạn xem lại đi,tớ không thấy câu hỏi?
Sao lại thế nhỉ
Bạn xem lại có nhìn thấy câu hỏi không,mình chỉ thấy dữ liệu đề bài cho chứ không có câu hỏi,bạn có viết thiếu đề không?
ko có sao làm