Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Alcohol SVIP
I. KHÁI NIỆM VÀ DANH PHÁP
1. Khái niệm
Alcohol là hợp chất hữu cơ có nhóm hydroxy (-OH) gắn với nguyên tử carbon no.
- Alcohol được phân loại dựa vào gốc hydrocarbon liên kết với nhóm -OH:
+ Nhóm -OH liên kết với gốc hydrocarbon no thì gọi là alcohol no.
+ Nhóm -OH liên kết với gốc hydrocarbon không no thì gọi là alcohol không no.
+ Nhóm -OH liên kết với gốc hydrocarbon thơm thì gọi là alcohol thơm.
Ví dụ:

- Alcohol được phân loại dựa vào số nhóm -OH trong phân tử:
+ Alcohol có 1 nhóm -OH được gọi là alcohol đơn chức (monoalcohol).
+ Alcohol có nhiều nhóm -OH được gọi là alcohol đa chức (polyalcohol hay polyol).
Ví dụ:

- Alcohol được phân loại dựa vào bậc của nguyên tử carbon no liên kết với nhóm -OH.
+ Nếu nhóm -OH gắn vào carbon bậc I được gọi là alcohol bậc I.
+ Nếu nhóm -OH gắn vào carbon bậc II được gọi là alcohol bậc II.
+ Nếu nhóm -OH gắn vào carbon bậc III được gọi là alcohol bậc III.
Ví dụ:

Câu hỏi:
@206142746726@
Dãy đồng đẳng alcohol no, đơn chức, mạch hở có công thức tổng quát CnH2n+1OH (n ≥ 1).
- Methyl alcohol (CH3OH) và ethyl alcohol (C2H5OH) là hai alcohol đơn giản nhất.

2. Danh pháp
Tên theo danh pháp thay thế của alcohol đơn chức
Ví dụ:

Chú ý:
- Nhóm -OH được coi là nhóm thế gắn trên mạch chính.
- Ưu tiên đánh số từ phía gần nhóm -OH hơn trong mạch chính.
Câu hỏi:
@205936423814@
Tên của polyalcohol:

Ví dụ:

Ngoài ra, một số alcohol còn được gọi theo tên thông thường.
Ví dụ:

II. TÍNH CHẤT VẬT LÍ
- Ở điều kiện thường, các alcohol có thể tồn tại ở trạng thái lỏng hoặc rắn.
- Các polyalcohol (ethylene glycol, glycerol) là chất lỏng sánh, nặng hơn nước và có vị ngọt.
- Alcohol có nhiệt độ sôi cao hơn hydrocarbon và dẫn xuất halogen có phân tử khối tương đương.
- Alcohol dễ tan trong nước nhờ khả năng tạo liên kết hydrogen với nước. Khi số nguyên tử carbon tăng, độ tan giảm do gốc hydrocarbon chiếm ưu thế.
Liên kết hydrogen giữa các phân tử ethanol (a) và giữa ethanol với nước (b):

Tính chất vật lí của một số alcohol
Alcohol | tonc (oC) | tos (oC) | Độ tan ở 25 oC (g/100g nước) |
|---|---|---|---|
CH3OH | -97,7 | 64,7 | Tan vô hạn |
CH3CH2OH | -114,5 | 78,3 | Tan vô hạn |
CH3CH2CH2OH | -126,2 | 97,2 | Tan vô hạn |
CH3CH(OH)CH3 | -89,5 | 82,4 | Tan vô hạn |
CH2=CHCH2OH | -129,0 | 97,1 | Tan vô hạn |
CH3CH2CH2CH2OH | -88,6 | 117,7 | 7,4 |
CH3CH2CH2CH2CH2OH | -78,9 | 137,8 | 2,7 |
HOCH2CH2OH | -13,0 | 197,6 | Tan vô hạn |
HOCH2CH(OH)CH2OH | 18,2 | 289,0 | Tan vô hạn |
Câu hỏi:
@205936424683@
III. TÍNH CHẤT HÓA HỌC
Nguyên tử O trong nhóm -OH của alcohol có độ âm điện lớn, tạo liên kết phân cực, làm cho H hoặc nhóm -OH dễ bị tách ra trong phản ứng hóa học.
1. Phản ứng thế nguyên tử hydrogen trong nhóm -OH
Alcohol phản ứng với các kim loại mạnh (Na hoặc K) giải phóng khí H2.
Ví dụ: Ethanol phản ứng với kim loại sodium:
\(2CH_3-CH_2-OH+2Na\rightarrow2CH_3-CH_2-ONa+H_2\)
2. Phản ứng thế nhóm -OH tạo ether
Khi đun nóng ở điều kiện thích hợp với H2SO4 đặc, hai phân tử alcohol có thể kết hợp với nhau tạo thành ether.
Ví dụ:

3. Phản ứng tách H2O tạo alkene
Khi cho hơi alcohol no, đơn chức, mạch hở qua bột Al2O3 nung nóng hoặc đun nóng alcohol với H2SO4/H3PO4 đặc sẽ xảy ra phản ứng tách nước tạo thành alkene (sản phẩm chính tuân theo quy tắc Zaitsev).
Ví dụ:

4. Phản ứng oxi hóa
a. Phản ứng oxi hóa hoàn toàn
Alcohol có thể cháy trong không khí và tỏa nhiều nhiệt.
⚡ THÍ NGHIỆM 1
- Dùng que đóm đốt cháy 1 mL cồn 90o trong bát sứ.

- Ethanol cháy trong không khí tỏa nhiều nhiệt nên được dùng làm nhiên liệu trong đèn cồn, bếp cồn và phối trộn với xăng.
\(C_2H_5OH(l)+3O_2(g)\overset{t{^\circ}}{\rightarrow}2CO_2(g)+3H_2O(g)\) \(\mathrm{\Delta}_{r}H_{298}^{o}=-1300\) \(kJ\)
b. Phản ứng oxi hóa không hoàn toàn
- Alcohol bậc I bị oxi hóa bởi CuO tạo thành aldehyde.
Ví dụ:
\(CH_3CH_2OH+CuO\overset{t{^\circ}}{\rightarrow}\ CH_3CHO+Cu+H_2O\)
- Alcohol bậc II bị oxi hóa bởi CuO tạo thành ketone.
Ví dụ:
\(CH_3–CH(OH)–CH_3+CuO\overset{t{^\circ}}{\rightarrow}CH_3–CO–CH_3+Cu+H_2O\)
- Alcohol bậc III không bị oxi hóa.
Câu hỏi:
@205936439460@
5. Phản ứng riêng của glycerol
Polyalcohol có các nhóm -OH kề nhau nên phản ứng được với copper(II) hydroxide tạo thành dung dịch màu xanh lam đậm. Phản ứng này dùng để nhận biết polyalcohol có các nhóm -OH liền kề.
Ví dụ: Ethylene glycol tác dụng với Cu(OH)2:

⚡ THÍ NGHIỆM 2
- Chuẩn bị hai ống nghiệm, mỗi ống chứa 1 mL dung dịch CuSO4 2% và 1 mL dung dịch NaOH 10%, lắc đều.

- Thêm 5 giọt ethanol vào ống nghiệm (1) và 5 giọt glycerol vào ống nghiệm (2), sau đó lắc đều cả hai ống nghiệm.

Câu hỏi:
@205936442933@
IV. ỨNG DỤNG VÀ ĐIỀU CHẾ
1. Ứng dụng
Alcohol có nhiều ứng dụng quan trọng trong công nghiệp và đời sống.
- Methanol thường được dùng làm dung môi và nguyên liệu để tổng hợp hóa chất.
- Ethanol được ứng dụng để sản xuất dung môi, đồ uống có cồn, nhiên liệu trong động cơ.
- Ethylene glycol chủ yếu được dùng để sản xuất polyester và là thành phần trong dung dịch chống đông, làm mát động cơ.
- Glycerol được ứng dụng trong sản xuất nitroglycerol (dược phẩm, thuốc nổ), thuốc da, mực in và có tính giữ ẩm.

Câu hỏi:
@202836507645@
2. Điều chế
a. Điều chế ethanol
Ethanol được điều chế bằng phương pháp sinh hóa hoặc hydrate hóa ethylene.
- Ethanol được sản xuất thông qua quá trình lên men tinh bột (gạo, ngô, sắn,...), phế phẩm công nghiệp đường và chế phẩm thủy phân cellulose.
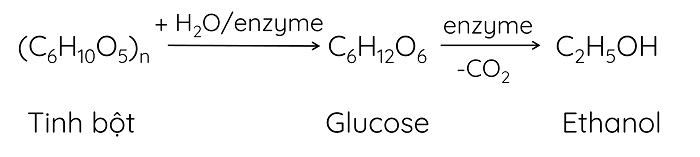
- Trong công nghiệp, ethanol được điều chế bằng cách hydrate hóa ethylene.
\(CH_2=CH_2+H_2O\overset{H_{3}PO_{4},t{^\circ}}{\rightarrow}C_2H_5OH\)
Câu hỏi:
@202836507645@
b. Điều chế glycerol
Trong công nghiệp, glycerol được sản xuất từ propylene hoặc thu được từ quá trình thủy phân chất béo.
Sơ đồ sản xuất:

Bạn có thể đăng câu hỏi về bài học này ở đây

