
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Axit ít oxi: là axit mà có ít nguyên tử O trong một gốc axit cùng phi kim.
VD: H2SO3: axit sunfurơ.
- Axit nhiều oxi: là axit mà có nhiều nguyên tử O trong một gốc axit cùng phi kim
+ Nếu như gốc axit của phi kim chỉ có 1 cái thì đó là axit nhiều oxi.
VD: H2CO3: axit cacbonic
H2SO4: axit sunfuric

| Axit ít oxi | Axit nhiều oxi |
|
- Axit ít oxi là axit mà có ít nguyên tử O trong một gốc axit cùng phi kim. VD: H2SO3: axit sunfurơ. |
- Axit nhiều oxi là axit mà có nhiều nguyên tử O trong một gốc axit cùng phi kim. - Nếu như gốc axit của phi kim chỉ có 1 cái thì đó là axit nhiều oxi. VD: H2CO3: axit cacbonic H2SO4: axit sunfuric |
bạn có thể nói cụ thể hơn và cho ví dụ kèm theo dẫn chứng đc chứ
"có ít nguyên tử o trong 1 gốc axit cùng phi kim "
"nhiêu nguyên tử o trong 1 gốc axit cùng phi kim" mình ko hiểu cái này cho lắm
thanks

| Axit ít oxi | Axit nhiều oxi |
|
- Axit ít oxi là axit mà có ít nguyên tử O trong một gốc axit cùng phi kim. VD: H2SO3: axit sunfurơ. |
- Axit nhiều oxi là axit mà có nhiều nguyên tử O trong một gốc axit cùng phi kim. - Nếu như gốc axit của phi kim chỉ có 1 cái thì đó là axit nhiều oxi. VD: H2CO3: axit cacbonic H2SO4: axit sunfuric |
Axit là 1 phân tử gồm 1 hay nhiều nguyên tử hidro liên kết với 1 gốc axit. Muốn biết axit có oxi hay không có oxi bạn chỉ việc nhìn vào gốc axit:
+ Nếu gốc axit có O : SO3 2-, SO4 2-, PO4 3-, NO3 -, CO3 2-. Tương ứng với các axit: H2SO3, H2SO4, H3PO4, HNO3, H2CO3 -> đây là những axit có oxi.
+ Nếu gốc axit không có O: Cl-, S 2-, ... Tương ứng với axit HCl, H2S -> Đây là những axit không có oxi

Đó là theo từng CTHH bạn ơi!
vd:
+ Đối với \(HNO_3\) thì đây chính là công thức có nhiều nguyên tử Oxi nhất trong các công thức tương tự \(\left(HNO_2\right)\)
+ Đối với \(H_2SO_3\) thì ngược lại, trên nó còn có \(\left(H_2SO_4\right)\) nên nó được xếp vào ít Oxi hơn

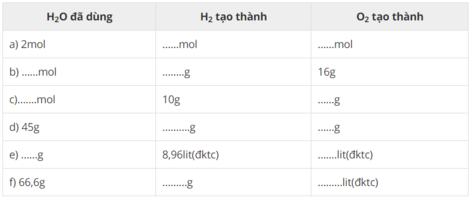
| H2O đã dùng | H2 tạo thành | O2 tạo thành |
|---|---|---|
| a) 2 mol | 2 mol | 1 mol |
| b) 1 mol | 2 g | 16g |
| c)5 mol | 10g | 80 g |
| d) 45 g | 5 g | 40 g |
| e) 7,2 g | 8,96lit(đktc) | 4,48 lit(đktc) |
| f) 66,6g | 7,4g | 41,44 lit(đktc) |
Cách tính:
a) Theo tỉ lệ phương trình: nH2O = 2 mol ⇒ nH2 = 2 mol; nO2 = 1.2/2 = 1 mol
b) nO2 = 16/32 = 0,5 mol ⇒ nH2O = nH2 = 2.nO2 = 2. 0,5 = 1 mol; mH2 = 1.2 = 2g
c) nH2 = 10/2 = 5 mol ⇒nH2O = nH2 = 5mol ; nO2 = 5.1/2 = 2,5 mol ⇒mO2 = 32. 2,5 = 80g
d) nH2O = 45/18 = 2,5 mol ⇒ nH2 = 2,5 mol ⇒ mH2 = 2,5. 2 = 5g
nO2 = 2,5.1/2 = 1,25 mol ⇒mO2 = 32. 1,25 = 40g
e) nH2 = 8,96/22,4 = 0,4 mol ⇒ nH2O = 0,4 mol ⇒ mH2O = = 0,4 .18 = 7,2 g
nO2 = 0,4.1/2 = 0,2 mol ⇒ VO2 = 0,2 . 22,4 = 4,48 l
f) nH2O = 66,6/18 = 3,7 mol ⇒ nH2 = 3,7 mol ⇒ mH2 = 3,7 .2 = 7,4 g
nO2 = 3,7.1/2 = 1,85 mol ⇒ VO2 = 41,44 lit
) Theo tỉ lệ phương trình: nH2O = 2 mol ⇒ nH2 = 2 mol; nO2 = 1.2/2 = 1 mol
b) nO2 = 16/32 = 0,5 mol ⇒ nH2O = nH2 = 2.nO2 = 2. 0,5 = 1 mol; mH2 = 1.2 = 2g
c) nH2 = 10/2 = 5 mol ⇒nH2O = nH2 = 5mol ; nO2 = 5.1/2 = 2,5 mol ⇒mO2 = 32. 2,5 = 80g
d) nH2O = 45/18 = 2,5 mol ⇒ nH2 = 2,5 mol ⇒ mH2 = 2,5. 2 = 5g
nO2 = 2,5.1/2 = 1,25 mol ⇒mO2 = 32. 1,25 = 40g
e) nH2 = 8,96/22,4 = 0,4 mol ⇒ nH2O = 0,4 mol ⇒ mH2O = = 0,4 .18 = 7,2 g
nO2 = 0,4.1/2 = 0,2 mol ⇒ VO2 = 0,2 . 22,4 = 4,48 l
f) nH2O = 66,6/18 = 3,7 mol ⇒ nH2 = 3,7 mol ⇒ mH2 = 3,7 .2 = 7,4 g
nO2 = 3,7.1/2 = 1,85 mol ⇒ VO2 = 41,44 lit
no2=3,7 .1/2=1.85

Đáp án: D
Giải thích:
Ta có: \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
Bạn tham khảo nhé!
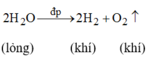
Nhiều oxi:
Tên axit = axit + tên phi kim + ic
Tên gốc = tên phi kim + at
Ít oxi:
Tên axit = axit + tên phi kim + ơ
Tên gốc = tên phi kim + it
AXIT nhiều oxi :
Tên axit = ax + tên PK + ic
Vd ; axit cabonic
axit sunfuric
Tên gốc axit = Tên PK + at
Vd ; Cabonat
sufat
Axit ít oxi ;
Tên ax = ax + tên PK + Ơ
VD : axit sunfurơ
TÊN GỐC = tên FK + it
VD : sunfit, nitric
Muốn biết axit có ít oxi hay có nhiều oxi, ta cần:
+ Học thuộc hoá trị của các nguyên tố.
+ Tìm hoá trị của phi kim hoặc kim loại.
Cách tìm: Lấy tổng số đơn vị của oxi trừ đi tổng số đơn vị của nguyên tố đứng trước.
Ví dụ: \(H_2SO_4\) thì tổng số đơn vị hóa trị của S = 4.2-2.1(vì O hóa trị II và H có hoá trị I) = 6
Đây là hóa trị cao nhất của S
Vậy đây là acid có nhiều oxi
Ví dụ 2: Với \(H_3PO_3\) cũng tương tự ta tìm được hóa trị P là 3(giá trị thấp nhất)
Vậy đây là acid có ít oxi.
Trog sgk hóa 8 có đó bạn
mình không hỏi về cách gọi tên, mình hỏi về dấu hiệu phân biệt hai loại axit này khi nhìn vào CTHH của nó cơ
Câu trả lời này hay này, mấy câu trả lời kia chung chung quá không thể phân biệt khi nhìn vào công thức hóa học, chứ đọc tên của chất nó lại bình thường. Cảm ơn bạn nhé